“铝热反应”是将单质铝与金属氧化物混合物反应获得金属单质的化学反应。在野外焊接钢轨时可利用此反应。实验室中可用如下装置实现:
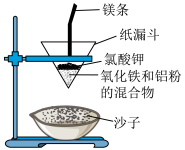
(1)写出该反应的化学方程式_______ 。
(2)实验中能观察到的现象有_______ 、_______ (例举两点)。
(3)可表示铝与氧化铁反应的热效应的图是
A .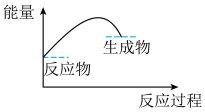 B.
B.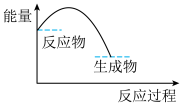 C.
C.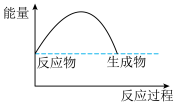
(4)工业上可用铝热反应冶炼锰、钒等金属,其原因与下列无关的是_______
(5)以下实验中属于放热反应的是_______
A.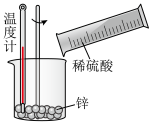 B.
B.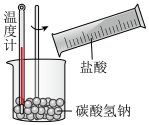 C.
C.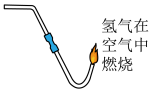

(1)写出该反应的化学方程式
(2)实验中能观察到的现象有
(3)可表示铝与氧化铁反应的热效应的图是
A .
 B.
B. C.
C.
(4)工业上可用铝热反应冶炼锰、钒等金属,其原因与下列无关的是_______
| A.铝还原性较强 | B.锰、钒熔点高 | C.铝能形成多种合金 | D.反应放出大量热 |
(5)以下实验中属于放热反应的是
A.
 B.
B. C.
C.
更新时间:2024-03-27 07:21:45
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】铝在材料、冶炼金属等方面用途非常广泛。回答下列问题:
(1)真空碳热还原Al2O3制铝是目前正在开发的一种方法。
①该法制铝时会产生一种可燃性气体,发生的总反应的化学方程式为__________ 。
②反应机理表明,碳化铝是冶炼过程中的一种中间产物,碳化铝与水反应生成Al(OH)3和一种含氢量最高的烃,碳化铝的化学式为__________ 。
(2)用如图所示的装置进行铝粉和Fe2O3的铝热反应实验。
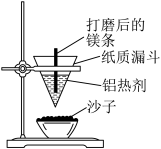
①纸质漏斗中发生的反应为________ (填“放热”或“吸热”)反应。
②实验结束后用磁铁靠近蒸发皿沙中的熔化物,能被磁铁吸引,________ (填“能”或“不能”)确认其为纯铁,说明理由:_________ 。
(3)某溶液中只含有H+、Na+、 、Ba2+、Al3+、Ag+、Cl-、
、Ba2+、Al3+、Ag+、Cl-、 、OH-、
、OH-、 、
、 、
、 中某几种,该溶液中各离子的物质的量浓度均相同。取少量溶液于试管中,滴入甲基橙,溶液呈红色,再加入NaOH溶液,溶液先变浑浊,后变澄清;另取少量溶液于试管中,加入铝片,有无色气体产生,该无色气体遇空气变为红棕色。
中某几种,该溶液中各离子的物质的量浓度均相同。取少量溶液于试管中,滴入甲基橙,溶液呈红色,再加入NaOH溶液,溶液先变浑浊,后变澄清;另取少量溶液于试管中,加入铝片,有无色气体产生,该无色气体遇空气变为红棕色。
①溶液中一定存在的阳离子为_______ (填离子符号,下同),一定存在的阴离子为_______ 。
②加入铝片时反应的离子方程式为_________ 。
(1)真空碳热还原Al2O3制铝是目前正在开发的一种方法。
①该法制铝时会产生一种可燃性气体,发生的总反应的化学方程式为
②反应机理表明,碳化铝是冶炼过程中的一种中间产物,碳化铝与水反应生成Al(OH)3和一种含氢量最高的烃,碳化铝的化学式为
(2)用如图所示的装置进行铝粉和Fe2O3的铝热反应实验。

①纸质漏斗中发生的反应为
②实验结束后用磁铁靠近蒸发皿沙中的熔化物,能被磁铁吸引,
(3)某溶液中只含有H+、Na+、
 、Ba2+、Al3+、Ag+、Cl-、
、Ba2+、Al3+、Ag+、Cl-、 、OH-、
、OH-、 、
、 、
、 中某几种,该溶液中各离子的物质的量浓度均相同。取少量溶液于试管中,滴入甲基橙,溶液呈红色,再加入NaOH溶液,溶液先变浑浊,后变澄清;另取少量溶液于试管中,加入铝片,有无色气体产生,该无色气体遇空气变为红棕色。
中某几种,该溶液中各离子的物质的量浓度均相同。取少量溶液于试管中,滴入甲基橙,溶液呈红色,再加入NaOH溶液,溶液先变浑浊,后变澄清;另取少量溶液于试管中,加入铝片,有无色气体产生,该无色气体遇空气变为红棕色。①溶液中一定存在的阳离子为
②加入铝片时反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】A、J是日常生活中常见的两种金属,这两种金属和NaOH溶液组成原电池,A作负极;F常温下是气体,各物质有以下的转化关系(部分产物及条件已略去):
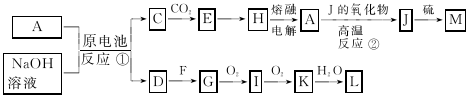
回答以下问题:
(1)A的原子结构示意图为_________________ ,M的化学式为________ 。
(2)A与NaOH溶液反应的离子方程式为_________________ 。
(3)反应②又称为________ 。
(4)含A元素的某盐X常作净水剂,X做焰色反应时,透过蓝色钴玻璃观察火焰呈紫色。X的水溶液与NaHCO3溶液混合,反应的离子方程式为_____________ 。

回答以下问题:
(1)A的原子结构示意图为
(2)A与NaOH溶液反应的离子方程式为
(3)反应②又称为
(4)含A元素的某盐X常作净水剂,X做焰色反应时,透过蓝色钴玻璃观察火焰呈紫色。X的水溶液与NaHCO3溶液混合,反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】有关物质的转化关系如下图所示(部分物质与条件已略去)。A是最常见的无色液体,B、C是常见的金属单质,D、E是气体单质,且D在空气中的含量最多,F是一种具有磁性的化合物,H是既能与强酸反应又能与强碱反应的氧化物;I具有耐高温、抗冲击、导热性好的优良性质,广泛应用于电子工业、陶瓷工业中。
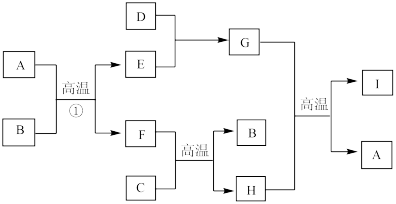
请回答下列问题:
(1) H的化学式为________________ 。
(2) D的电子式为________________ 。
(3) 写出反应①的化学方程式:________________ 。
(4) 写出G的水溶液与C的硝酸盐溶液反应的离子方程式:________________ 。

请回答下列问题:
(1) H的化学式为
(2) D的电子式为
(3) 写出反应①的化学方程式:
(4) 写出G的水溶液与C的硝酸盐溶液反应的离子方程式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】以CO2生产甲醇(CH3OH)是实现“碳中和”的重要途径。其原理是 。
。
(1)该反应的能量变化如图所示,该反应为_____ (填“放热”或“吸热”)反应。
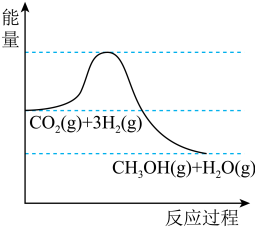
(2)恒容容器中,对于上述反应,下列措施能加快反应速率的是_____。
(3)在体积为2L的密闭容器中,充入1molCO2和3molH2,测得CO2、CH3OH的物质的量随时间变化如图。反应达到平衡状态,此时H2的转化率为_____ 。
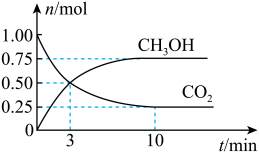
(4)在相同温度、容积不变的条件下,不能说明该反应已达平衡状态的是_____。
 。
。(1)该反应的能量变化如图所示,该反应为

(2)恒容容器中,对于上述反应,下列措施能加快反应速率的是_____。
| A.升高温度 | B.充入He |
| C.加入合适的催化剂 | D.降低压强 |
(3)在体积为2L的密闭容器中,充入1molCO2和3molH2,测得CO2、CH3OH的物质的量随时间变化如图。反应达到平衡状态,此时H2的转化率为

(4)在相同温度、容积不变的条件下,不能说明该反应已达平衡状态的是_____。
| A.CO2、H2的浓度均不再变化 |
| B.体系压强不变 |
| C.n(CH3OH)∶n(H2O)=1∶1 |
| D.H2的消耗速率与CH3OH的生成速率之比为3∶1 |
您最近一年使用:0次
【推荐2】工业生产和社会生活重要应用。
Ⅰ.工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g) CH3OH(g)。图1表示反应中能量变化;图2表示一定温度下,在容积为2L的密闭容器中加入4molH2和一定量的CO后,CO和CH3OHg的浓度随时间变化。请回答下列问题:
CH3OH(g)。图1表示反应中能量变化;图2表示一定温度下,在容积为2L的密闭容器中加入4molH2和一定量的CO后,CO和CH3OHg的浓度随时间变化。请回答下列问题:
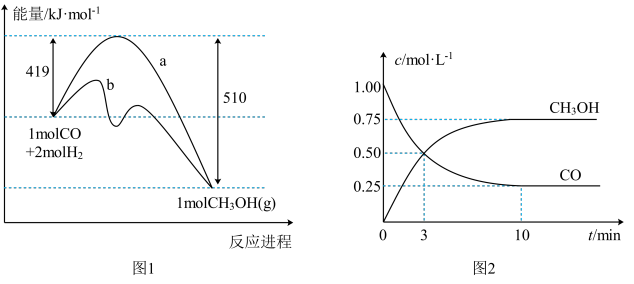
(1)在图1中,曲线___________ (填“a”或“b”)表示使用了催化剂。
(2)该反应属于___________ (填“吸热”或“放热”)反应。
(3)增大反应体系压强,则该反应化学平衡常数___________ (填“增大”“减小”或“不变”)。
(4)下列说法中正确的是___________
Ⅱ.CuSO4溶液是一种重要的铜盐试剂,在电镀、印染、颜料、农药等方面有广泛应用。某同学利用CuSO4溶液进行以下实验探究:
(5)以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是___________ (填字母)。
a.溶液中Cu2+向阳极移动
b.粗铜接电源正极,发生还原反应
c.电解后CuSO4溶液的浓度减小
d.利用阳极泥可回收Ag、Pt、Au等金属
(6)下图中,Ⅰ是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,该同学想在Ⅱ中实现铁上镀铜:
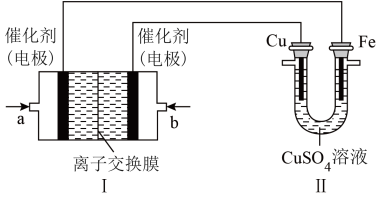
①b处通入的是___________ (填“CH4”或“O2”),a处的电极反应式为___________ 。
②当铜电极的质量减轻3.2g,则消耗的CH4在标准状况下的体积为___________ 。
Ⅰ.工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g)
 CH3OH(g)。图1表示反应中能量变化;图2表示一定温度下,在容积为2L的密闭容器中加入4molH2和一定量的CO后,CO和CH3OHg的浓度随时间变化。请回答下列问题:
CH3OH(g)。图1表示反应中能量变化;图2表示一定温度下,在容积为2L的密闭容器中加入4molH2和一定量的CO后,CO和CH3OHg的浓度随时间变化。请回答下列问题:
(1)在图1中,曲线
(2)该反应属于
(3)增大反应体系压强,则该反应化学平衡常数
(4)下列说法中正确的是___________
| A.起始充入的CO为1mol |
| B.增加CO的浓度,CO的转化率增大 |
| C.容器中压强恒定时,反应已达化学平衡状态 |
D.保持温度和密闭容器体积不变,再冲入1molCO和2molH2,再次达到平衡时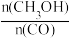 会减小 会减小 |
Ⅱ.CuSO4溶液是一种重要的铜盐试剂,在电镀、印染、颜料、农药等方面有广泛应用。某同学利用CuSO4溶液进行以下实验探究:
(5)以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是
a.溶液中Cu2+向阳极移动
b.粗铜接电源正极,发生还原反应
c.电解后CuSO4溶液的浓度减小
d.利用阳极泥可回收Ag、Pt、Au等金属
(6)下图中,Ⅰ是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,该同学想在Ⅱ中实现铁上镀铜:

①b处通入的是
②当铜电极的质量减轻3.2g,则消耗的CH4在标准状况下的体积为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】回答下列问题
(1)下列变化过程,属于放热反应的是__________ 。
①水蒸气凝固成冰;②酸碱中和反应;③浓硫酸稀释;④固体氢氧化钠溶于水;⑤甲烷燃烧;⑥食物腐败;⑦锌与稀硫酸
(2)几个有关CO的热化学方程式如下:
Ⅰ.

Ⅱ.

Ⅲ.

则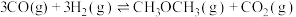

______ (用含 、
、 、
、 的代数表示)。
的代数表示)。
(3)常见有机物A、B、C、D、E的相互转化关系如图。已知D是有香味且不易溶于水的油状液体,E的产量可以用来衡量一个国家的石油化工发展水平。

请回答:
Ⅰ.A中含有的官能团名称是__________ 。
Ⅱ.B的结构筒式是__________ 。
Ⅲ.①的化学方程式是__________ 。
Ⅳ.下列说法正确的是__________ 。
a.E分子中所有原子在同一平面上
b.用饱和碳酸钠溶液除去D中混有的C
c.E在一定条件下可以形成高分子化合物。
Ⅴ.②在一定条件下能发生反应,写出反应方程式__________ ,反应类型为__________ 反应。
(1)下列变化过程,属于放热反应的是
①水蒸气凝固成冰;②酸碱中和反应;③浓硫酸稀释;④固体氢氧化钠溶于水;⑤甲烷燃烧;⑥食物腐败;⑦锌与稀硫酸
(2)几个有关CO的热化学方程式如下:
Ⅰ.


Ⅱ.


Ⅲ.


则
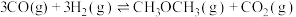

 、
、 、
、 的代数表示)。
的代数表示)。(3)常见有机物A、B、C、D、E的相互转化关系如图。已知D是有香味且不易溶于水的油状液体,E的产量可以用来衡量一个国家的石油化工发展水平。

请回答:
Ⅰ.A中含有的官能团名称是
Ⅱ.B的结构筒式是
Ⅲ.①的化学方程式是
Ⅳ.下列说法正确的是
a.E分子中所有原子在同一平面上
b.用饱和碳酸钠溶液除去D中混有的C
c.E在一定条件下可以形成高分子化合物。
Ⅴ.②在一定条件下能发生反应,写出反应方程式
您最近一年使用:0次



