某食品添加剂的主要成分为WZ(RY4)•12H2O。已知X、Y、Z、R、W为原子序数依次增大的前20号元素,X、Z的周期序数等于主族序数,Y和R位于同主族且W的焰色为紫色。下列叙述正确的是
| A.简单氢化物的沸点:Y>R |
| B.原子半径:W>R>Z>Y>X |
| C.常温下,Z、W单质都能与水发生置换反应 |
| D.R在纯净的Y2中燃烧可生成RY3 |
更新时间:2024-03-27 09:30:36
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列有几个结论是正确的
①金属性: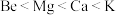
②氢化物的稳定性: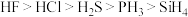
③微粒半径:
④氧化性: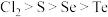
⑤酸性: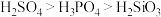
⑥沸点:
⑦离子的还原性:
①金属性:
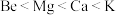
②氢化物的稳定性:
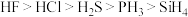
③微粒半径:

④氧化性:
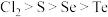
⑤酸性:
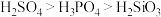
⑥沸点:

⑦离子的还原性:

| A.7个 | B.6个 | C.5个 | D.4个 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】几种短周期元素的原子半径及主要化合价见表:
下列叙述正确的是
| 元素代号 | K | L | M | Q | R | T | N |
| 原子半径/nm | 0.186 | 0.160 | 0.143 | 0.106 | 0.111 | 0.066 | 0.152 |
| 主要化合价 |  |  |  |  、 、 |  |  | +1 |
| A.Q元素的非金属性比T元素强 |
B.L的单质与 形成的化合物中,存在的化学键类型是共价键 形成的化合物中,存在的化学键类型是共价键 |
| C.Q元素的最高价氧化物为电解质,其水溶液能够导电 |
| D.元素N广泛应用于电池、贮氢等领域 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】M、W、X、Y、Z是原子序数依次增大的前四周期元素,其元素性质或基态原子结构如表。
下列说法不正确的是
| 元素 | 元素性质或原子结构 |
| M | 宇宙中含量最多的元素 |
| W | 价层电子排布是nsnnpn-1 |
| X | 最外能层中的最高能级不同轨道均填充有电子,且自旋方向相同 |
| Y | 最外层电子数是次外层电子数的一半 |
| Z | +3价阳离子中电子所占据的最高能级处于半充满状态 |
| A.原子半径:W>X>M |
| B.电负性:X>Y |
| C.元素W、Y的单质均可做半导体材料 |
| D.Z位于元素周期表的ds区 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】如图所示,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22。下列说法中,正确的是


| A.X和Y最多可形成4种化合物 |
| B.YZ2分子的空间构型是V形 |
| C.W和Z形成的共价化合物WZ4在常温下是固体 |
| D.W、X、Y、Z的最简单氢化物中,W的氢化物沸点最高 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】W、X、Y、Z均为短周期主族元素,原子序数依次增加,且原子核外L电子层的电子数分别为0、5、8、8,它们的最外层电子数之和为18。下列说法正确的是( )
| A.电负性:W>X | B.原子半径: Y>Z |
| C.氧化物的水化物的酸性:Y<Z | D.X与Y不能存在于同一离子化合物中 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】X、Y、Z、W、M为原子序数依次增大的短周期主族元素。已知:①元素对应的原子半径大小为X<Z<Y<M<W;②Y是组成有机物的必要元素;③Z与X可形成两种常见的共价化合物,与W可形成两种常见的离子化合物;④M的电子层数与最外层电子数相等。下列说法不正确的是
| A.Z与X形成的化合物的沸点偏高是因其分子间存在氢键 |
| B.YZ2为共价化合物,W2Z2既含有离子键又含有共价键 |
| C.W、M的简单离子半径为M>W |
| D.Z与M形成的化合物可作为耐高温材料 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】X、Y、Z、W是元素周期表中原子序数依次增大的四种短周期元素,其相关信息如下表:
则相关判断正确的是
元素 | 相关信息 |
X | X的最高价氧化物对应的水化物化学式为H2XO3 |
Y | Y是地壳中含量最高的元素 |
Z | Z元素的原子最外层有3个电子 |
W | W的一种核素的质量数为28,中子数为14 |
| A.W原子半径大于Z |
| B.氢元素可以与X、Y分别形成的二元化合物分子间容易形成氢键 |
| C.向Z单质与盐酸反应后的无色溶液中滴加NaOH溶液直至过量无现象 |
| D.W的单质与氢氟酸反应生成两种无色气体 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】甲、乙、丙、丁都是短周期元素,其中甲、丁在周期表中的相对位置如下表,甲原子最外层电子数是其内层电子数的2倍,乙单质在空气中燃烧发出黄色火焰,丙是地壳中含量最高的金属元素。下列判断正确的是( )
| 甲 | |||
| 丁 |
| A.原子半径:丙<丁 |
| B.甲与丁的核外电子数相差10 |
| C.甲、乙的最高价氧化物均是共价化合物 |
| D.氢氧化物碱性:乙>丙 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列叙述正确的是( )
| A.H2O 是一种非常稳定的化合物,这是由于氢键所致 |
| B.PCl3分子中三个共价键的键长,键角都相等,故为非极性分子 |
| C.NH3分子中 N 原子形成三个杂化轨道,CH4分子中 C 原子形成 4 个杂化轨道 |
| D.BeCl2为共价化合物,两个 Be-Cl 键间的夹角为180°,是由极性键构成的非极性分子 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】解释下列现象的原因不正确的是
| 选项 | 现象 | 原因 |
| A | AlCl3中含有共价键 | Al与C1元素间的电负性差值小于1.7 |
| B | HF的稳定性强于HCl | HF分子之间除了范德华力以外还存在氢键 |
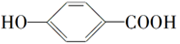
| C | 对羟基苯甲醛的熔沸点比邻羟基苯甲醛的高 | 对羟基苯甲醛形成分子间氢键,而邻羟基苯甲醛形成分子内氢键 |
| D | 碘在CCl4中的溶解度比在水中大 | 碘和CCl4均为非极性分子,水是极性分子 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次