某活动小组利用如图装置验证NO的还原性及探究工业生产硝酸的原理(装置气密性已检查完毕)。

Ⅰ.向广口瓶中通入NO并测定NO的体积。
①通入NO前,从滴定管向广口瓶中加入水;
②从导管a通入一定量的NO,并记录滴定管液面变化的示数为V L(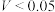 ,气体体积已换算为标准状况)。
,气体体积已换算为标准状况)。
Ⅱ.验证NO的还原性、探究工业生产硝酸的原理。
(1)停止通入NO后关闭 、
、 ,打开
,打开 ,从导管b缓缓通入
,从导管b缓缓通入 ,可观察到的现象是
,可观察到的现象是______ ,写出对应现象的化学方程式:_______ 、________ ;
(2)继续通入 ,打开
,打开 并及时调整滴定管;使液面与广口瓶中液面相平,直至广口瓶中刚好充满液体。
并及时调整滴定管;使液面与广口瓶中液面相平,直至广口瓶中刚好充满液体。
①当通入氧气的体积为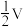 L时,广口瓶中剩余的是
L时,广口瓶中剩余的是______ 气体。
②当广口瓶中刚好充满液体时,所得溶液的物质的量浓度为______ mol⋅L 。
。

Ⅰ.向广口瓶中通入NO并测定NO的体积。
①通入NO前,从滴定管向广口瓶中加入水;
②从导管a通入一定量的NO,并记录滴定管液面变化的示数为V L(
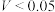 ,气体体积已换算为标准状况)。
,气体体积已换算为标准状况)。Ⅱ.验证NO的还原性、探究工业生产硝酸的原理。
(1)停止通入NO后关闭
 、
、 ,打开
,打开 ,从导管b缓缓通入
,从导管b缓缓通入 ,可观察到的现象是
,可观察到的现象是(2)继续通入
 ,打开
,打开 并及时调整滴定管;使液面与广口瓶中液面相平,直至广口瓶中刚好充满液体。
并及时调整滴定管;使液面与广口瓶中液面相平,直至广口瓶中刚好充满液体。①当通入氧气的体积为
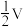 L时,广口瓶中剩余的是
L时,广口瓶中剩余的是②当广口瓶中刚好充满液体时,所得溶液的物质的量浓度为
 。
。
更新时间:2024-04-01 13:16:49
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某学习小组用如图所示的实验装置探究 能否被硝酸盐氧化(部分夹持仪器省略)。
能否被硝酸盐氧化(部分夹持仪器省略)。

回答下列问题:
(1)盛装浓硫酸的仪器名称是___________ ,该仪器使用的第一步操作是___________ 。
(2)实验时,先打开弹簧夹通一段时间 ,再滴加70%浓硫酸,目的是
,再滴加70%浓硫酸,目的是___________ 。
(3)装置A中发生反应的化学方程式为___________ 。
(4)开始实验后装置C中产生白色沉淀,实验结束后装置D试管中收集到的气体遇空气变为红棕色,则实验初期装置C中发生反应的离子方程式是___________ 。
(5)若D中试管收集到标准状况下0.224L气体,再向其中通入标准状况下___________ L  ,可使试管内充满液体。
,可使试管内充满液体。
(6)测定反应后装置B溶液中 的浓度时,只考虑
的浓度时,只考虑 与
与 的反应。用0.10
的反应。用0.10 酸性
酸性 溶液与20.00mLB中溶液中的
溶液与20.00mLB中溶液中的 反应,共消耗
反应,共消耗 溶液18.00mL,则B中
溶液18.00mL,则B中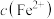 为
为___________ (保留两位小数)。
 能否被硝酸盐氧化(部分夹持仪器省略)。
能否被硝酸盐氧化(部分夹持仪器省略)。
回答下列问题:
(1)盛装浓硫酸的仪器名称是
(2)实验时,先打开弹簧夹通一段时间
 ,再滴加70%浓硫酸,目的是
,再滴加70%浓硫酸,目的是(3)装置A中发生反应的化学方程式为
(4)开始实验后装置C中产生白色沉淀,实验结束后装置D试管中收集到的气体遇空气变为红棕色,则实验初期装置C中发生反应的离子方程式是
(5)若D中试管收集到标准状况下0.224L气体,再向其中通入标准状况下
 ,可使试管内充满液体。
,可使试管内充满液体。(6)测定反应后装置B溶液中
 的浓度时,只考虑
的浓度时,只考虑 与
与 的反应。用0.10
的反应。用0.10 酸性
酸性 溶液与20.00mLB中溶液中的
溶液与20.00mLB中溶液中的 反应,共消耗
反应,共消耗 溶液18.00mL,则B中
溶液18.00mL,则B中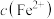 为
为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D是四种常见气体单质。E的相对分子质量比F小16,且F为红棕色。有关的转化关系如图1所示(反应条件与部分反应的生成物略去)。
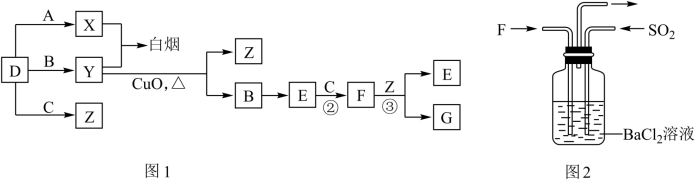
请回答下列问题:
(1)Y的化学式为______ 。
(2)Y与氧化铜反应,每生成1molB消耗3mol氧化铜,该反应的化学方程式为______ 。
(3)Y与E在一定条件下可反应生成B和Z,这是一个具有实际意义的反应,可消除E对环境的污染,该反应的化学方程式为______ 。
(4)气体F和气体SO2在通常条件下同时通入盛有BaCl2溶液的洗气瓶中(如图2所示),洗气瓶中白色沉淀是______ 。
(5)标准状况下,将NO2充满干燥烧瓶,将烧瓶倒置于水中,瓶内液面逐渐上升,假设烧瓶内溶液不扩散,则最终该溶液中溶质的物质的量浓度为______ mol·L﹣1(分数或小数表示均可)

请回答下列问题:
(1)Y的化学式为
(2)Y与氧化铜反应,每生成1molB消耗3mol氧化铜,该反应的化学方程式为
(3)Y与E在一定条件下可反应生成B和Z,这是一个具有实际意义的反应,可消除E对环境的污染,该反应的化学方程式为
(4)气体F和气体SO2在通常条件下同时通入盛有BaCl2溶液的洗气瓶中(如图2所示),洗气瓶中白色沉淀是
(5)标准状况下,将NO2充满干燥烧瓶,将烧瓶倒置于水中,瓶内液面逐渐上升,假设烧瓶内溶液不扩散,则最终该溶液中溶质的物质的量浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.氮元素在地球上含量丰富,氮及其化合物在工农业生产和生活中有着重要作用,氮氧化物也是主要的大气污染物。
(1)汽车尾气中的NO和CO气体,可以利用催化剂转化为对环境无害的两种气体,请写出该过程的化学方程式___________ ;
(2)含有NO和NO2的工业尾气可以利用NaOH溶液吸收处理。主要反应为NO+NO2+2OH-=2NO +H2O、2NO2+2OH-=NO
+H2O、2NO2+2OH-=NO +NO
+NO +H2O。
+H2O。
①下列措施不能提高尾气中NO和NO2去除率的有___________ (填标号)。
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气的过程中定期补加适量NaOH溶液
D.将尾气通入NaOH溶液的同时通入氧气
②若将NO和NO2组成的混合气体通入1L0.5mol/LNaOH溶液中,NaOH和气体恰好完全反应,吸收后的溶液经浓缩、结晶、过滤、洗涤、干燥后,得到晶体36.9g,则原混合气体中NO和NO2的物质的量之比为___________ 。
(3)用HClO也可以吸收工业尾气中的NO,HClO氧化NO生成Cl-和NO ,其离子方程式为
,其离子方程式为___________ 。
Ⅱ.该研究性学习小组同学还认为NO易与O2发生反应,应该更易被氧化。查阅资料:2NO+Na2O2=2NaNO2;2NaNO2+2HCl=2NaCl+NO2↑+NO↑+H2O;酸性条件下,NO能与MnO 反应生成NO
反应生成NO 和Mn2+。
和Mn2+。
(4)丙同学用下图所示装置(部分夹持装置略)探究NO与Na2O2的反应。___________ ;
②C中所装试剂可以是___________ ;
③充分反应后,检验D装置中产物的方法是:取D装置中产物少许,___________ ,则产物是NaNO2。
(1)汽车尾气中的NO和CO气体,可以利用催化剂转化为对环境无害的两种气体,请写出该过程的化学方程式
(2)含有NO和NO2的工业尾气可以利用NaOH溶液吸收处理。主要反应为NO+NO2+2OH-=2NO
 +H2O、2NO2+2OH-=NO
+H2O、2NO2+2OH-=NO +NO
+NO +H2O。
+H2O。①下列措施不能提高尾气中NO和NO2去除率的有
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气的过程中定期补加适量NaOH溶液
D.将尾气通入NaOH溶液的同时通入氧气
②若将NO和NO2组成的混合气体通入1L0.5mol/LNaOH溶液中,NaOH和气体恰好完全反应,吸收后的溶液经浓缩、结晶、过滤、洗涤、干燥后,得到晶体36.9g,则原混合气体中NO和NO2的物质的量之比为
(3)用HClO也可以吸收工业尾气中的NO,HClO氧化NO生成Cl-和NO
 ,其离子方程式为
,其离子方程式为Ⅱ.该研究性学习小组同学还认为NO易与O2发生反应,应该更易被氧化。查阅资料:2NO+Na2O2=2NaNO2;2NaNO2+2HCl=2NaCl+NO2↑+NO↑+H2O;酸性条件下,NO能与MnO
 反应生成NO
反应生成NO 和Mn2+。
和Mn2+。(4)丙同学用下图所示装置(部分夹持装置略)探究NO与Na2O2的反应。
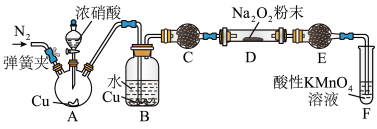
②C中所装试剂可以是
③充分反应后,检验D装置中产物的方法是:取D装置中产物少许,
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】(1)实验室用金属铜和稀硝酸制取NO的离子方程式为__ 。
(2)NO是有毒气体,某学生为防止污染,用分液漏斗和烧杯装配了一套简易的、能随开随用、随关随停的NO气体发生装置,如图甲所示。

①实验室若没有铜丝,而只有小铜粒,在使用上述装置进行实验时,可用丝状材料包裹铜粒以代替铜丝进行实验,这种丝状材料的成分可以是__ (填字母)。
A.铁 B.铝 C.铂 D.玻璃
②打开分液漏斗的活塞使反应进行,在分液漏斗中实际看到的气体是红棕色的,原因是__ (填化学方程式)。
(3)为证明铜丝与稀硝酸反应生成的确实是NO,某学生另设计了一套如图乙所示的装置制取NO。反应开始后,可以在U形管右端观察到无色的NO气体。
①长玻璃管的作用是__ 。
②让反应停止的操作方法及原因是__ 。
(4)以下收集NO气体的装置,合理的是__ (填字母)。
A. B.
B. C.
C.  D.
D. E.
E.
(2)NO是有毒气体,某学生为防止污染,用分液漏斗和烧杯装配了一套简易的、能随开随用、随关随停的NO气体发生装置,如图甲所示。

①实验室若没有铜丝,而只有小铜粒,在使用上述装置进行实验时,可用丝状材料包裹铜粒以代替铜丝进行实验,这种丝状材料的成分可以是
A.铁 B.铝 C.铂 D.玻璃
②打开分液漏斗的活塞使反应进行,在分液漏斗中实际看到的气体是红棕色的,原因是
(3)为证明铜丝与稀硝酸反应生成的确实是NO,某学生另设计了一套如图乙所示的装置制取NO。反应开始后,可以在U形管右端观察到无色的NO气体。
①长玻璃管的作用是
②让反应停止的操作方法及原因是
(4)以下收集NO气体的装置,合理的是
A.
 B.
B. C.
C.  D.
D. E.
E.
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】为了探究一氧化氮、二氧化氮、硝酸之间的相互转化,有同学设计了如下实验:如图将少量铜片装入小试管中,再加入适量稀硝酸,然后迅速将大试管倒扣在小试管外。将套好的大、小试管一起竖立在烧杯中,使水浸没大试管口。充分反应完后,通过弯玻璃管往大试管中吹人足量空气,并往烧杯中滴入几滴紫色石蕊试液。试回答:
(1)写出铜片溶于稀硝酸的离子方程式________ 。
(2)吹入空气前小试管中的现象是铜片逐渐溶解.溶液变蓝色及________ 。
(3)假设小试管中加入了 0.192g铜片和5ml浓度为2mol/L的稀硝酸,则充分反应后小试管内溶 液中NO 物质的量浓度为
物质的量浓度为________ mol/L(忽略溶液体积变化)。
(4)若将水换成氢氧化钠溶液,实验过程中生成的一种红棕色气体会与它发生反应,生成两种钠盐和水,且氧化产物与还原产物的物质的量相等,试写出该反应的离子方程式________ 。
(5)将等质里的铜片分别与等体积过量的浓、稀硝酸反应(假设溶液体积不变 所得溶液前者呈绿色,后者呈蓝色。某同学认为可能是Cu2+浓度的差异引起的,你认为是否正确?________ (填“正确”或“不正确”),理由是________ 。
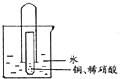
(1)写出铜片溶于稀硝酸的离子方程式
(2)吹入空气前小试管中的现象是铜片逐渐溶解.溶液变蓝色及
(3)假设小试管中加入了 0.192g铜片和5ml浓度为2mol/L的稀硝酸,则充分反应后小试管内溶 液中NO
 物质的量浓度为
物质的量浓度为(4)若将水换成氢氧化钠溶液,实验过程中生成的一种红棕色气体会与它发生反应,生成两种钠盐和水,且氧化产物与还原产物的物质的量相等,试写出该反应的离子方程式
(5)将等质里的铜片分别与等体积过量的浓、稀硝酸反应(假设溶液体积不变 所得溶液前者呈绿色,后者呈蓝色。某同学认为可能是Cu2+浓度的差异引起的,你认为是否正确?
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】亚硝酸钙[ ]是水泥混凝土外加剂的主要原料,可配制成混凝土防冻剂、钢筋阻锈剂等。某学习小组用如图所示实验装置及药品来制备亚硝酸钙(夹持装置略去)。
]是水泥混凝土外加剂的主要原料,可配制成混凝土防冻剂、钢筋阻锈剂等。某学习小组用如图所示实验装置及药品来制备亚硝酸钙(夹持装置略去)。
②酸性条件下, 能与
能与 溶液反应生成
溶液反应生成 和
和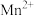 。
。
请回答下列问题:
(1)上述装置按气流方向连接的顺序为_______ (填字母)。
(2)检查装置的气密性,装入药品,实验开始前通入一段时间 ,然后关闭弹簧夹,再滴加稀硝酸,通入
,然后关闭弹簧夹,再滴加稀硝酸,通入 的作用是
的作用是______ 。
(3)A装置中反应的化学方程式为______ ,稀硝酸在反应中体现的性质为_______ 。
(4)B装置的作用是______ ;E装置的作用是______ 。
(5)C装置中反应的离子方程式为______ 。
(6)工业上可用石灰乳和硝酸工业的尾气(含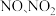 )反应,既能净化尾气,又能获得应用广泛的
)反应,既能净化尾气,又能获得应用广泛的 ,反应原理为:
,反应原理为: 。若
。若 ,则会导致
,则会导致_______ 。
 ]是水泥混凝土外加剂的主要原料,可配制成混凝土防冻剂、钢筋阻锈剂等。某学习小组用如图所示实验装置及药品来制备亚硝酸钙(夹持装置略去)。
]是水泥混凝土外加剂的主要原料,可配制成混凝土防冻剂、钢筋阻锈剂等。某学习小组用如图所示实验装置及药品来制备亚硝酸钙(夹持装置略去)。

②酸性条件下,
 能与
能与 溶液反应生成
溶液反应生成 和
和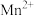 。
。请回答下列问题:
(1)上述装置按气流方向连接的顺序为
(2)检查装置的气密性,装入药品,实验开始前通入一段时间
 ,然后关闭弹簧夹,再滴加稀硝酸,通入
,然后关闭弹簧夹,再滴加稀硝酸,通入 的作用是
的作用是(3)A装置中反应的化学方程式为
(4)B装置的作用是
(5)C装置中反应的离子方程式为
(6)工业上可用石灰乳和硝酸工业的尾气(含
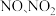 )反应,既能净化尾气,又能获得应用广泛的
)反应,既能净化尾气,又能获得应用广泛的 ,反应原理为:
,反应原理为: 。若
。若 ,则会导致
,则会导致
您最近一年使用:0次



