完全电解0.1mol/LAgNO3(水的体积变化忽略不计),所得溶液pH为
| A.1 | B.2 | C.3 | D.5 |
更新时间:2024-04-01 10:13:51
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列关于溶液酸碱性说法不正确的是
| A.25℃ pH=3的H2SO4与pH=11的氨水等体积混合后,加入酚酞溶液为无色 |
| B.25℃ 1L pH=5的氯化铵溶液,c(H+)=10-5mol·L-1,由水电离出n(OH-)=10-5mol |
| C.某温度下纯水中c(OH-)=4×10-7mol·L-1,则该温度下0.1mol·L-1的盐酸的pH=1 |
| D.313K时,Kw=2.9×10-14,则pH=7时,溶液呈碱性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】25℃时,pH=3的硝酸和pH=10的氢氧化钾溶液按照体积比为1∶9混合,混合溶液的pH为
| A.5 | B.6 | C.7 | D.8 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
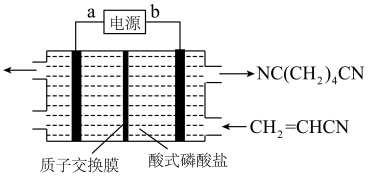
【推荐1】己二腈 是工业制造尼龙
是工业制造尼龙 的原料,现代工业常用电有机合成法制备,总反应为
的原料,现代工业常用电有机合成法制备,总反应为 ,装置如图所示。下列说法错误的是
,装置如图所示。下列说法错误的是
 是工业制造尼龙
是工业制造尼龙 的原料,现代工业常用电有机合成法制备,总反应为
的原料,现代工业常用电有机合成法制备,总反应为 ,装置如图所示。下列说法错误的是
,装置如图所示。下列说法错误的是
| A.b为电源的负极 |
B.阳极的电极反应为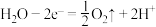 |
C.当电路中转移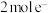 时,阳极室溶液质量减少16 g 时,阳极室溶液质量减少16 g |
D.阴极的电极反应为: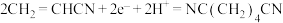 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】双极膜是一种离子交换膜,在电场作用下能将中间层的水分子解离成 和
和 ,并分别向两极移动。一种用双极膜电解法制取
,并分别向两极移动。一种用双极膜电解法制取 和丁二酸的装置如下图所示。
和丁二酸的装置如下图所示。
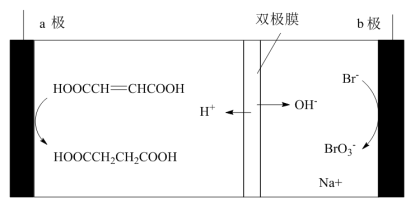
下列说法正确的是
 和
和 ,并分别向两极移动。一种用双极膜电解法制取
,并分别向两极移动。一种用双极膜电解法制取 和丁二酸的装置如下图所示。
和丁二酸的装置如下图所示。
下列说法正确的是
| A.b极应与直流电源的负极相连 |
B.a极上的电极反应为 |
C.外电路中每转移1 电子,双极膜中有1 电子,双极膜中有1 水解离 水解离 |
D.电解一段时间后,若溶液中 不足,则b极处可能有 不足,则b极处可能有 产生 产生 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】Na2SO3溶液吸收含SO2的烟气得到NaHSO3溶液(pH=6),可用图装置将吸收液再生循环利用。已知电解过程中I室内气体逐渐减少,下列有关说法错误的是


A.II室的HSO 移向I室 移向I室 |
| B.I室溶液的pH先减小后增大 |
C.III室的电极反应:2HSO +2e-=H2↑+2SO +2e-=H2↑+2SO |
| D.当电路通过1mol电子时,理论上III室得到11.2L气体(标准状况下) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在如图所示的装置中,若通直流电5min时,铜电极质量增加2.16g。下列说法错误的是


| A.电源中X电极为直流电源的负极 |
| B.pH变化:A:增大,B:减小,C:不变 |
| C.通电5min时,B中共收集224mL(标准状况下)气体,该气体是氧气 |
| D.若A中KCl足量且溶液的体积为200mL,则电解后,溶液的pH为13(假设电解前后溶液体积无变化) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】设 为阿伏加德罗常数的值,下列叙述中正确的是
为阿伏加德罗常数的值,下列叙述中正确的是
 为阿伏加德罗常数的值,下列叙述中正确的是
为阿伏加德罗常数的值,下列叙述中正确的是A. 和 和 的混合物中含有 的混合物中含有 硫,则含有的氧原子数为 硫,则含有的氧原子数为 |
B.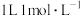 溴化铵水溶液中 溴化铵水溶液中 与 与 数目之和大于 数目之和大于 |
C.电解饱和食盐水时,若阴、阳两极产生气体的总质量为 ,则转移电子数为 ,则转移电子数为 |
D.80℃时, 的硫酸溶液中,含有的 的硫酸溶液中,含有的 数目为 数目为 |
您最近一年使用:0次


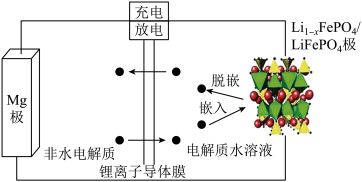
 减小
减小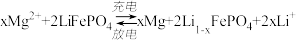 ,其装置示意图如下:(锂离子导体膜只允许Li+通过)。下列说法正确的是
,其装置示意图如下:(锂离子导体膜只允许Li+通过)。下列说法正确的是