工业上由含铜废料(含有 、
、 、
、 等)制备硝酸铜晶体的流程如下:
等)制备硝酸铜晶体的流程如下:
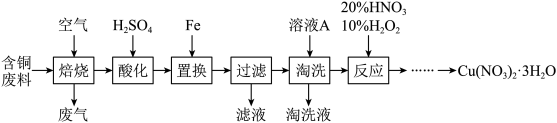
(1)“焙烧”在600℃时进行,写出 转化为
转化为 和
和 的化学方程式:
的化学方程式:________ 。
(2)“淘洗”所用的溶液A可以是________(填字母)。
(3)“反应”这一步所用 试剂是 和
和 ,反应过程中无气体生成,该反应的化学方程式:
,反应过程中无气体生成,该反应的化学方程式:________ 。
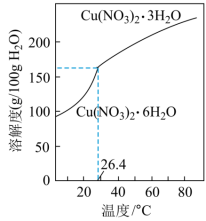
(4)根据题图分析从“反应”所得溶液中析出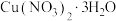 的方法是
的方法是________ 。
 、
、 、
、 等)制备硝酸铜晶体的流程如下:
等)制备硝酸铜晶体的流程如下:
(1)“焙烧”在600℃时进行,写出
 转化为
转化为 和
和 的化学方程式:
的化学方程式:(2)“淘洗”所用的溶液A可以是________(填字母)。
| A.稀硫酸 | B.浓硫酸 | C.稀硝酸 | D.浓硝酸 |
(3)“反应”这一步所用 试剂是
 和
和 ,反应过程中无气体生成,该反应的化学方程式:
,反应过程中无气体生成,该反应的化学方程式:(4)根据题图分析从“反应”所得溶液中析出
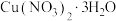 的方法是
的方法是
更新时间:2024-04-02 15:34:34
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
【推荐1】硝酸是氧化性酸,其本质是NO3-有氧化性,某课外实验小组进行了下列有关NO3-氧化性的探究(实验均在通风橱中完成)。
(1)实验Ⅰ中,铝片作____________ (填“正”或“负”)极。液面上方产生红棕色气体的化学方程式是____________ 。
(2)实验Ⅱ中电流计指针先偏向右边后偏向左边的原因是________________ 。
查阅资料:活泼金属与1 mol·L-1稀硝酸反应有H2和NH4+生成,NH4+生成的原理是产生H2的过程中NO3-被还原。
(3)用上图装置进行实验Ⅲ:溶液X为1 mol·L-1稀硝酸溶液,观察到电流计指针向右偏转。
① 反应后的溶液中含NH4+。实验室检验NH4+的方法是________ 。
② 生成NH4+的电极反应式是________ 。
(4)进一步探究碱性条件下NO3-的氧化性,进行实验Ⅳ:

① 观察到A中有NH3生成,B中无明显现象。A、B产生不同现象的解释是________ 。
②A中生成NH3的离子方程式是________ 。
(5)将铝粉加入到NaNO3溶液中无明显现象,结合实验Ⅲ和Ⅳ说明理由________ 。
| 实验装置 | 编号 | 溶液X | 实验现象 |
 | 实验Ⅰ | 6 mol·L-1稀硝酸 | 电流计指针向右偏转,铜片表面产生无色气体,在液面上方变为红棕色。 |
| 实验Ⅱ | 15 mol·L-1浓硝酸 | 电流计指针先向右偏转,很快又偏向左边,铝片和铜片表面产生红棕色气体,溶液变为绿色。 |
(1)实验Ⅰ中,铝片作
(2)实验Ⅱ中电流计指针先偏向右边后偏向左边的原因是
查阅资料:活泼金属与1 mol·L-1稀硝酸反应有H2和NH4+生成,NH4+生成的原理是产生H2的过程中NO3-被还原。
(3)用上图装置进行实验Ⅲ:溶液X为1 mol·L-1稀硝酸溶液,观察到电流计指针向右偏转。
① 反应后的溶液中含NH4+。实验室检验NH4+的方法是
② 生成NH4+的电极反应式是
(4)进一步探究碱性条件下NO3-的氧化性,进行实验Ⅳ:

① 观察到A中有NH3生成,B中无明显现象。A、B产生不同现象的解释是
②A中生成NH3的离子方程式是
(5)将铝粉加入到NaNO3溶液中无明显现象,结合实验Ⅲ和Ⅳ说明理由
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】Cu—Fe合金由于长时间置于空气中,表面产生了一层氧化膜(成分为Fe2O3和CuO),现进行如下实验(以下气体体积均在标况下测得):
①将此合金块5.76g置于烧杯中,然后将稀H2SO4逐渐缓慢加入至过量,收集产生的气体为672mL,过滤得浅绿色溶液A,还有滤渣B。
②将滤渣B投入到一定浓度的HNO3中,完全溶解,得NO、NO2的混合气体896mL,经测定,同温同压下此混合气体对氢气的相对密度为17。
③将①中所得滤液加入到同浓度足量的HNO3中,用排水法收集一烧瓶气体,再向烧瓶中通入224mL O2,气体恰好完全溶于水。
(1)A中存在的阳离子有________________ ;
(2)896mL混合气体中NO、NO2的物质的量之比为______________ ;
(3)B的单质为______________ ,质量为_________________ g;
(4)③中被HNO3氧化了的阳离子的物质的量为______________ mol;
(5)此合金块中氧元素的质量为_______________ g。
①将此合金块5.76g置于烧杯中,然后将稀H2SO4逐渐缓慢加入至过量,收集产生的气体为672mL,过滤得浅绿色溶液A,还有滤渣B。
②将滤渣B投入到一定浓度的HNO3中,完全溶解,得NO、NO2的混合气体896mL,经测定,同温同压下此混合气体对氢气的相对密度为17。
③将①中所得滤液加入到同浓度足量的HNO3中,用排水法收集一烧瓶气体,再向烧瓶中通入224mL O2,气体恰好完全溶于水。
(1)A中存在的阳离子有
(2)896mL混合气体中NO、NO2的物质的量之比为
(3)B的单质为
(4)③中被HNO3氧化了的阳离子的物质的量为
(5)此合金块中氧元素的质量为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】某校化学实验小组为了证明铜与稀硝酸反应产生一氧化氮,用如图所示装置进行实验(加热装置和夹持装置均已略去,装置气密性良好,F是用于鼓入空气的双连打气球)。

实验步骤与现象如下:
Ⅰ.将B装置下移,使碳酸钙与稀硝酸接触,产生气体;
Ⅱ.当C装置中产生白色沉淀时,立刻将B装置上提;
Ⅲ.将A装置中铜丝放入稀硝酸中,给A装置微微加热,A装置中产生无色气体,E装置中开始时出现浅红棕色气体;
Ⅳ.用F装置向E装置中鼓入空气,E装置中气体颜色逐渐加深;一段时间后,装置C中白色沉淀溶解。
回答下列问题:
(1)写出操作Ⅰ中的化学方程式:____________________ 。
(2)C装置中白色沉淀的化学式是______ 。操作Ⅱ中当C装置中产生白色沉淀时立刻将B装置上提的原因是____________________ 。
(3)写出操作Ⅲ中A装置中产生无色气体的化学方程式:____________________ 。
(4)E装置内气体颜色逐渐加深的原因是____________________ 。
(5)若该小组另取30 mL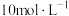 的硝酸溶液与上述实验剩余的6.4 g铜丝在加热条件下反应,恰好完全反应,产生一定量NO和NO2的混合气体(反应过程中溶液体积变化忽略不计),则反应后的溶液中硝酸铜的物质的量浓度为
的硝酸溶液与上述实验剩余的6.4 g铜丝在加热条件下反应,恰好完全反应,产生一定量NO和NO2的混合气体(反应过程中溶液体积变化忽略不计),则反应后的溶液中硝酸铜的物质的量浓度为______  (保留3位有效数字)。混合气体中NO的物质的量为
(保留3位有效数字)。混合气体中NO的物质的量为______ mol。

实验步骤与现象如下:
Ⅰ.将B装置下移,使碳酸钙与稀硝酸接触,产生气体;
Ⅱ.当C装置中产生白色沉淀时,立刻将B装置上提;
Ⅲ.将A装置中铜丝放入稀硝酸中,给A装置微微加热,A装置中产生无色气体,E装置中开始时出现浅红棕色气体;
Ⅳ.用F装置向E装置中鼓入空气,E装置中气体颜色逐渐加深;一段时间后,装置C中白色沉淀溶解。
回答下列问题:
(1)写出操作Ⅰ中的化学方程式:
(2)C装置中白色沉淀的化学式是
(3)写出操作Ⅲ中A装置中产生无色气体的化学方程式:
(4)E装置内气体颜色逐渐加深的原因是
(5)若该小组另取30 mL
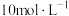 的硝酸溶液与上述实验剩余的6.4 g铜丝在加热条件下反应,恰好完全反应,产生一定量NO和NO2的混合气体(反应过程中溶液体积变化忽略不计),则反应后的溶液中硝酸铜的物质的量浓度为
的硝酸溶液与上述实验剩余的6.4 g铜丝在加热条件下反应,恰好完全反应,产生一定量NO和NO2的混合气体(反应过程中溶液体积变化忽略不计),则反应后的溶液中硝酸铜的物质的量浓度为 (保留3位有效数字)。混合气体中NO的物质的量为
(保留3位有效数字)。混合气体中NO的物质的量为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
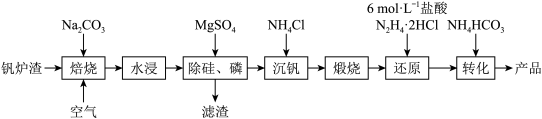
【推荐1】工业上以钒炉渣(主要含V2O5,还有少量SiO2、P2O5等杂质)为原料可以制备氧钒碱式碳酸铵晶([NH4)5(VO)6(CO3)4(OH)9·10H2O],其生产工艺流程如下:_____________ 。
(2)“沉钒”得到偏钒酸铵(NH4VO3),若滤液中c( )=0.lmol/L,为使钒元素的沉降率达到98%,至少应调节c(
)=0.lmol/L,为使钒元素的沉降率达到98%,至少应调节c( )为
)为_____ mol/L.[已知Ksp(NH4VO3)=0.6×10-3]
(3)“还原”V2O5过程中,生成VOCl2和一种无色无污染的气体,该反应的化学方程式为_____________ ,用浓盐酸与V2O5反应也可以制得VOCl2,该方法的缺点是___________ 。
(4)称量ag产品于于锥形瓶中,用20mL蒸馏水与30mL稀硫酸溶解后,加入0.02mol/LKMnO4溶液至稍过量,充分反应后继续滴加1%的NaNO2溶液至稍过量,再用尿素除去过量NaNO2,最后用cmol/L(NH4)2Fe(SO4)2标准溶液滴定至终点,消耗标准溶液的体积为bmL。(已知滴定反应为 +Fe2++2H+=
+Fe2++2H+= +Fe3++H2O)
+Fe3++H2O)
①KMnO4溶液的作用是___________________________ 。
②粗产品品中钒的质量分数表达式为_____________________ (以VO2计)。
③若(NH4)2Fe(SO4)2标准溶液部分变质,会使测定结果________ (填“偏高”、“偏低”或“无影响”)。
(2)“沉钒”得到偏钒酸铵(NH4VO3),若滤液中c(
 )=0.lmol/L,为使钒元素的沉降率达到98%,至少应调节c(
)=0.lmol/L,为使钒元素的沉降率达到98%,至少应调节c( )为
)为(3)“还原”V2O5过程中,生成VOCl2和一种无色无污染的气体,该反应的化学方程式为
(4)称量ag产品于于锥形瓶中,用20mL蒸馏水与30mL稀硫酸溶解后,加入0.02mol/LKMnO4溶液至稍过量,充分反应后继续滴加1%的NaNO2溶液至稍过量,再用尿素除去过量NaNO2,最后用cmol/L(NH4)2Fe(SO4)2标准溶液滴定至终点,消耗标准溶液的体积为bmL。(已知滴定反应为
 +Fe2++2H+=
+Fe2++2H+= +Fe3++H2O)
+Fe3++H2O)①KMnO4溶液的作用是
②粗产品品中钒的质量分数表达式为
③若(NH4)2Fe(SO4)2标准溶液部分变质,会使测定结果
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】工业上利用软锰矿(主要成分为 ,还含有
,还含有 、
、 、
、 、
、 、
、 、
、 等杂质)与纤维素制备
等杂质)与纤维素制备 ,工艺流程如图1所示。
,工艺流程如图1所示。

(1)相对于“ 酸浸法”,利用纤维素“酸浸”,除了原料来源丰富、耗能低外,还具有的优点是
酸浸法”,利用纤维素“酸浸”,除了原料来源丰富、耗能低外,还具有的优点是_______ (答出两点)。
(2)“酸浸”时,由纤维素水解得到的葡萄糖与软锰矿反应。完成葡萄糖与软锰矿反应的离子方程式:_______ 。_______ _______
_______ _______=_______
_______=_______ _______
_______ _______。
_______。
(3)相关离子形成氢氧化物沉淀的 范围如表所示。
范围如表所示。
滤渣2的主要成分是_______ 。
(4)“净化”时,加入 、
、 是为了将
是为了将 、
、 转化为
转化为 和
和 沉淀除去,还能除去
沉淀除去,还能除去_______ (填元素符号)。
(5)“沉锰”时,主要生成 和
和 沉淀,其中生成
沉淀,其中生成 沉淀的离子方程式为
沉淀的离子方程式为_______ 。
(6)“氧化”时,氧化时间对产品中的锰含量及溶液 的影响如图2所示。最合理的氧化时间为
的影响如图2所示。最合理的氧化时间为_______  ;下列说法错误的是
;下列说法错误的是_______ (填标号)。

A.前15min,主要发生的反应是6Mn(OH)2+O2=2Mn3O4+6H2O,pH下降较慢
B.15~150min,主要发生的反应是3Mn2(OH)2SO4+O2=2Mn3O4+6H++3SO ,pH下降较快
,pH下降较快
C.150min之后,pH趋于稳定,则Mn2(OH)2SO4已完全氧化
D.250min后,继续通入空气,可能将产品氧化生成Mn2O3及MnO2,使产品中的锰含量下降
 ,还含有
,还含有 、
、 、
、 、
、 、
、 、
、 等杂质)与纤维素制备
等杂质)与纤维素制备 ,工艺流程如图1所示。
,工艺流程如图1所示。
(1)相对于“
 酸浸法”,利用纤维素“酸浸”,除了原料来源丰富、耗能低外,还具有的优点是
酸浸法”,利用纤维素“酸浸”,除了原料来源丰富、耗能低外,还具有的优点是(2)“酸浸”时,由纤维素水解得到的葡萄糖与软锰矿反应。完成葡萄糖与软锰矿反应的离子方程式:
 _______
_______ _______=_______
_______=_______ _______
_______ _______。
_______。(3)相关离子形成氢氧化物沉淀的
 范围如表所示。
范围如表所示。| 金属离子 |  |  |  |  |  |
开始沉淀时 | 1.6 | 3.0 | 8.9 | 6.0 | 8.1 |
完全沉淀时 | 2.8 | 4.7 | 10.9 | 8.0 | 10.1 |
滤渣2的主要成分是
(4)“净化”时,加入
 、
、 是为了将
是为了将 、
、 转化为
转化为 和
和 沉淀除去,还能除去
沉淀除去,还能除去(5)“沉锰”时,主要生成
 和
和 沉淀,其中生成
沉淀,其中生成 沉淀的离子方程式为
沉淀的离子方程式为(6)“氧化”时,氧化时间对产品中的锰含量及溶液
 的影响如图2所示。最合理的氧化时间为
的影响如图2所示。最合理的氧化时间为 ;下列说法错误的是
;下列说法错误的是
A.前15min,主要发生的反应是6Mn(OH)2+O2=2Mn3O4+6H2O,pH下降较慢
B.15~150min,主要发生的反应是3Mn2(OH)2SO4+O2=2Mn3O4+6H++3SO
 ,pH下降较快
,pH下降较快C.150min之后,pH趋于稳定,则Mn2(OH)2SO4已完全氧化
D.250min后,继续通入空气,可能将产品氧化生成Mn2O3及MnO2,使产品中的锰含量下降
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】某研究小组利用氮气、氧化铝和活性炭制取氮化铝,设计如图1所示实验装置。

请回答:
(1)图1中用饱和NaNO2溶液与NH4Cl溶液加热制取氮气,该离子方程式为____ 。
(2)图1装置中各仪器导管口连接的顺序是(可重复使用,用小写字母a→g填写):_______ ;
导管A的作用是_________________________________________ 。
(3)按要求连接好实验装置后,接下来的操作是_____________________ 。
(4)反应结束后,某同学用图2装置进行实验来测定 氮化铝样品的质量分数(实验中导管体积忽略不计)。
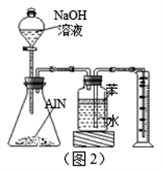
①氮化铝与过量的NaOH溶液反应生成氨气化学反应方程式为_______________ ;
② 集气瓶中的苯的作用是____________ ;集气瓶中的液体没有装满,则实验测得NH3的体积将__________ (填“偏大” “偏小”或“不变”)。
③若实验中称取氮化铝样品的质量为8.0 g,测得氨气的体积2.8 L(标准状况),则样品中AlN的质量分数为___________ (保留3位有效数字)。

请回答:
(1)图1中用饱和NaNO2溶液与NH4Cl溶液加热制取氮气,该离子方程式为
(2)图1装置中各仪器导管口连接的顺序是(可重复使用,用小写字母a→g填写):
导管A的作用是
(3)按要求连接好实验装置后,接下来的操作是
(4)反应结束后,某同学用图2装置进行实验来测定 氮化铝样品的质量分数(实验中导管体积忽略不计)。

①氮化铝与过量的NaOH溶液反应生成氨气化学反应方程式为
② 集气瓶中的苯的作用是
③若实验中称取氮化铝样品的质量为8.0 g,测得氨气的体积2.8 L(标准状况),则样品中AlN的质量分数为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐1】在金属活动顺序中,铁、铝均比铜活泼,但常温下,将铁棒或铝棒插入浓硝酸中,你观察不到任何现象,因为发生了钝化;将铜棒插入投浓硝酸中,却剧烈反应,放热,且产生红棕色的气体。铁、铝插入稀硝酸或稀硫酸中时,也不会发生钝化。
(1)钝化是___________ (填“物理”“化学”)变化。
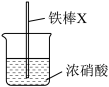
(2)如图所示,常温下能说明铁棒X已被钝化的是___________
(3)将铜投入一定量浓硝酸中完全溶解,产生的氮氧化物气体用500 mL 2 mol/L NaOH溶液恰好完全吸收,得到含0.2 mol  和若干摩尔
和若干摩尔 ,则___________
,则___________
(4)实验证明: 溶液呈酸性,可与
溶液呈酸性,可与 反应。现向两份相同的
反应。现向两份相同的 溶液中,分别滴入物质的量浓度相等的
溶液中,分别滴入物质的量浓度相等的 、
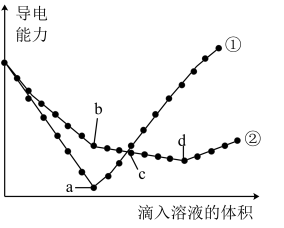
、 溶液,测得其导电能力随滴入溶液体积变化的曲线如图所示。对此进行的分析判断错误的是___________
溶液,测得其导电能力随滴入溶液体积变化的曲线如图所示。对此进行的分析判断错误的是___________
(1)钝化是
(2)如图所示,常温下能说明铁棒X已被钝化的是___________

| A.将铁棒X洗净,浸泡于浓硫酸,无变化 |
| B.将铁棒X洗净,浸泡于硫酸铜溶液中,无红色物析出 |
| C.将铁棒X洗净,浸泡于稀硫酸中,无气泡产生 |
| D.将铁棒X洗净,浸泡于氢氧化钠溶液中,无变化 |
 和若干摩尔
和若干摩尔 ,则___________
,则___________A.产生气体一定含 ,可能含NO和 ,可能含NO和 , , |
B.产生的气体与8.96 L  混合后通入水中,恰好转化为 混合后通入水中,恰好转化为 |
| C.消耗铜的质量为5.12 g |
| D.原浓硝酸中可能含2.6 mol溶质 |
 溶液呈酸性,可与
溶液呈酸性,可与 反应。现向两份相同的
反应。现向两份相同的 溶液中,分别滴入物质的量浓度相等的
溶液中,分别滴入物质的量浓度相等的 、
、 溶液,测得其导电能力随滴入溶液体积变化的曲线如图所示。对此进行的分析判断错误的是___________
溶液,测得其导电能力随滴入溶液体积变化的曲线如图所示。对此进行的分析判断错误的是___________
A.②代表滴加 溶液的变化曲线 溶液的变化曲线 |
B.b点,溶液中大量存在的离子是 、 、 |
C.c点,两溶液中含有相同量的 |
| D.a、d两点对应的溶液均显中性 |
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】甲、乙两同学用如图所示装置进行实验,探究硝酸与铁反应的产物。

【文献记载】
①在浓硝酸和活泼金属反应过程中,随着硝酸浓度降低,其生成的产物有 、
、 、
、 价等氮的化合物。
价等氮的化合物。
② (棕色);
(棕色);
③ 和NO都能被
和NO都能被 氧化吸收。
氧化吸收。
甲的实验操作和现象记录如下,请回答下列问题:
(1)滴入浓硝酸加热前,没有明显现象的原因是________ 。
(2)检验是否生成 价氮的化合物,应进行的实验操作是
价氮的化合物,应进行的实验操作是________ 。
(3)甲取少量B中溶液,加热,实验现象是棕色溶液变浅,无色气体逸出,且在空气中变为红棕色。请用化学方程式结合适当文字解释产生该现象的原因:________ 。甲依据该现象得出的结论是A中有NO生成。
(4)乙认为甲得出A中有NO生成的证据不足。为获取充足的证据,乙仍采用该装置和操作进行对照实验。乙作出的改变是________ ,证明有NO生成的实验现象是________ 。
(5)向含有 和
和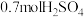 的混合溶液中逐渐加入铁粉至过量,溶液中金属正离子a、b与所加铁粉的物质的量的关系如图所示。(已知稀硝酸的还原产物只有NO)。
的混合溶液中逐渐加入铁粉至过量,溶液中金属正离子a、b与所加铁粉的物质的量的关系如图所示。(已知稀硝酸的还原产物只有NO)。
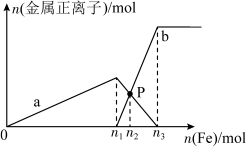
【注意】本题要求书写解题过程,仅有答案不得分。
①a表示的是________ 的变化曲线。
②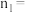
________ ,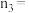
________ 。(结果保留两位小数)
③向P点溶液中加入铜粉,最多可溶解铜粉的质量是________ g。

【文献记载】
①在浓硝酸和活泼金属反应过程中,随着硝酸浓度降低,其生成的产物有
 、
、 、
、 价等氮的化合物。
价等氮的化合物。②
 (棕色);
(棕色);③
 和NO都能被
和NO都能被 氧化吸收。
氧化吸收。甲的实验操作和现象记录如下,请回答下列问题:
| 实验操作 | 实验现象 |
打开弹簧夹,通入一段时间 ,关闭弹簧夹。 ,关闭弹簧夹。 | |
| 打开分液漏斗活塞,将浓硝酸缓慢滴入烧瓶中,关闭活塞。 | 无明显现象 |
| 加热烧瓶,反应开始后停止加热。 | ①A中有红棕色气体产生,一段时间后,气体颜色逐渐变浅;B中溶液变棕色;C中溶液紫色变浅。 ②反应停止后,A中无固体剩余。 |
(2)检验是否生成
 价氮的化合物,应进行的实验操作是
价氮的化合物,应进行的实验操作是(3)甲取少量B中溶液,加热,实验现象是棕色溶液变浅,无色气体逸出,且在空气中变为红棕色。请用化学方程式结合适当文字解释产生该现象的原因:
(4)乙认为甲得出A中有NO生成的证据不足。为获取充足的证据,乙仍采用该装置和操作进行对照实验。乙作出的改变是
(5)向含有
 和
和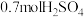 的混合溶液中逐渐加入铁粉至过量,溶液中金属正离子a、b与所加铁粉的物质的量的关系如图所示。(已知稀硝酸的还原产物只有NO)。
的混合溶液中逐渐加入铁粉至过量,溶液中金属正离子a、b与所加铁粉的物质的量的关系如图所示。(已知稀硝酸的还原产物只有NO)。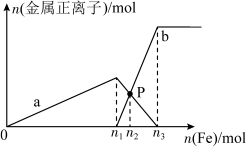
【注意】本题要求书写解题过程,仅有答案不得分。
①a表示的是
②
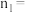
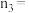
③向P点溶液中加入铜粉,最多可溶解铜粉的质量是
您最近一年使用:0次



