请根据硫元素的价类二维图,回答下列问题:___________ (填化学式)。
(2)宋代著名法医学家宋慈的 洗冤集录
洗冤集录 中有关于“银针验毒”的记载,银针主要用于检验是否有含硫元素的有毒物质。其反应原理之一为:Ag + X + O2 →Ag2S + H2O(反应未配平),已知:Ag2S为一种不溶于水的灰黑色固体。以下有关说法
中有关于“银针验毒”的记载,银针主要用于检验是否有含硫元素的有毒物质。其反应原理之一为:Ag + X + O2 →Ag2S + H2O(反应未配平),已知:Ag2S为一种不溶于水的灰黑色固体。以下有关说法错误 的是___________(填字母)。
(3)Y转化为Z可以选择下列试剂___________ 。
A.酸性KMnO4溶液 B.FeCl2溶液 C.NaOH溶液 D.X的水溶液
写出你所选试剂将Y转化为Z的离子方程式___________ 。
(4)若N是CuSO4,某同学设计了甲和乙两种方法制备:
甲: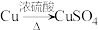 乙:
乙:
①写出甲方法反应的化学方程式:___________ 。
②甲和乙方法更合理的是___________ (填“甲”或“乙”),理由是___________ (答两点)。
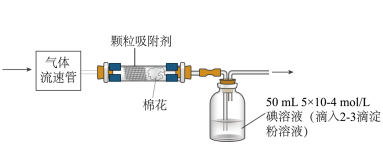
(5)已知空气中SO2的最大允许排放浓度不得超过0.02 mg•L-1,可通过下列装置定量分析空气中SO2的含量。___________ mg•L-1(结果精确到0.001)。

(2)宋代著名法医学家宋慈的
 洗冤集录
洗冤集录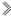 中有关于“银针验毒”的记载,银针主要用于检验是否有含硫元素的有毒物质。其反应原理之一为:Ag + X + O2 →Ag2S + H2O(反应未配平),已知:Ag2S为一种不溶于水的灰黑色固体。以下有关说法
中有关于“银针验毒”的记载,银针主要用于检验是否有含硫元素的有毒物质。其反应原理之一为:Ag + X + O2 →Ag2S + H2O(反应未配平),已知:Ag2S为一种不溶于水的灰黑色固体。以下有关说法| A.当银针变黑时,说明所检验的物质中可能有毒 |
| B.银针验毒时,Ag被氧化 |
| C.X在上述验毒反应中作还原剂 |
| D.上述验毒反应中氧化剂和还原剂的物质的量之比为4∶1 |
(3)Y转化为Z可以选择下列试剂
A.酸性KMnO4溶液 B.FeCl2溶液 C.NaOH溶液 D.X的水溶液
写出你所选试剂将Y转化为Z的离子方程式
(4)若N是CuSO4,某同学设计了甲和乙两种方法制备:
甲:
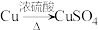 乙:
乙:
①写出甲方法反应的化学方程式:
②甲和乙方法更合理的是
(5)已知空气中SO2的最大允许排放浓度不得超过0.02 mg•L-1,可通过下列装置定量分析空气中SO2的含量。
更新时间:2024-04-29 08:29:32
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
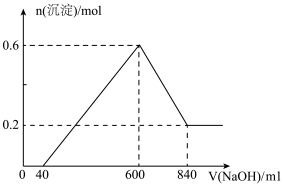
【推荐1】将一定质量的镁铝合金投入一定浓度的200mL盐酸中,使金属全部溶解,向所得溶液中滴加3.0 mol·L-1的NaOH溶液至过量,生成沉淀的物质的量与加入NaOH溶液体积的关系如图所示。
计算:
(1)原合金中镁和铝的物质的量_______ 。
(2)反应中生成的H2在标况下的体积_______ 。
(3)盐酸中HCl的物质的量浓度_______ 。

计算:
(1)原合金中镁和铝的物质的量
(2)反应中生成的H2在标况下的体积
(3)盐酸中HCl的物质的量浓度
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】氯酸是一种强酸,浓度超过40%时会发生分解,反应可表示为
a HClO3→ bO2↑+ c Cl2↑+ d HClO4+ e H2O,
(1)该反应的氧化产物是__________________________ 。
(2)若化学计量数a=8,b=3,则c=___ ;d= ___ ;你判断的依据是_______________ 。
(3)若氯酸分解所得混合气体,经干燥后,lmol混合气体质量为51.5g,请配平该反应方程式:___HClO3→___O2↑+ ___Cl2↑+ ___ HClO4+ ___ H2O___
a HClO3→ bO2↑+ c Cl2↑+ d HClO4+ e H2O,
(1)该反应的氧化产物是
(2)若化学计量数a=8,b=3,则c=
(3)若氯酸分解所得混合气体,经干燥后,lmol混合气体质量为51.5g,请配平该反应方程式:___HClO3→___O2↑+ ___Cl2↑+ ___ HClO4+ ___ H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】I.高铁酸钾 是一种新型、高效、多功能绿色水处理剂,比
是一种新型、高效、多功能绿色水处理剂,比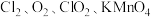 氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入
氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入 至饱和,使高铁酸钾析出。
至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为: ,该反应中
,该反应中 做
做_______ (填“氧化剂”、“还原剂”)。
(2)湿法制备高铁酸钾的反应体系中有六种微粒: 。
。
①碱性条件下,氧化剂和还原剂的物质的量的比为3∶2发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:_______ 。
②若反应过程中转移了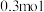 电子,则还原产物的物质的量为
电子,则还原产物的物质的量为_______  。
。
II.将某铁铝合金均分为两份,一份加入足量盐酸,另一份加入足量 溶液,同温同压下产生的气体体积比为5∶4。
溶液,同温同压下产生的气体体积比为5∶4。
(3)样品中铁、铝物质的量之比为_______ 。
 是一种新型、高效、多功能绿色水处理剂,比
是一种新型、高效、多功能绿色水处理剂,比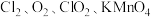 氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入
氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入 至饱和,使高铁酸钾析出。
至饱和,使高铁酸钾析出。(1)干法制备高铁酸钠的主要反应为:
 ,该反应中
,该反应中 做
做(2)湿法制备高铁酸钾的反应体系中有六种微粒:
 。
。①碱性条件下,氧化剂和还原剂的物质的量的比为3∶2发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:
②若反应过程中转移了
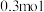 电子,则还原产物的物质的量为
电子,则还原产物的物质的量为 。
。II.将某铁铝合金均分为两份,一份加入足量盐酸,另一份加入足量
 溶液,同温同压下产生的气体体积比为5∶4。
溶液,同温同压下产生的气体体积比为5∶4。(3)样品中铁、铝物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)下列物质中:①NaCl溶液 ②氢氧化钠 ③二氧化碳 ④金刚石⑤水 ⑥酒精,属于电解质的是__________ ;非电解质的是_________ 。(请用序号填空)
(2)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,也永远会激励着我们去奋发图强。黑火药在发生爆炸时,发生如下的反应:2KNO3+C+S=K2S+2NO2↑+CO2↑。其中被还原的元素是_____ ,还原剂是_______ ,还原产物是______ 。
(3)161g Na2SO4·10H2O中所含的Na+的物质的量是_______ SO42—的质量是_____ ,所含O原子的数目是______________ 个。
(2)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,也永远会激励着我们去奋发图强。黑火药在发生爆炸时,发生如下的反应:2KNO3+C+S=K2S+2NO2↑+CO2↑。其中被还原的元素是
(3)161g Na2SO4·10H2O中所含的Na+的物质的量是
您最近一年使用:0次
【推荐2】根据化学反应:①2Fe3++2I-=2Fe2++I2②Br2+2Fe2+=2Fe3++2Br-③Cl2+2Br-=2Cl-+Br2④KClO3+6HCl=KCl+3C12↑+3H2O,回答下列问题:
(1)判断下列离子的还原性由强到弱的顺序是( ) 。
A.Cl->Br->Fe2+>I- B.I->Fe2+>Br->Cl-
C.Br->I->Fe2+>Cl- D.Fe2+>Cl->I->Br-
(2)反应④中,标况下当生成67.2 L的C12时,反应过程中转移电子的物质的量为__ 。
(3)依据题中信息,判断下列化学物质难以稳定存在的是( ) 。
A.FeI2 B.FeI3 C.FeCl2 D.FeBr3
(4)新制氯水中所含的分子有_______ (用分子式表述),有同学认为久置的氯水里面所含的物质没有氧化性,对此你______ (填“是”或“否”)支持此观点,如果不支持,请用化学方程式予以解释_______ ;如果支持,此空不作答。
(1)判断下列离子的还原性由强到弱的顺序是
A.Cl->Br->Fe2+>I- B.I->Fe2+>Br->Cl-
C.Br->I->Fe2+>Cl- D.Fe2+>Cl->I->Br-
(2)反应④中,标况下当生成67.2 L的C12时,反应过程中转移电子的物质的量为
(3)依据题中信息,判断下列化学物质难以稳定存在的是
A.FeI2 B.FeI3 C.FeCl2 D.FeBr3
(4)新制氯水中所含的分子有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氧化还原是一类重要的反应。
(1)某同学写出以下三个化学方程式(未配平)
①N2O4+H2O→HNO3+HNO2 ②NO+HNO3→N2O3+H2O ③NH3+NO→HNO2+H2O
其中你认为一定不可能实现的是(填代号)____________ ;
(2)以下反应中H2O2仅体现还原性的是(填代号)____________ ,H2O2既体现氧化性又体现还原性的是(填代号)____________ ,从反应中判断H2O2、Ag2O、K2CrO4氧化性由强到弱的顺序是_______________ ;
A.H2O2+2Fe2++2H+=2Fe3++2H2O
B.2H2O2=2H2O+O2↑
C.Ag2O+H2O2=2Ag+O2↑+H2O
D.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
E.H2O2+MnSO4=MnO2+H2SO4
(3)用“双线桥法”标明以下反应中电子转移的方向和数目________ ,若反应中有3.01×1023个电子转移,则被氧化的还原剂的物质的量为___________ 。
2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
(1)某同学写出以下三个化学方程式(未配平)
①N2O4+H2O→HNO3+HNO2 ②NO+HNO3→N2O3+H2O ③NH3+NO→HNO2+H2O
其中你认为一定不可能实现的是(填代号)
(2)以下反应中H2O2仅体现还原性的是(填代号)
A.H2O2+2Fe2++2H+=2Fe3++2H2O
B.2H2O2=2H2O+O2↑
C.Ag2O+H2O2=2Ag+O2↑+H2O
D.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
E.H2O2+MnSO4=MnO2+H2SO4
(3)用“双线桥法”标明以下反应中电子转移的方向和数目
2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】硫酸或硝酸在下列用途或反应中各表现的性质是:
A.强酸性 B.易挥发性 C.吸水性 D.脱水性 E.强氧化性 F.不稳定性
(1)胆矾中加入浓硫酸,久置变为白色粉末__________ ;
(2)用铝槽车装运浓硫酸或浓硝酸__________ ;
(3)蔗糖中加入浓硫酸,形成“黑色发糕”__________ ;
(4)浓硝酸久置会变黄____________________ ;
(5)浓硝酸与不活泼金属铜单质反应_____ ;
(6)98%以上的浓硝酸俗称“发烟硝酸”________ 。
A.强酸性 B.易挥发性 C.吸水性 D.脱水性 E.强氧化性 F.不稳定性
(1)胆矾中加入浓硫酸,久置变为白色粉末
(2)用铝槽车装运浓硫酸或浓硝酸
(3)蔗糖中加入浓硫酸,形成“黑色发糕”
(4)浓硝酸久置会变黄
(5)浓硝酸与不活泼金属铜单质反应
(6)98%以上的浓硝酸俗称“发烟硝酸”
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】浓硫酸的特性
(1)吸水性
浓硫酸能吸收存在于周围环境中的水分(自由水和结晶水),常用作_______ 。
(2)脱水性
使有机物分子中的H和O以原子数2:1比例脱去,而使物质结构发生改变,生成新物质的性质
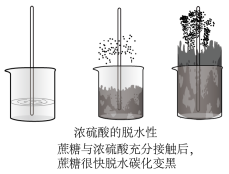
实验现象:向蔗糖中加入浓硫酸,搅拌,可观察到蔗糖_______ ,体积_______ ,变成疏松多孔的海绵状的炭,并放出有_______ 气味的气体。反应化学方程式_______ 。
(3)强氧化性
①浓硫酸与Cu反应
②浓硫酸与非金属反应
碳与浓硫酸反应_______ 。
③浓硫酸与金属反应
a.常温下,Fe、Al与浓H2SO4发生钝化,生成了致密的氧化膜。
b.氢前的活泼金属(如Zn):常温下与浓硫酸反应先产生_______ ,后产生_______ 。
c.氢后的活泼金属(如铜):加热下与浓硫酸反应先产生_______ ,后反应停止。
(1)吸水性
浓硫酸能吸收存在于周围环境中的水分(自由水和结晶水),常用作
(2)脱水性
使有机物分子中的H和O以原子数2:1比例脱去,而使物质结构发生改变,生成新物质的性质

实验现象:向蔗糖中加入浓硫酸,搅拌,可观察到蔗糖
(3)强氧化性
①浓硫酸与Cu反应
| 实验操作 | 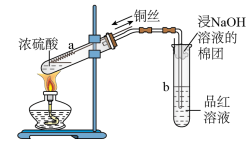 |
| 实验现象 | 铜丝表面 |
| 实验结论 | 在反应中,浓硫酸体现 |
| 化学方程式 |
碳与浓硫酸反应
③浓硫酸与金属反应
a.常温下,Fe、Al与浓H2SO4发生钝化,生成了致密的氧化膜。
b.氢前的活泼金属(如Zn):常温下与浓硫酸反应先产生
c.氢后的活泼金属(如铜):加热下与浓硫酸反应先产生
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】浓硫酸具有:①难挥发性(高沸点);②酸性;③强氧化性;④吸水性;⑤脱水性。下列各项分别表现浓硫酸的什么性质,请将序号填于空白处:
(1)浓硫酸与食盐共热,浓硫酸表现的性质为__ 。
(2)浓硫酸与铜共热,化学方程式为__ ,浓硫酸表现的性质是__ 。
(3)浓硫酸与红热木炭反应,化学方程式为__ ,浓硫酸表现的性质是__ 。
(4)可用浓硫酸干燥H2、CO2、HCl等气体,浓硫酸表现的性质为__ 。
(5)蔗糖中倒入浓硫酸,蔗糖变黑,体积膨胀,且有刺激性气味的气体产生,浓硫酸表现的性质是__ 。
(1)浓硫酸与食盐共热,浓硫酸表现的性质为
(2)浓硫酸与铜共热,化学方程式为
(3)浓硫酸与红热木炭反应,化学方程式为
(4)可用浓硫酸干燥H2、CO2、HCl等气体,浓硫酸表现的性质为
(5)蔗糖中倒入浓硫酸,蔗糖变黑,体积膨胀,且有刺激性气味的气体产生,浓硫酸表现的性质是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】A是由四种短周期常见元素组成的正盐,D是红棕色气体、G能使品红溶液褪色;A与其他物质在一定条件下存在如下转化关系(部分产物略去):
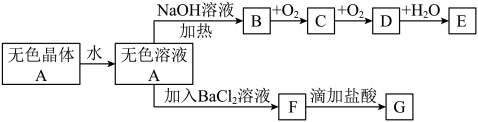
试回答下列问题:
(1) A、E的化学式依次为_______________ 、_______________ 。
(2)写出下列反应的化学方程式:
①C→D:_______________ 。
②F→G:_______________________________________ 。
(3)检验A溶液中阳离子的方法是____________________ ;若B→C的反应中转移2.5mol电子,则生成的C在标准状况下的体积为_______________ 。
(4)将D和G同时通入水中,生成C和一种强酸,则反应的离子方程式为_____________________ 。

试回答下列问题:
(1) A、E的化学式依次为
(2)写出下列反应的化学方程式:
①C→D:
②F→G:
(3)检验A溶液中阳离子的方法是
(4)将D和G同时通入水中,生成C和一种强酸,则反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】利用元素的化合价推测物质的性质是化学研究的重要手段。硫及其化合物的“价—类”二维图如下:___________ (填化学式)。
(2)将X与Y混合可生成淡黄色固体,该反应中还原剂与氧化剂的物质的量之比为___________ ;实验室常用热的氢氧化钠溶液洗去试管内壁附着的该淡黄色固体,其原理为___________ (用化学方程式表示)。
(3)检验N盐溶液是否变质的方法是___________ 。
(4)Z的浓溶液与碳单质在一定条件下可以发生化学反应,该反应的化学方程式为___________ 。
(5)已知 能被
能被 氧化为Na2SO4,则240mL0.05mol/L的Na2SO3溶液与200mL0.02mol/L的
氧化为Na2SO4,则240mL0.05mol/L的Na2SO3溶液与200mL0.02mol/L的 溶液恰好完全反应时,Cr元素在还原产物中的化合价为
溶液恰好完全反应时,Cr元素在还原产物中的化合价为___________ 。
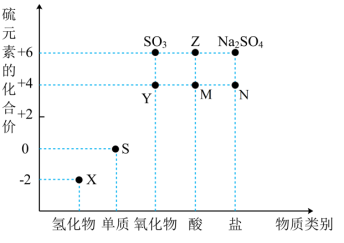
(2)将X与Y混合可生成淡黄色固体,该反应中还原剂与氧化剂的物质的量之比为
(3)检验N盐溶液是否变质的方法是
(4)Z的浓溶液与碳单质在一定条件下可以发生化学反应,该反应的化学方程式为
(5)已知
 能被
能被 氧化为Na2SO4,则240mL0.05mol/L的Na2SO3溶液与200mL0.02mol/L的
氧化为Na2SO4,则240mL0.05mol/L的Na2SO3溶液与200mL0.02mol/L的 溶液恰好完全反应时,Cr元素在还原产物中的化合价为
溶液恰好完全反应时,Cr元素在还原产物中的化合价为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】物质的类别和核心元素的化合价是研究物质性质的两个重要角度。下图所示是硫及其部分化合物的“价类二维图”。
1.X的化学式为___________ ,将X与 混合,可生成淡黄色固体,该反应的氧化产物与还原产物的质量之比为
混合,可生成淡黄色固体,该反应的氧化产物与还原产物的质量之比为___________ 。
2.过量的Zn粉与一定量W浓溶液混合加热反应,生成___________ (填化学式)气体。转化①可由S粉与热的W浓溶液反应实现,反应的化学方程式为___________ 。
3.欲制备 ,从氧化还原角度分析,下列合理的是___________(选填字母)
,从氧化还原角度分析,下列合理的是___________(选填字母)
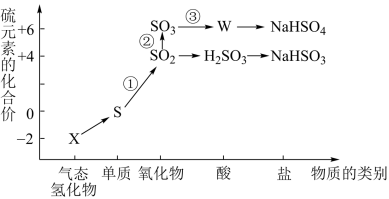
1.X的化学式为
 混合,可生成淡黄色固体,该反应的氧化产物与还原产物的质量之比为
混合,可生成淡黄色固体,该反应的氧化产物与还原产物的质量之比为2.过量的Zn粉与一定量W浓溶液混合加热反应,生成
3.欲制备
 ,从氧化还原角度分析,下列合理的是___________(选填字母)
,从氧化还原角度分析,下列合理的是___________(选填字母)A. | B. | C. | D.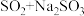 |
您最近一年使用:0次



