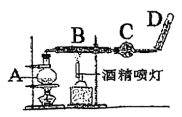
铁是生活中常见的金属,完成"Fe与水蒸气的高温反应实验”。_____ 。
(2)反应的方程式为_____ 。
(3)分析得出B中是铁的氧化物与铁单质,为探究B中反应产物的氧含量,选取5g固体放入硬质试管中,通入足量CO,高温下充分反应,将生成的气体全部通入足量的澄清石灰水中,生成白色沉淀6g。则产物中氧的质量分数为_____ 。
(2)反应的方程式为
(3)分析得出B中是铁的氧化物与铁单质,为探究B中反应产物的氧含量,选取5g固体放入硬质试管中,通入足量CO,高温下充分反应,将生成的气体全部通入足量的澄清石灰水中,生成白色沉淀6g。则产物中氧的质量分数为
更新时间:2024-04-10 11:28:13
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】选考(15)化学与技术
侯氏制碱法的生产流程可表示如下,请回答下列问题:
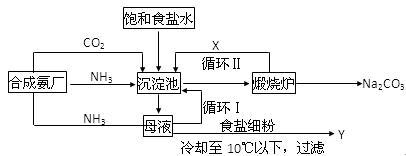
(1)沉淀池中加入(或通入)有关物质的顺序为_____________ →___________ →___________
(2)写出上述流程中X、Y的化学式:X____________ Y___________
(3)写出沉淀池中发生的化学反应方程式__________________________________________
(4)侯氏制碱法的生产流程中可以循环使用的物质主要为____________ 、______________
(5)从沉淀池中取出沉淀的操作是___________ ,为了进一步提纯NaHCO3晶体,可采用_______ 法
(6)若在煅烧炉中燃烧的时间较短,NaHCO3将分解不完全。现若取10.5g NaHCO3固体,加热一定时间后,剩余固体的质量为7.1g,如果把此剩余固体全部加入到200mL 1mol/L的盐酸中,充分反应后溶液中H+的物质的量浓度为___________ mol/L(溶液体积变化忽略不计)
侯氏制碱法的生产流程可表示如下,请回答下列问题:

(1)沉淀池中加入(或通入)有关物质的顺序为
(2)写出上述流程中X、Y的化学式:X
(3)写出沉淀池中发生的化学反应方程式
(4)侯氏制碱法的生产流程中可以循环使用的物质主要为
(5)从沉淀池中取出沉淀的操作是
(6)若在煅烧炉中燃烧的时间较短,NaHCO3将分解不完全。现若取10.5g NaHCO3固体,加热一定时间后,剩余固体的质量为7.1g,如果把此剩余固体全部加入到200mL 1mol/L的盐酸中,充分反应后溶液中H+的物质的量浓度为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】新冠肺炎期间,化学消毒剂大显身手.高铁酸钾 是一种高效多功能的绿色消毒剂,广泛应用于生活用水和废水的杀菌、消毒.实验室模拟湿法制备高铁酸钾的流程如下:
是一种高效多功能的绿色消毒剂,广泛应用于生活用水和废水的杀菌、消毒.实验室模拟湿法制备高铁酸钾的流程如下:
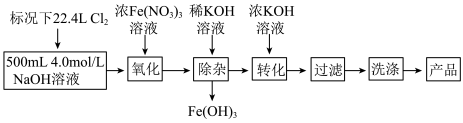
已知:转化过程发生复分解反应.
回答下列问题:
(1)配制上述 溶液,需要
溶液,需要 的质量为
的质量为_______________ 。
(2)下列操作可能导致溶液浓度偏大的有_______________ (填序号)。
A.将 放在滤纸上称量
放在滤纸上称量
B. 溶液转移到容量瓶后,未洗涤玻璃棒就定容
溶液转移到容量瓶后,未洗涤玻璃棒就定容
C.容量瓶洗净之后未干燥
D.定容时俯视刻度线
E.摇匀后发现液面低于刻度线,再加水至刻度线
(3) 溶液应置于冰水浴中,否则温度升高将发生如下副反应:
溶液应置于冰水浴中,否则温度升高将发生如下副反应:
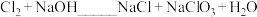 (未配平)
(未配平)
①若有 发生该副反应,该过程中转移电子数目为
发生该副反应,该过程中转移电子数目为_______________ ;
②若反应后溶液中 和
和 的物质的量之比为
的物质的量之比为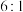 ,则生成
,则生成 和
和 的物质的量之比为
的物质的量之比为__________ 。
(4)氧化过程中溶液保持碱性.写出反应的离子方程式:______________ 。
(5) ,试解释该反应能发生的原因
,试解释该反应能发生的原因__________ 。
(6)产品经干燥后得到纯品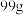 ,则
,则 的产率为
的产率为____________ (用百分数表示)。
 是一种高效多功能的绿色消毒剂,广泛应用于生活用水和废水的杀菌、消毒.实验室模拟湿法制备高铁酸钾的流程如下:
是一种高效多功能的绿色消毒剂,广泛应用于生活用水和废水的杀菌、消毒.实验室模拟湿法制备高铁酸钾的流程如下:
已知:转化过程发生复分解反应.
回答下列问题:
(1)配制上述
 溶液,需要
溶液,需要 的质量为
的质量为(2)下列操作可能导致溶液浓度偏大的有
A.将
 放在滤纸上称量
放在滤纸上称量B.
 溶液转移到容量瓶后,未洗涤玻璃棒就定容
溶液转移到容量瓶后,未洗涤玻璃棒就定容C.容量瓶洗净之后未干燥
D.定容时俯视刻度线
E.摇匀后发现液面低于刻度线,再加水至刻度线
(3)
 溶液应置于冰水浴中,否则温度升高将发生如下副反应:
溶液应置于冰水浴中,否则温度升高将发生如下副反应: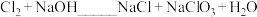 (未配平)
(未配平)①若有
 发生该副反应,该过程中转移电子数目为
发生该副反应,该过程中转移电子数目为②若反应后溶液中
 和
和 的物质的量之比为
的物质的量之比为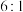 ,则生成
,则生成 和
和 的物质的量之比为
的物质的量之比为(4)氧化过程中溶液保持碱性.写出反应的离子方程式:
(5)
 ,试解释该反应能发生的原因
,试解释该反应能发生的原因(6)产品经干燥后得到纯品
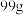 ,则
,则 的产率为
的产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】亚硝酰氯( ,沸点:
,沸点: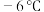 ;易水解,能与
;易水解,能与 反应)可作为有机合成试剂。在实验室可用
反应)可作为有机合成试剂。在实验室可用 (沸点:
(沸点: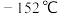 )和
)和 (沸点:
(沸点: )在一定条件下反应制备,其反应原理为
)在一定条件下反应制备,其反应原理为 。回答下列问题:
。回答下列问题:
(1)实验室常用铜与稀硝酸反应制备 ,若将
,若将 加入100mL稀硫酸(足量)和稀硝酸的混合溶液中制备NO,最多溶解19.2g铜,则
加入100mL稀硫酸(足量)和稀硝酸的混合溶液中制备NO,最多溶解19.2g铜,则 物质的量浓度为
物质的量浓度为_______ 。
(2)实验室若以 和浓盐酸为原料,利用以下装置(部分夹持仪器已省略)制备一瓶干燥纯净的
和浓盐酸为原料,利用以下装置(部分夹持仪器已省略)制备一瓶干燥纯净的 ,则其连接顺序为
,则其连接顺序为_______ →jh(按气流方向,用小写字母表示)。

(3) 的制备,装置(夹持仪器已省略)如下图所示。
的制备,装置(夹持仪器已省略)如下图所示。
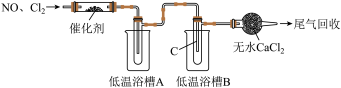
①将催化剂负载在玻璃棉上的目的是_______ 。
②为分离产物和未反应的原料,低温浴槽A的温度区间应控制在_______ (填字母)。
A.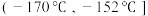 B.
B.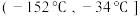 C.
C.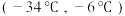
③仪器C中收集的物质是_______ (填化学式)。
(4) 样品中
样品中 的质量分数测定。取
的质量分数测定。取
 样品(杂质中不含有氯元素)溶于水,配制成250mL溶液;取出25.00mL样品溶于锥形瓶中,用
样品(杂质中不含有氯元素)溶于水,配制成250mL溶液;取出25.00mL样品溶于锥形瓶中,用 的
的 标准溶液滴定至终点,消耗标准溶液的体积为20.00mL。
标准溶液滴定至终点,消耗标准溶液的体积为20.00mL。 的质量分数为
的质量分数为_______ 。
 ,沸点:
,沸点: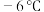 ;易水解,能与
;易水解,能与 反应)可作为有机合成试剂。在实验室可用
反应)可作为有机合成试剂。在实验室可用 (沸点:
(沸点: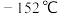 )和
)和 (沸点:
(沸点: )在一定条件下反应制备,其反应原理为
)在一定条件下反应制备,其反应原理为 。回答下列问题:
。回答下列问题:(1)实验室常用铜与稀硝酸反应制备
 ,若将
,若将 加入100mL稀硫酸(足量)和稀硝酸的混合溶液中制备NO,最多溶解19.2g铜,则
加入100mL稀硫酸(足量)和稀硝酸的混合溶液中制备NO,最多溶解19.2g铜,则 物质的量浓度为
物质的量浓度为(2)实验室若以
 和浓盐酸为原料,利用以下装置(部分夹持仪器已省略)制备一瓶干燥纯净的
和浓盐酸为原料,利用以下装置(部分夹持仪器已省略)制备一瓶干燥纯净的 ,则其连接顺序为
,则其连接顺序为
(3)
 的制备,装置(夹持仪器已省略)如下图所示。
的制备,装置(夹持仪器已省略)如下图所示。
①将催化剂负载在玻璃棉上的目的是
②为分离产物和未反应的原料,低温浴槽A的温度区间应控制在
A.
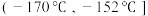 B.
B.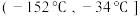 C.
C.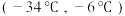
③仪器C中收集的物质是
(4)
 样品中
样品中 的质量分数测定。取
的质量分数测定。取
 样品(杂质中不含有氯元素)溶于水,配制成250mL溶液;取出25.00mL样品溶于锥形瓶中,用
样品(杂质中不含有氯元素)溶于水,配制成250mL溶液;取出25.00mL样品溶于锥形瓶中,用 的
的 标准溶液滴定至终点,消耗标准溶液的体积为20.00mL。
标准溶液滴定至终点,消耗标准溶液的体积为20.00mL。 的质量分数为
的质量分数为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】两种常见的非金属元素A与B,与常见的三种金属元素C、D、E,A的一种单质是自然界硬度最大的物质,B与C的单质在加热条件下反应生成淡黄色化合物X,D的单质既能与盐酸、也能与NaOH溶液反应生成H2。E的单质在B的单质中燃烧火星四溅,生成一种黑色固体Y。请回答下列问题:
(1)物质X的名称__________________ 。


(2)将D的单质用砂纸打磨,然后灼烧,液态的D并不滴落的原因_____________________
(3)写出E的单质与H2O加热时反应的化学方程式,并用单线桥分析电子转移的方向和数目:________________________________________________________ 。
(4)ag C的单质投入足量CuSO4溶液中,下列实验现象正确的有__________________ 。
A.钠沉在溶液底部 B.熔化成银色光亮的小球
C.小球四处游动发出”嘶嘶”的声音 D.生成红色固体物质
可能的离子方程式为___________________________________________________ 。将所得沉淀过滤、洗涤、灼烧,可得到___________ g固体。
(1)物质X的名称



(2)将D的单质用砂纸打磨,然后灼烧,液态的D并不滴落的原因
(3)写出E的单质与H2O加热时反应的化学方程式,并用单线桥分析电子转移的方向和数目:
(4)ag C的单质投入足量CuSO4溶液中,下列实验现象正确的有
A.钠沉在溶液底部 B.熔化成银色光亮的小球
C.小球四处游动发出”嘶嘶”的声音 D.生成红色固体物质
可能的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下"Fe与水蒸气反应的实验"。

请回答该实验中的问题。
(1)实验前必须对整套装置进行气密性的检查,操作方法是_____________ 。
(2)圆底烧瓶中盛装的是水,该装置受热后的主要作用是_______________ ;烧瓶底部放置了几片碎瓷片,碎瓷片的作用是_______________ 。
(3)酒精灯和酒精喷灯点燃的顺序是__________ 。
(4)干燥管中盛装的物质可以是_____________ ,作用是__________ 。
(5)如果要在A处玻璃管口处点燃该气体,则必须对该气体进行_________ ,这一操作的目的_____ 。

请回答该实验中的问题。
(1)实验前必须对整套装置进行气密性的检查,操作方法是
(2)圆底烧瓶中盛装的是水,该装置受热后的主要作用是
(3)酒精灯和酒精喷灯点燃的顺序是
(4)干燥管中盛装的物质可以是
(5)如果要在A处玻璃管口处点燃该气体,则必须对该气体进行
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】在常温下,Fe 与水并不起反应,但在高温下,Fe与水蒸气可发生反应。应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,完成高温下“Fe与水蒸气的反应实验”然后对产物进行检验。请回答该实验中的问题。
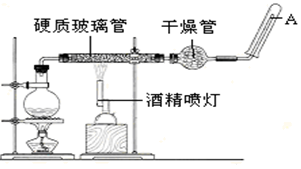
(1)写出该反应的化学方程式______
(2)实验开始时应先点燃_______ ,实验结束时应先熄灭_______ 。
(3)该同学探究反应后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②该同学马上另取少量溶液B,使其跟NaOH溶液反应。若按如图所示的操作,可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出有关变色反应的化学方程式_______ 。
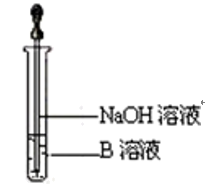
氢氧化亚铁具有强还原性极容易被氧化变色:写出一种实验制备氢氧化亚铁防止氧化的措施:______ 。
(4)一段时间后,该同学发现(3)中未变红的溶液变成红色,说明Fe2+ 具有还原性。由此可知,实验室中含Fe2+盐溶液现用现配制的原因_______ ,并且配制含Fe2+的盐溶液时应加入少量 _______ ,检验硫酸铁盐溶液中是否含有硫酸亚铁盐的方法是 _______ 。

(1)写出该反应的化学方程式
(2)实验开始时应先点燃
(3)该同学探究反应后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②该同学马上另取少量溶液B,使其跟NaOH溶液反应。若按如图所示的操作,可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出有关变色反应的化学方程式

氢氧化亚铁具有强还原性极容易被氧化变色:写出一种实验制备氢氧化亚铁防止氧化的措施:
(4)一段时间后,该同学发现(3)中未变红的溶液变成红色,说明Fe2+ 具有还原性。由此可知,实验室中含Fe2+盐溶液现用现配制的原因
您最近一年使用:0次



