下列方案设计、现象和结论都正确的是
| 实验方案 | 现象 | 结论 | |
| A | 取某固体试样加入适量水,取少许于试管中,滴加NaOH溶液,并将湿润的红色石蕊试纸接近管口 | 湿润红色石蕊试纸无明显现象 | 该固体试样中一定不存在NH |
| B | 在橡胶塞侧面挖一个凹槽,嵌入下端卷成螺旋状的铜丝,向具支试管中加入2mL浓硝酸,用橡胶塞塞住试管口,使铜丝与硝酸接触,一段时间后,向上拉铜丝,终止反应 | 剧烈反应,铜丝表面放出红棕色的气泡,铜不断溶解,溶液变成绿色 | 浓硝酸具有强氧化性 |
| C | 取未知溶液于试管中,加入BaCl2溶液,有白色沉淀生成,再加足量稀盐酸 | 沉淀不溶解 | 溶液中一定含有SO |
| D | 向Fe(NO3)2溶液中滴加稀盐酸,再加入几滴KSCN溶液 | 溶液变为红色 | 稀盐酸可以将Fe2+氧化为Fe3+ |
| A.A | B.B | C.C | D.D |
更新时间:2024-04-10 12:41:53
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列关于实验操作、现象、得出的结论正确的是
| 选项 | 实验操作及现象 | 结论 |
| A | 向某溶液中先滴加硝酸酸化,再滴加BaCl2溶液,出现白色沉淀 | 原溶液中一定含有SO |
| B | 向某盐溶液中滴加NaOH溶液,没有检测到使湿润红色石蕊试纸变蓝的气体 | 该溶液中一定没有NH |
| C | 将蔗糖和稀硫酸混合加热,冷却后加入NaOH溶液至碱性,再加入少量新制Cu(OH)2加热,有砖红色沉淀产生 | 蔗糖已经水解 |
| D | 用大理石和盐酸反应制取CO2气体,立即通入定浓度的Na2SiO3溶液中,出现白色沉淀 | H2CO3的酸性比H2SiO3的酸性强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】根据下列实验操作及现象得到的结论正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向某溶液中滴加 溶液 溶液 | 有白色沉淀生成 | 溶液中含有 |
| B | 向放有铁片的试管中加入浓 | 无明显现象 | 铁片与浓 不反应 不反应 |
| C | 向某溶液中滴加NaOH溶液,在试管口放置一片湿润的蓝色石蕊试纸 | 试纸不变色 | 溶液中不存在 |
| D | 将浓 加入到蔗糖中,并不断搅拌 加入到蔗糖中,并不断搅拌 | 蔗糖变黑,体积膨胀,有刺激性气味 | 浓 具有脱水性、强氧化性 具有脱水性、强氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列根据实验现象得到的实验结论正确的是
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 将Fe(N03)2样品溶于稀硫酸后,滴加KSCN溶液 | 溶液变成红色 | Fe(NO3)2样品中一定含有Fe3+ |
| B | 向KI溶液中加入少量苯,然后加入FcCl3溶液 | 有机层呈橙红色 | 还原性 Fe3+>I- |
| C | 向浓度均为0.1mol/L的Na2CO3和Na2S混合溶液滴入少量AgNO3溶液 | 产生黑色沉淀(Ag2S) | Ksp(Ag2S)>Ksp(Ag2CO3) |
| D | 向某溶液中加入KOH溶液并加热,管口放湿润的红色石蕊试纸 | 试纸变为蓝色 | 原溶液片含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是 ( )
| A.向某溶液中加入BaCl2溶液,有白色沉淀生成,则溶液中一定存在SO42— |
| B.向某溶液中加入盐酸,产生能使澄清石灰水变浑浊的气体,溶液中一定存在CO32— |
| C.向某溶液中加入Ca(OH)2溶液,有白色沉淀生成,则溶液中一定存在CO32— |
| D.加入硝酸酸化的AgNO3溶液有白色沉淀生成,则溶液中有Cl- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列关于某些物质(离子)检验方法或结论正确的是
A.向溶液X中先滴加稀硝酸,再滴加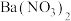 溶液,出现白色沉淀,则溶液X中一定含有 溶液,出现白色沉淀,则溶液X中一定含有 |
B.加入 溶液有白色沉淀产生,再加盐酸,白色沉淀消失,原溶液一定含有 溶液有白色沉淀产生,再加盐酸,白色沉淀消失,原溶液一定含有 |
C.加入 溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝,原溶液一定有 溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝,原溶液一定有 ` ` |
D.加入 溶液有白色沉淀产生,则原溶液中一定含有 溶液有白色沉淀产生,则原溶液中一定含有 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列实验操作、实验现象、解释或结论都正确且有因果关系的是
| 选项 | 实验操作 | 实验现象 | 解释或结论 |
| A | 向盛有2mL0.1mol∙L-1AgNO3溶液的试管中滴加5mL0.1mol∙L-1NaCl溶液,再向其中滴加一定0.1mol∙L-1KI溶液 | 先有白色沉淀后黄色沉淀 | 常温下,溶度积:Ksp(AgCl)>Ksp(AgI) |
| B | 常温下,用pH计分别测定1mol∙L-1CH3COONH4溶液和0.1mol∙L-1CH3COONH4溶液的pH | 测得pH都等于7 | 同温下,不同浓度的CH3COONH4溶液中水的电离程度相同 |
| C | 用铂电极电解等浓度的足量Fe2(SO4)3、Cu(NO3)2混合溶液 | 阴极有红色固体物质析出 | 金属活动性:Cu>Fe |
| D | 向5mL0.1mol∙L-1FeCl3溶液中滴加2mL0.1mol∙L-1KI溶液,充分反应后,取少量反应后溶液于试管中,再滴入几滴KSCN溶液 | 溶液变红 | KI与FeCl3的反应为可逆反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
【推荐2】依据下列实验中的操作和现象,对应的结论正确的是
选项 | 实验操作 | 现象 | 解释或结论 |
A | 某溶液中加入少量氯水振荡后,再滴加1-2滴 | 溶液呈红色 | 原溶液中一定含有 |
B | 某溶液中滴加用足量盐酸酸化的 | 有白色沉淀出现 | 原溶液中一定含有 |
C | 用铂丝蘸取某纯净物固体粉末做焰色试验 | 透过蓝色钴玻璃观察焰色呈紫色 | 此固体物质一定是钾盐 |
D | 将某种铁的氧化物溶于足量的稀硫酸中,取其溶液滴加少量 | 溶液紫红色褪去 | 原氧化物中一定含有+2价铁元素 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某小组在实验室中用下图所示装置(夹持装置已略去)制取碳酸镧[La2(CO3)3],制备原理为2LaCl3+6NH3+3CO2+3H2O=La2(CO3)3↓+6NH4Cl。下列说法正确的是
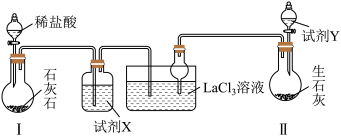

| A.分液漏斗使用前需检查是否漏水,干燥管的作用是增大与反应物间的接触面积 |
| B.试剂X为饱和Na2CO3溶液,试剂Y为饱和NH4Cl溶液 |
| C.若用稀硫酸代替装置I中的稀盐酸,则实验时可以不用盛试剂X的装置 |
| D.实验时一般先通入装置II所产生的气体,再通入装置I产生的气体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】某同学进行如下实验:
已知: i.H2O2 H+ + HO
H+ + HO HO
HO
 H++O
H++O
ii.BaO2是一种白色难溶于水的固体
下列说法不合理的是
| 序号 | 实验① | 实验② | 实验③ | 实验④ | 实验⑤ |
| 方案 | BaCl2溶液
| BaCl2溶液
| BaCl2溶液
| 先加MnO2粉末,后加酸性 KMnO4溶液 | 稀H2SO4
|
| 现象 | 出现白色沉淀 | 无明显现象 | 出现白色沉淀 | 产生大量气泡,高锰酸钾溶液不褪色 | 出现白色沉淀 |
 H+ + HO
H+ + HO HO
HO
 H++O
H++O
ii.BaO2是一种白色难溶于水的固体
下列说法不合理的是
| A.实验①和②说明BaO2可溶于酸 |
| B.实验①和③得到的沉淀组成一样 |
| C.实验⑤的白色沉淀经检验为BaSO4,说明溶解度BaO2> BaSO4 |
| D.可用BaCl2、MnO2、H2O检验长期放置的Na2O2中是否含有Na2CO3 |
您最近一年使用:0次

 溶液
溶液
 溶液
溶液
 溶液,振荡。
溶液,振荡。 、
、 、
、 、
、 溶液中:
溶液中: 、
、 的溶液中:
的溶液中: 、
、 、
、 、
、






