NaOH溶液可用于中和反应反应热测定和酸碱中和滴定实验中。回答下列问题:
(1)在实验室中进行中和反应反应热测定和中和滴定实验时,一定没有用到的仪器是_____ (填字母,下同)。_____ 。
(3)用标准NaOH溶液滴定未知浓度的盐酸时,下列操作可能会导致所测盐酸的物质的量浓度偏低的是_____。
(4)某实验小组用0.55mol·L-1的NaOH溶液和0.25mol·L-1的H2SO4溶液进行中和反应反应热的测定。取50mLNaOH溶液和50mLH2SO4溶液在_____ (填仪器名称)中进行实验。数据如下:
近似认为50mL0.55mol·L-1NaOH溶液和50mL0.25mol·L-1H2SO4溶液的密度都是1g·mL-1,中和后生成溶液的比热容c=4.18J·g-1·℃-1,则测得中和反应反应热(生成1molH2O) ΔH=_____ kJ・mol-1(精确到小数点后一位)。
(5)常温下,在25.00mL氢氧化钠溶液中逐滴加入0.2000mol·L-1的醋酸溶液,滴定曲线如图所示。_____ mol·L-1。
②若所加入的酸为0.2000mol·L-1的盐酸,则D点时溶液的c(H+)=_____ mol·L-1。
(1)在实验室中进行中和反应反应热测定和中和滴定实验时,一定没有用到的仪器是
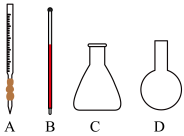
(3)用标准NaOH溶液滴定未知浓度的盐酸时,下列操作可能会导致所测盐酸的物质的量浓度偏低的是_____。
| A.碱式滴定管用蒸馏水洗净后,直接注入标准浓度的NaOH溶液 |
| B.碱式滴定管尖端滴定前无气泡,滴定后有气泡 |
| C.记录消耗的碱液,滴定前平视读数,滴定后仰视读数 |
| D.锥形瓶未用待测盐酸润洗 |
(4)某实验小组用0.55mol·L-1的NaOH溶液和0.25mol·L-1的H2SO4溶液进行中和反应反应热的测定。取50mLNaOH溶液和50mLH2SO4溶液在
| 实验次数 | 起始温度T1/C | 终止温度T2/°C | ||
| H2SO4 | NaOH | 平均值 25.1 26.3 25.3 26.3 | ||
| 1 | 25.2 | 25.0 | 28.5 | |
| 2 | 26.2 | 26.4 | 32.5 | |
| 3 | 25.3 | 25.3 | 28.8 | |
| 4 | 26.1 | 26.5 | 29.6 | |
(5)常温下,在25.00mL氢氧化钠溶液中逐滴加入0.2000mol·L-1的醋酸溶液,滴定曲线如图所示。

②若所加入的酸为0.2000mol·L-1的盐酸,则D点时溶液的c(H+)=
更新时间:2024-04-10 21:08:33
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】如图是某实验小组改进的中和反应反应热测定实验装置。组装仪器后,先在塑料瓶中加入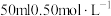 盐酸,然后通过注射器注入
盐酸,然后通过注射器注入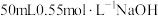 溶液,通过测定反应过程中所放出的热量可计算反应热。回答下列问题:
溶液,通过测定反应过程中所放出的热量可计算反应热。回答下列问题:
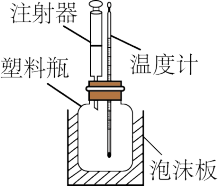
(1)塑料瓶外泡沫板的作用是_______ ,缺少的仪器是_______ 。
(2)假设盐酸和氢氧化钠溶液的密度都是 ,又知中和反应后生成溶液的比热容
,又知中和反应后生成溶液的比热容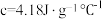 ,为了计算中和热,某学生实验记录数据如下:
,为了计算中和热,某学生实验记录数据如下:
依据该学生的实验数据计算,该实验测得的中和热
_______ (结果保留一位小数)。
(3)有同学考虑注射器针筒中会有NaOH溶液残留(不超过0.5mL),认为上述实验会导致所测得反应热偏小,请判断该观点是否正确并说明理由:_______ 。
(4)如果用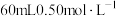 盐酸与
盐酸与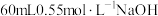 溶液进行反应,与上述实验相比,所放出的热量
溶液进行反应,与上述实验相比,所放出的热量_______ (填“相等”或“不相等”,下同)、所求中和热_______ 。
(5)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和 的稀盐酸恰好完全反应,其反应热分别为
的稀盐酸恰好完全反应,其反应热分别为 、
、 、
、 ,则
,则 、
、 、
、 的大小关系为
的大小关系为_______ 。
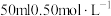 盐酸,然后通过注射器注入
盐酸,然后通过注射器注入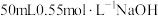 溶液,通过测定反应过程中所放出的热量可计算反应热。回答下列问题:
溶液,通过测定反应过程中所放出的热量可计算反应热。回答下列问题:
(1)塑料瓶外泡沫板的作用是
(2)假设盐酸和氢氧化钠溶液的密度都是
 ,又知中和反应后生成溶液的比热容
,又知中和反应后生成溶液的比热容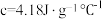 ,为了计算中和热,某学生实验记录数据如下:
,为了计算中和热,某学生实验记录数据如下:| 实验序号 | 起始温度 /℃ /℃ | 终止温度 /℃ /℃ | |
| 盐酸 | 氢氧化钠溶液 | 混合溶液 | |
| 1 | 20.0 | 20.2 | 23.2 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3 | 20.3 | 20.5 | 25.6 |

(3)有同学考虑注射器针筒中会有NaOH溶液残留(不超过0.5mL),认为上述实验会导致所测得反应热偏小,请判断该观点是否正确并说明理由:
(4)如果用
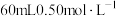 盐酸与
盐酸与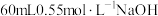 溶液进行反应,与上述实验相比,所放出的热量
溶液进行反应,与上述实验相比,所放出的热量(5)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和
 的稀盐酸恰好完全反应,其反应热分别为
的稀盐酸恰好完全反应,其反应热分别为 、
、 、
、 ,则
,则 、
、 、
、 的大小关系为
的大小关系为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】50 mL 0.50 mol/L盐酸与50 mL 0.55 mol/L NaOH溶液在如图所示的装置中进行
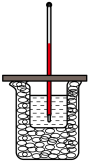
中和反应。通过测定反应过程中所放出的热量可计算中和热,回答下列问题:
(1)从实验装置上看,图中缺少的一种玻璃用品是_____________ 。
(2)实验中改用60 mL 0.50 mol/L盐酸与60 mL 0.55 mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量____ (填“相等”或“不相等”),所求得的中和热____ (填“相等”或“不相等”),简述理由:___________________________________________ 。
(3)实验中改用6.94 mL 15 mol/L硫酸溶液跟60 mL 0.55 mol/L NaOH溶液进行反应,与上述实验相比,所求中和热________ (填“相等”或“不相等”),简述理由:_____________________________________________________________________
(4)若三次平行操作测得数据中起始时盐酸与烧碱溶液平均温度相同,而终止温度与起始温度差(t2-t1)分别为①3.3 ℃、②3.5 ℃、③4.5 ℃,则最终代入计算式的温差平均值为____ ℃。
(5)请利用上(4)小题的结论,计算该实验测得的中和反应反应热ΔH=____ [设盐酸和NaOH溶液的密度为1 g/cm3,反应后混合溶液的比热容(c)为4.18 J/(g·℃)]。
(6)若将NaOH溶液改为相同体积、相同浓度的氨水,测得中和反应反应热为ΔH1,则ΔH1与原题中ΔH的关系为ΔH1____ (填“<”“>”或“=”)ΔH,理由是________ 。

中和反应。通过测定反应过程中所放出的热量可计算中和热,回答下列问题:
(1)从实验装置上看,图中缺少的一种玻璃用品是
(2)实验中改用60 mL 0.50 mol/L盐酸与60 mL 0.55 mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量
(3)实验中改用6.94 mL 15 mol/L硫酸溶液跟60 mL 0.55 mol/L NaOH溶液进行反应,与上述实验相比,所求中和热
(4)若三次平行操作测得数据中起始时盐酸与烧碱溶液平均温度相同,而终止温度与起始温度差(t2-t1)分别为①3.3 ℃、②3.5 ℃、③4.5 ℃,则最终代入计算式的温差平均值为
(5)请利用上(4)小题的结论,计算该实验测得的中和反应反应热ΔH=
(6)若将NaOH溶液改为相同体积、相同浓度的氨水,测得中和反应反应热为ΔH1,则ΔH1与原题中ΔH的关系为ΔH1
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】利用下图所示装置测定中和热的实验步骤如下:
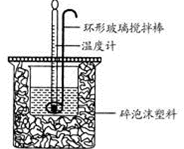
①用量筒量取50mL0.50mol·L-1盐酸倒入小烧杯中,测出盐酸温度;②用另一量筒量取50mL0.55mol·L-1NaOH溶液,并用另一温度计测出其温度;③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测得混合液最高温度,回答下列问题:
(1)为什么所用NaOH溶液要稍过量?_________
(2)倒入NaOH溶液的正确操作是________ (填序号)。
A.沿玻璃棒缓慢倒入
B.分三次少量倒入
C.一次迅速倒入
(3)使盐酸与NaOH溶液混合均匀的正确操作是________ (填序号)。
A.用温度计小心搅拌
B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯
D.用套在温度计上的环形玻璃搅拌棒轻轻地搅动
(4)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和1L 1mol·L-1的稀盐酸恰好完全反应,其反应热分别为△H1、△H2、△H3,则△H1、△H2、△H3的大小关系为________ 。
(5)________ (填“能”或“不能”)用Ba(OH)2溶液和硫酸代替氢氧化钠溶液和盐酸,理由是__________________

①用量筒量取50mL0.50mol·L-1盐酸倒入小烧杯中,测出盐酸温度;②用另一量筒量取50mL0.55mol·L-1NaOH溶液,并用另一温度计测出其温度;③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测得混合液最高温度,回答下列问题:
(1)为什么所用NaOH溶液要稍过量?
(2)倒入NaOH溶液的正确操作是
A.沿玻璃棒缓慢倒入
B.分三次少量倒入
C.一次迅速倒入
(3)使盐酸与NaOH溶液混合均匀的正确操作是
A.用温度计小心搅拌
B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯
D.用套在温度计上的环形玻璃搅拌棒轻轻地搅动
(4)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和1L 1mol·L-1的稀盐酸恰好完全反应,其反应热分别为△H1、△H2、△H3,则△H1、△H2、△H3的大小关系为
(5)
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某校化学兴趣小组的同学运用滴定法对一含有少量Na2SO4的NaOH样品中NaOH的含量进行测定,请回答下列问题:
(1)用分析天平准确称取该样品5.360g,全部溶于水配制成1000.0mL的溶液。用碱式滴定管取其中20.00mL放在锥形瓶中,滴加几滴甲基橙做指示剂。用标准的盐酸溶液滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视着____ 。滴定终点的现象是____________ 。
(2)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是_____ (填写序号)
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,滴定结束时俯视读数
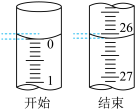
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示:则滴定终点的读数为____ mL。
(4)某学生根据三次实验分别记录有关数据如下:
请选用其中合理的数据列式计算出该样品中NaOH的质量百分含量。(写出计算过程)__
(1)用分析天平准确称取该样品5.360g,全部溶于水配制成1000.0mL的溶液。用碱式滴定管取其中20.00mL放在锥形瓶中,滴加几滴甲基橙做指示剂。用标准的盐酸溶液滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视着
(2)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,滴定结束时俯视读数
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示:则滴定终点的读数为

(4)某学生根据三次实验分别记录有关数据如下:
| 滴定次数 | 待测氢氧化钠溶液的体积/mL | 0.1000mol/L盐酸的体积(mL) | ||
| 滴定前刻度 | 滴定后刻度 | |||
| 第1次 | 20.00 | 0.00 | 26.01 | |
| 第2次 | 20.00 | 1.56 | 30.30 | |
| 第3次 | 20.00 | 0.22 | 26.21 | |
请选用其中合理的数据列式计算出该样品中NaOH的质量百分含量。(写出计算过程)
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】Ⅰ.现用中和滴定法测定某烧碱溶液的浓度,有关数据记录如下:
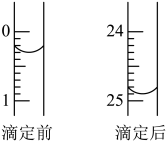
(1)如图表示 盐酸标准液第二次滴定前后
盐酸标准液第二次滴定前后 滴定管中液面的位置,该次滴定所用标准盐酸体积为
滴定管中液面的位置,该次滴定所用标准盐酸体积为_______  。
。
(2)根据所给数据,该烧碱样品的物质的量浓度为_______  (保留两位有效数字)。
(保留两位有效数字)。
(3)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是_______。
Ⅱ.某研究小组为测定软锰矿中 的质量分数,实验步骤如下:准确称取
的质量分数,实验步骤如下:准确称取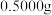 软锰矿样品,加入
软锰矿样品,加入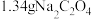 再加入足量的稀硫酸并加热(杂质不参加反应),充分反应之后冷却、滤去杂质,将所得溶液全部转移到
再加入足量的稀硫酸并加热(杂质不参加反应),充分反应之后冷却、滤去杂质,将所得溶液全部转移到 容量瓶中并定容。取出
容量瓶中并定容。取出 待测液置于锥形瓶中,再用
待测液置于锥形瓶中,再用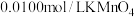 标准溶液进行滴定,当滴入
标准溶液进行滴定,当滴入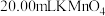 溶液时恰好完全反应。(已知
溶液时恰好完全反应。(已知 、
、 在酸性条件下均能将
在酸性条件下均能将 氧化,且还原产物均为
氧化,且还原产物均为 。)
。)
(4) 标准溶液应该置于
标准溶液应该置于_______ 滴定管中,滴定终点的实验现象是_______
(5) 和
和 在酸性条件下反应的离子方程式为
在酸性条件下反应的离子方程式为_______
(6)根据实验数据计算,软锰矿中 的质量分数为
的质量分数为_______  。
。
| 滴定序号 | 待测液体积(mL) | 所消耗盐酸标准液的体积(mL) | ||
| 滴定前 | 滴定后 | 消耗的体积 | ||
| 1 | 25.00 | 0.50 | 26.80 | 26.30 |
| 2 | 25.00 | |||
| 3 | 25.00 | 5.00 | 31.34 | 26.34 |
 盐酸标准液第二次滴定前后
盐酸标准液第二次滴定前后 滴定管中液面的位置,该次滴定所用标准盐酸体积为
滴定管中液面的位置,该次滴定所用标准盐酸体积为 。
。
(2)根据所给数据,该烧碱样品的物质的量浓度为
 (保留两位有效数字)。
(保留两位有效数字)。(3)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是_______。
| A.碱式滴定管未用待测氢氧化钠溶液润洗就直接注入溶液 |
| B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥 |
| C.读取盐酸体积时,滴定结束时俯视读数 |
| D.酸式滴定管在滴定前有气泡,滴定后气泡消失 |
Ⅱ.某研究小组为测定软锰矿中
 的质量分数,实验步骤如下:准确称取
的质量分数,实验步骤如下:准确称取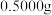 软锰矿样品,加入
软锰矿样品,加入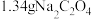 再加入足量的稀硫酸并加热(杂质不参加反应),充分反应之后冷却、滤去杂质,将所得溶液全部转移到
再加入足量的稀硫酸并加热(杂质不参加反应),充分反应之后冷却、滤去杂质,将所得溶液全部转移到 容量瓶中并定容。取出
容量瓶中并定容。取出 待测液置于锥形瓶中,再用
待测液置于锥形瓶中,再用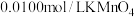 标准溶液进行滴定,当滴入
标准溶液进行滴定,当滴入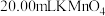 溶液时恰好完全反应。(已知
溶液时恰好完全反应。(已知 、
、 在酸性条件下均能将
在酸性条件下均能将 氧化,且还原产物均为
氧化,且还原产物均为 。)
。)(4)
 标准溶液应该置于
标准溶液应该置于(5)
 和
和 在酸性条件下反应的离子方程式为
在酸性条件下反应的离子方程式为(6)根据实验数据计算,软锰矿中
 的质量分数为
的质量分数为 。
。
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】硫脲[CS(NH2)2]是一种白 色晶体,易溶于水,受热发生异构化反应而生成硫氰化铵。用氰氨化钙(CaCN2)与硫氢化钙溶液反应制取硫脲的实验装置(夹持及加热装置省略)如图。
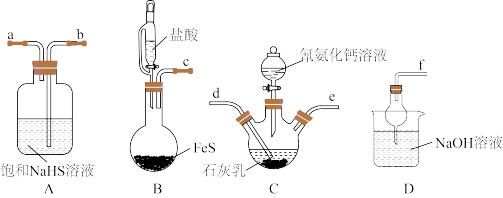
回答下列问题:
(1)上述装置的连接顺序为_______ (按气流方向,用小写字母表示)。
(2)当装置C中出现_______ 现象时,关闭装置B中恒压滴液漏斗活塞;再打开装置C中分液漏斗活塞,加热至80℃时生成硫脲和一种碱,该反应的化学方程式为_______ ,控制温度为80℃的原因是_______ 。
(3)测定硫脲纯度的方法如下。
步骤1:称取mg产品,加水溶解配成1 L溶液。
步骤2:量取25.00 mL上述溶液注入碘量瓶中加入V1mLc1 mol·L-1 I2的标准溶液及适量的NaOH溶液(2NaOH+I2= NaIO+NaI+H2O),于暗处放置10 min。
步骤3:加水及适量的稀硫酸,摇匀。
步骤4:加入少量淀粉溶液,用c2 mol·L-1 Na2S2O3标准溶液滴定剩余的I2(I2+2 Na2S2O3=2NaI+ Na2S4O6) ,滴定至终点时消耗Na2S2O3溶液V2 mL。
①“步骤2”中NaIO氧化硫脲生成尿素、硫酸和碘化钠的离子方程式为_______ 。
②“步骤4”滴定终点时的现象是_______ 。
③产品中CS( NH2 )2的质量分数为_______ 。

回答下列问题:
(1)上述装置的连接顺序为
(2)当装置C中出现
(3)测定硫脲纯度的方法如下。
步骤1:称取mg产品,加水溶解配成1 L溶液。
步骤2:量取25.00 mL上述溶液注入碘量瓶中加入V1mLc1 mol·L-1 I2的标准溶液及适量的NaOH溶液(2NaOH+I2= NaIO+NaI+H2O),于暗处放置10 min。
步骤3:加水及适量的稀硫酸,摇匀。
步骤4:加入少量淀粉溶液,用c2 mol·L-1 Na2S2O3标准溶液滴定剩余的I2(I2+2 Na2S2O3=2NaI+ Na2S4O6) ,滴定至终点时消耗Na2S2O3溶液V2 mL。
①“步骤2”中NaIO氧化硫脲生成尿素、硫酸和碘化钠的离子方程式为
②“步骤4”滴定终点时的现象是
③产品中CS( NH2 )2的质量分数为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】柠檬酸(分子式为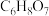 ,其结构简式为
,其结构简式为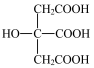 ,相对分子质量为192)是一种三元弱酸,是一种食品添加剂,经常出现在我们的日常生活中,特别是在各类碳酸饮料中广泛使用,某实验小组在实验室探究雪碧中柠檬酸的含量,以检测其是否对人产生危害。
,相对分子质量为192)是一种三元弱酸,是一种食品添加剂,经常出现在我们的日常生活中,特别是在各类碳酸饮料中广泛使用,某实验小组在实验室探究雪碧中柠檬酸的含量,以检测其是否对人产生危害。
已知:雪碧中主要包括:水、果葡萄浆、白砂糖、食品添加剂(二氧化碳、柠檬酸、柠檬酸钠、苯甲酸钠)、食用香精,其中主要的酸性物质是二氧化碳和柠檬酸。
具体实验操作如下,请回答下列问题:
(1)量取1L雪碧,在热水浴中加热并不断搅拌,直至没有气泡为止,目的是___________ 。
(2)用___________ (填“酸式”或“碱式”)滴定管量取25.00 mL雪碧于锥形瓶中,滴加几滴指示剂,用 的
的 溶液滴定至终点,重复上述操作两次,实验数据记录如下:
溶液滴定至终点,重复上述操作两次,实验数据记录如下:
①指示剂为___________ ;
②滴定过程中反应的化学方程式为___________ ;
③滴定终点的实验现象是___________ ;
④雪碧中柠檬酸的含量为___________  (精确到0.1)。
(精确到0.1)。
(3)下列操作会导致测定结果偏大的是___________(填选项字母)。
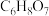 ,其结构简式为
,其结构简式为 ,相对分子质量为192)是一种三元弱酸,是一种食品添加剂,经常出现在我们的日常生活中,特别是在各类碳酸饮料中广泛使用,某实验小组在实验室探究雪碧中柠檬酸的含量,以检测其是否对人产生危害。
,相对分子质量为192)是一种三元弱酸,是一种食品添加剂,经常出现在我们的日常生活中,特别是在各类碳酸饮料中广泛使用,某实验小组在实验室探究雪碧中柠檬酸的含量,以检测其是否对人产生危害。已知:雪碧中主要包括:水、果葡萄浆、白砂糖、食品添加剂(二氧化碳、柠檬酸、柠檬酸钠、苯甲酸钠)、食用香精,其中主要的酸性物质是二氧化碳和柠檬酸。
具体实验操作如下,请回答下列问题:
(1)量取1L雪碧,在热水浴中加热并不断搅拌,直至没有气泡为止,目的是
(2)用
 的
的 溶液滴定至终点,重复上述操作两次,实验数据记录如下:
溶液滴定至终点,重复上述操作两次,实验数据记录如下:| 实验序号 | 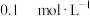 的雪碧的体积/mL 的雪碧的体积/mL | 滴定前盛 溶液的滴定管的读数/mL 溶液的滴定管的读数/mL | 滴定后盛 溶液的滴定管的读数/mL 溶液的滴定管的读数/mL |
| 1 | 25.00 | 0.00 | 5.80 |
| 2 | 25.00 | 8.00 | 13.90 |
| 3 | 25.00 | 2.00 | 6.20 |
②滴定过程中反应的化学方程式为
③滴定终点的实验现象是
④雪碧中柠檬酸的含量为
 (精确到0.1)。
(精确到0.1)。(3)下列操作会导致测定结果偏大的是___________(填选项字母)。
| A.滴定前,未在热水浴中加热或搅拌雪碧 |
| B.未用雪碧润洗滴定管 |
C.盛装 溶液的滴定管,滴定前尖嘴处有一气泡,滴定后气泡消失 溶液的滴定管,滴定前尖嘴处有一气泡,滴定后气泡消失 |
D.盛装 溶液的滴定管,滴定前仰视读数,滴定后俯视读数 溶液的滴定管,滴定前仰视读数,滴定后俯视读数 |
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某学习小组用0.1000mol/LNaOH标准溶液来测定未知物质的量浓度的盐酸时,选择酚酞作指示剂。请回答下列问题:
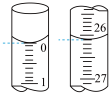
(1)若滴定开始和结束时,该仪器中溶液读数如图所示,所用NaOH标准溶液的体积为___________ mL。
依据表中数据计算该盐酸的物质的量浓度为___________ mol/L。
(3)下列操作会使所测结果偏高的是___________ (填字母)。
A.滴定前用蒸馏水冲洗锥形瓶
B.滴定过程中振荡锥形瓶时不慎将瓶内溶液溅出
C.滴定过程中不慎将数滴碱液滴在锥形瓶外
D.碱式滴定管在滴定前有气泡,滴定后气泡消失
E.读取NaOH体积时,开始仰视读数,滴定结束时俯视读数
(4)用0.1mol/LNaOH溶液分别滴定体积均为20.00mL、浓度均为0.1mol/L的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。___________ (填“I”或“Ⅱ”)。
② 和
和 的关系:
的关系:
___________  (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。
③M点对应溶液中,各离子的物质的量浓度由大到小的顺序是___________ 。
(1)若滴定开始和结束时,该仪器中溶液读数如图所示,所用NaOH标准溶液的体积为
| 滴定次数 | 待测盐酸的体积 | 标准NaOH溶液体积 | |
| 滴定前的刻度 | 滴定后的刻度mL | ||
| 第一次 | 25.00mL | 0.00mL | 26.11mL |
| 第二次 | 25.00mL | 1.56mL | 30.30mL |
| 第三次 | 25.00mL | 0.22mL | 26.31mL |
(3)下列操作会使所测结果偏高的是
A.滴定前用蒸馏水冲洗锥形瓶
B.滴定过程中振荡锥形瓶时不慎将瓶内溶液溅出
C.滴定过程中不慎将数滴碱液滴在锥形瓶外
D.碱式滴定管在滴定前有气泡,滴定后气泡消失
E.读取NaOH体积时,开始仰视读数,滴定结束时俯视读数
(4)用0.1mol/LNaOH溶液分别滴定体积均为20.00mL、浓度均为0.1mol/L的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。

②
 和
和 的关系:
的关系:
 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。③M点对应溶液中,各离子的物质的量浓度由大到小的顺序是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】叠氮化钠(NaN3)是一种防腐剂和分析试剂,在有机合成和汽车行业也有重要应用。学习小组对叠氮化钠的制备和产品纯度测定进行相关探究。
查阅资料:
I、氨基钠(NaNH2)熔点为208°C,易潮解和氧化;N2O有强氧化性,不与酸、碱反应;叠氮酸(HN3)不稳定,易分解爆炸。
II、2HNO3 + 8HCl + 4SnCl2=4SnCl 4+ 5H2O+ N2O↑,2NaNH2 +N2O NaN3 + NaOH+ NH3。
NaN3 + NaOH+ NH3。
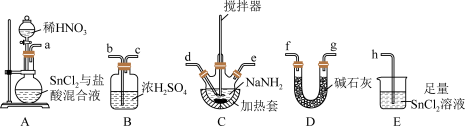
现有以上实验装置,请回答下列问题:
(1)制备NaN3
①按气流方向,上述装置合理的连接顺序为___________ (填仪器接口字母)。
②实验时E中生成SnO2·xH2O沉淀,且产生无色无味的无毒气体,反应的化学方程式为___________ 。
③C处充分反应后,停止加热,需继续进行的操作为___________ ,其目的为___________ 。
(2)产率计算
①称取2.0g叠氮化钠试样,配成100mL溶液,并量取10.00mL溶液于锥形瓶中。
②用滴定管加入0.10 mol·L-1六硝酸铈铵[(NH4 )2Ce(NO3)6]溶液40.00mL[发生的反应为2(NH4 )2Ce(NO3)6+ 2NaN3= 4NH4 NO3 + 2Ce( NO3)3 + 2NaNO3 +3N2↑](假设杂质均不参与反应)。
③充分反应后将溶液稀释并酸化,滴2入滴邻菲罗啉指示液,并用0.10 mol·L-1硫酸亚铁铵[(NH4 )2Ce(NO3)6]为标准液,滴定过量的Ce4+,终点时消耗标准溶液20. 00 mL(滴定原理:Ce4++Fe2+=Ce3++Fe3+ )。计算可知叠氮化钠的质量分数为___________ (保留2位有效数字)。若其他操作及读数均正确,滴定到终点后,下列操作会导致所测定样品中叠氮化钠质量分数偏大的是___________ (填字母代号)。
A.锥形瓶使用叠氮化钠溶液润洗
B.滴加六硝酸铈铵溶液时,滴加前仰视读数,滴加后俯视读数
C.滴加硫酸亚铁铵标准溶液时,开始时尖嘴处无气泡,结束时出现气泡
D.滴定过程中,将挂在锥形瓶壁上的硫酸亚铁铵标准液滴用蒸馏水冲进瓶内
(3)叠氮化钠有毒,可以使用次氯酸钠溶液对含有叠氮化钠的溶液进行销毁,反应后溶液碱性明显增强,且产生无色无味的无毒气体,试写出反应的离子方程式:___________ 。
查阅资料:
I、氨基钠(NaNH2)熔点为208°C,易潮解和氧化;N2O有强氧化性,不与酸、碱反应;叠氮酸(HN3)不稳定,易分解爆炸。
II、2HNO3 + 8HCl + 4SnCl2=4SnCl 4+ 5H2O+ N2O↑,2NaNH2 +N2O
 NaN3 + NaOH+ NH3。
NaN3 + NaOH+ NH3。
现有以上实验装置,请回答下列问题:
(1)制备NaN3
①按气流方向,上述装置合理的连接顺序为
②实验时E中生成SnO2·xH2O沉淀,且产生无色无味的无毒气体,反应的化学方程式为
③C处充分反应后,停止加热,需继续进行的操作为
(2)产率计算
①称取2.0g叠氮化钠试样,配成100mL溶液,并量取10.00mL溶液于锥形瓶中。
②用滴定管加入0.10 mol·L-1六硝酸铈铵[(NH4 )2Ce(NO3)6]溶液40.00mL[发生的反应为2(NH4 )2Ce(NO3)6+ 2NaN3= 4NH4 NO3 + 2Ce( NO3)3 + 2NaNO3 +3N2↑](假设杂质均不参与反应)。
③充分反应后将溶液稀释并酸化,滴2入滴邻菲罗啉指示液,并用0.10 mol·L-1硫酸亚铁铵[(NH4 )2Ce(NO3)6]为标准液,滴定过量的Ce4+,终点时消耗标准溶液20. 00 mL(滴定原理:Ce4++Fe2+=Ce3++Fe3+ )。计算可知叠氮化钠的质量分数为
A.锥形瓶使用叠氮化钠溶液润洗
B.滴加六硝酸铈铵溶液时,滴加前仰视读数,滴加后俯视读数
C.滴加硫酸亚铁铵标准溶液时,开始时尖嘴处无气泡,结束时出现气泡
D.滴定过程中,将挂在锥形瓶壁上的硫酸亚铁铵标准液滴用蒸馏水冲进瓶内
(3)叠氮化钠有毒,可以使用次氯酸钠溶液对含有叠氮化钠的溶液进行销毁,反应后溶液碱性明显增强,且产生无色无味的无毒气体,试写出反应的离子方程式:
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某烧碱样品含少量不与酸作用的杂质,为测定纯度,进行以下滴定操作:
A.在 250 mL 的容量瓶中定容配成 250 mL 烧碱溶液
B.用移液管移取 25 mL 烧碱溶液于锥形瓶中并滴几滴指示剂甲基橙
C.在天平上准确称取烧碱样品 Wg,在烧杯中用蒸馏水溶解
D.将物质的量浓度为 c 的标准盐酸溶液装入酸式滴定管,调节液面,记开始读数为 V1 E.在锥形瓶下垫一张白纸,滴定至终点,记读数 V2
回答下列各问题:
(1)正确操作步骤的顺序是(用字母填写)_______ → ________ → ________ →D→ ______ 。
(2)D 步骤中液面应调节到______ ,尖嘴部分应 ______ 。
(3)滴定终点时锥形瓶中颜色变化是______ 。
(4)若酸式滴定管不用标准盐酸润洗,在其他操作均正确的前提下,会对测定结果(指烧碱的纯度)有何影响?______ (填“偏高”、“低”或“不变”)
(5)该烧碱样品纯度的计算式为______ 。
A.在 250 mL 的容量瓶中定容配成 250 mL 烧碱溶液
B.用移液管移取 25 mL 烧碱溶液于锥形瓶中并滴几滴指示剂甲基橙
C.在天平上准确称取烧碱样品 Wg,在烧杯中用蒸馏水溶解
D.将物质的量浓度为 c 的标准盐酸溶液装入酸式滴定管,调节液面,记开始读数为 V1 E.在锥形瓶下垫一张白纸,滴定至终点,记读数 V2
回答下列各问题:
(1)正确操作步骤的顺序是(用字母填写)
(2)D 步骤中液面应调节到
(3)滴定终点时锥形瓶中颜色变化是
(4)若酸式滴定管不用标准盐酸润洗,在其他操作均正确的前提下,会对测定结果(指烧碱的纯度)有何影响?
(5)该烧碱样品纯度的计算式为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】欲测定某NaOH溶液的物质的量浓度,可用0.100 0 mol·L-1的HCl标准溶液滴定待测碱(用甲基橙作指示剂)。请回答下列问题:
(1)滴定时,盛装待测NaOH溶液的仪器名称为________ 。
(2)滴定至终点的颜色变化为____________ 。
(3)若甲学生在实验过程中做了三组平行实验,数据记录如下,则此时消耗标准溶液的体积为__________ 。计算出待测NaOH溶液的物质的量浓度为______ 。(保留四位有效数字)
(1)滴定时,盛装待测NaOH溶液的仪器名称为
(2)滴定至终点的颜色变化为
(3)若甲学生在实验过程中做了三组平行实验,数据记录如下,则此时消耗标准溶液的体积为
| 实验 序号 | 待测NaOH溶液的体积/mL | 0.100 0 mol·L-1 HCl溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 0.00 | 26.29 |
| 2 | 25.00 | 1.00 | 31.00 |
| 3 | 25.00 | 1.00 | 27.31 |
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某高二化学研究性学习小组对铬及其化合物进行实验探究。
查阅资料:①元素铬(Cr)在溶液中主要以Cr3+ (蓝紫色)、Cr(OH) (绿色)、Cr2O
(绿色)、Cr2O (橙色)、CrO
(橙色)、CrO (黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体;②Cr3+与Al3+化学性质相似。
(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体;②Cr3+与Al3+化学性质相似。
实验探究一:Cr3+在不同酸碱性条件下转化情况
(1)在Cr2(SO4)3溶液中逐滴加入NaOH溶液直至过量,可观察到的现象是___________ 。
实验探究二:现测某工业废水中铬的含量
步骤I.取25. 00 mL废水(含有一定量K2Cr2O7 和K2CrO4)于100 ml容量瓶中,加水稀释至刻度,摇匀,移取25.00mL稀释后的废水于锥形瓶中,加入适量稀硫酸酸化。
步骤II.加入稍过量的碘化钾溶液,滴入几滴指示剂。
步骤III.用0.1000 mol•L-1 Na2S2O3 溶液滴定(I2+2Na2S2O3=2NaI+Na2S4O6),记录滴定前和滴定终点数据。
步骤IV……
步骤V.处理数据:并将。上述反应后溶液进行处理(防止铬的污染并对资源回收利用)。
(2)步骤I加入适量稀硫酸酸化发生反应的离子方程式是___________ ,也为步骤II提供了酸性环境;步骤I的指示剂为___________ ;步骤IV为___________ 。
(3)0.1000mol•L-1Na2S2O3溶液装在___________ (填“酸式”或“碱式”)滴定管中。若某次滴定终点时消耗0.1000mol•L-1 Na2S2O3溶液体积为12. 50 mL。计算工业废水中铬元素的含量是___________ g•L-1(保留3位有效数字)。
(4)误差分析:①若盛装Na2S2O3溶液的滴定管没有润洗,测定结果会___________ (填“ 偏大”、“偏小”或“不变”,下同);②若步骤I加入稀硫酸酸化过量(溶液pH过低) ,测定结果会___________ 。
实验探究三:废水中铬的处理方法
为使废水能达标排放,作如下处理
(5)写出废水中加入绿矾和稀硫酸,Cr2O 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
查阅资料:①元素铬(Cr)在溶液中主要以Cr3+ (蓝紫色)、Cr(OH)
 (绿色)、Cr2O
(绿色)、Cr2O (橙色)、CrO
(橙色)、CrO (黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体;②Cr3+与Al3+化学性质相似。
(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体;②Cr3+与Al3+化学性质相似。实验探究一:Cr3+在不同酸碱性条件下转化情况
(1)在Cr2(SO4)3溶液中逐滴加入NaOH溶液直至过量,可观察到的现象是
实验探究二:现测某工业废水中铬的含量
步骤I.取25. 00 mL废水(含有一定量K2Cr2O7 和K2CrO4)于100 ml容量瓶中,加水稀释至刻度,摇匀,移取25.00mL稀释后的废水于锥形瓶中,加入适量稀硫酸酸化。
步骤II.加入稍过量的碘化钾溶液,滴入几滴指示剂。
步骤III.用0.1000 mol•L-1 Na2S2O3 溶液滴定(I2+2Na2S2O3=2NaI+Na2S4O6),记录滴定前和滴定终点数据。
步骤IV……
步骤V.处理数据:并将。上述反应后溶液进行处理(防止铬的污染并对资源回收利用)。
(2)步骤I加入适量稀硫酸酸化发生反应的离子方程式是
(3)0.1000mol•L-1Na2S2O3溶液装在
(4)误差分析:①若盛装Na2S2O3溶液的滴定管没有润洗,测定结果会
实验探究三:废水中铬的处理方法
为使废水能达标排放,作如下处理

(5)写出废水中加入绿矾和稀硫酸,Cr2O
 发生反应的离子方程式为
发生反应的离子方程式为
您最近半年使用:0次



