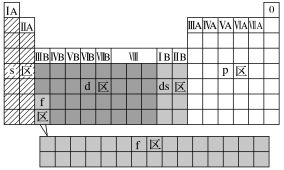
1869年俄国化学家门捷列夫制出第一张元素周期表元素,下图是元素周期表的一部分。回答下列问题:
(1)Ga的原子结构示意图为________ 。
(2)Ge位于金属元素和非金属元素的分界处,可以做________ 材料,其最高正价为________ 。
(3)Cl元素的最高价氧化物对应的水化物为________ (填化学式),设计实验方案证明Cl的得电子能力强于S。
(4)Bi的最高价氧化物为________ (填化学式), ,
, 混合溶液中滴入
混合溶液中滴入 溶液,溶液变为紫红色,
溶液,溶液变为紫红色, 转化为可溶的
转化为可溶的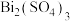 ,该反应的离子方程式为
,该反应的离子方程式为________ 。
(5)根据元素周期律,推断
①表中气态氢化物中稳定性最高的物质为________ (填名称),该物质的电子式为________ 。
②氢化物的还原性:
________  (填“>”、“<”、或“=”)。
(填“>”、“<”、或“=”)。
③ 、
、 、
、 的酸性由强到弱的顺序为
的酸性由强到弱的顺序为________ 。
④ 、
、 、
、 、
、 ,四种离子半径由大到小的顺序为
,四种离子半径由大到小的顺序为________ (用离子符号表示)。
B | C | N | O | F |
Al | Si | P | S | Cl |
Ga | Ge | As | Se | Br |
In | Sn | Sb | Te | I |
Tl | Pb | Bi | Po | At |
(2)Ge位于金属元素和非金属元素的分界处,可以做
(3)Cl元素的最高价氧化物对应的水化物为
(4)Bi的最高价氧化物为
 ,
, 混合溶液中滴入
混合溶液中滴入 溶液,溶液变为紫红色,
溶液,溶液变为紫红色, 转化为可溶的
转化为可溶的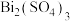 ,该反应的离子方程式为
,该反应的离子方程式为(5)根据元素周期律,推断
①表中气态氢化物中稳定性最高的物质为
②氢化物的还原性:

 (填“>”、“<”、或“=”)。
(填“>”、“<”、或“=”)。③
 、
、 、
、 的酸性由强到弱的顺序为
的酸性由强到弱的顺序为④
 、
、 、
、 、
、 ,四种离子半径由大到小的顺序为
,四种离子半径由大到小的顺序为
更新时间:2024-04-10 21:46:55
|
【知识点】 元素周期表提供的元素信息解读
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】2019年是元素周期表诞生150周年,元素周期表(律)在学习、研究和生产实践中有很重要的作用。下表为元素周期表的一部分,回答下列问题。
(1)元素①~⑧中,金属性最强的是________ (填元素符号)。
(2)中国青年化学家姜雪峰被国际组织推选为“元素⑦代言人”,元素⑦的原子结构示意图是_________ ,其氢化物的电子式是_________ 。
(3)比较元素②、③的最高价氧化物对应水化物的酸性:______ >______ (填化学式)。说明你判断的理由:_________ 。
(4)主族元素砷(As)的部分信息如图所示。

①砷(As)在周期表中的位置是______ 。
②下列说法正确的是_______ (填序号)。
a.砷元素的最高化合价为+4
b.推测砷有多种氧化物
c.③的气态氢化物的还原性大于砷的气态氢化物的还原性
(5)某小组同学设计实验比较VIIA元素的非金属性:Cl>Br>I。已知:常温下浓盐酸与高锰酸钾反应生成氯气。
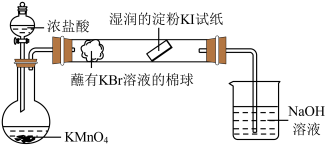
打开分液漏斗的活塞,烧瓶中产生黄绿色气体,蘸有KBr溶液的棉球变为橙红色,湿润的淀粉KI试纸变蓝,据此现象能否说明非金属性:Br >I,并说明理由_________ 。
| IA | 0 | |||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ||||||||
(2)中国青年化学家姜雪峰被国际组织推选为“元素⑦代言人”,元素⑦的原子结构示意图是
(3)比较元素②、③的最高价氧化物对应水化物的酸性:
(4)主族元素砷(As)的部分信息如图所示。

①砷(As)在周期表中的位置是
②下列说法正确的是
a.砷元素的最高化合价为+4
b.推测砷有多种氧化物
c.③的气态氢化物的还原性大于砷的气态氢化物的还原性
(5)某小组同学设计实验比较VIIA元素的非金属性:Cl>Br>I。已知:常温下浓盐酸与高锰酸钾反应生成氯气。

打开分液漏斗的活塞,烧瓶中产生黄绿色气体,蘸有KBr溶液的棉球变为橙红色,湿润的淀粉KI试纸变蓝,据此现象能否说明非金属性:Br >I,并说明理由
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知A、B两种元素,A的原子序数为x,A和B所在周期的元素种类数目分别为m和n。
(1)如果A和B同在IA族,当B在A的上一周期时,B的原子序数为___________ ,当B在A的下一周期时,B的原子序数为___________ ;
(2)如果A和B同在ⅦA族,当B在A的上一周期时,B的原子序数为___________ ;当B在A的下一周期时,B的原子序数为___________ 。
(1)如果A和B同在IA族,当B在A的上一周期时,B的原子序数为
(2)如果A和B同在ⅦA族,当B在A的上一周期时,B的原子序数为
您最近一年使用:0次