某中药试剂 具有泻下通便、清火消肿等功效,该药剂
具有泻下通便、清火消肿等功效,该药剂 的化学式为
的化学式为 ,
, 是原子序数依次增大的短周期元素,最外层电子数之和为14。
是原子序数依次增大的短周期元素,最外层电子数之和为14。 与
与 同主族,
同主族, 与
与 同主族,且
同主族,且 满足最高正价与最低负价的绝对值之差为4。下列说法错误的是
满足最高正价与最低负价的绝对值之差为4。下列说法错误的是
 具有泻下通便、清火消肿等功效,该药剂
具有泻下通便、清火消肿等功效,该药剂 的化学式为
的化学式为 ,
, 是原子序数依次增大的短周期元素,最外层电子数之和为14。
是原子序数依次增大的短周期元素,最外层电子数之和为14。 与
与 同主族,
同主族, 与
与 同主族,且
同主族,且 满足最高正价与最低负价的绝对值之差为4。下列说法错误的是
满足最高正价与最低负价的绝对值之差为4。下列说法错误的是A.非金属性: |
B. 分别与 分别与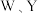 形成的18电子分子和10电子分子 形成的18电子分子和10电子分子 |
C.由 形成的化合物既含离子键又含共价键 形成的化合物既含离子键又含共价键 |
D.简单离子半径: |
更新时间:2024-04-12 16:15:49
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】有五组同族元素的物质,在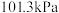 时测定它们的沸点(℃)如下表所示:
时测定它们的沸点(℃)如下表所示:
对应表中内容,下列各项中正确的是
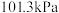 时测定它们的沸点(℃)如下表所示:
时测定它们的沸点(℃)如下表所示:| ① | 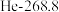 | (a)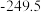 | 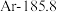 | 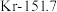 |
| ② | 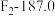 | 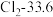 | (b)58.7 | 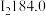 |
| ③ | (c)19.4 | 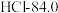 |  | 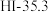 |
| ④ | 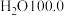 |  | (d)-42.0 |  |
| ⑤ | 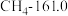 | 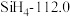 | 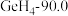 | (e)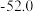 |
A.a、b、c的化学式分别为Xe、 、HF 、HF |
B.第④组中各化合物的稳定性顺序为: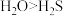 ,因为水中存在氢键 ,因为水中存在氢键 |
C.第②组物质均有氧化性;第③组物质酸性强弱是 |
| D.上表中同族物质对应的氢化物的沸点,均随相对分子质量的增大而升高 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列说法正确的是
①甲醛中碳的杂化方式为sp 2
②若R2-和M+的电子层结构相同,则原子序数:R>M
③F2、Cl2、Br2、I2熔、沸点随相对分子质量的增大而升高
④由于非金属性:Cl>Br>I,所以酸性:HCl>HBr>HI
⑤氨的液化会破坏共价键
⑥C与H形成的化合物中只存在极性共价键
⑦Na2O2固体中的阴离子和阳离子个数比是1∶2
①甲醛中碳的杂化方式为sp 2
②若R2-和M+的电子层结构相同,则原子序数:R>M
③F2、Cl2、Br2、I2熔、沸点随相对分子质量的增大而升高
④由于非金属性:Cl>Br>I,所以酸性:HCl>HBr>HI
⑤氨的液化会破坏共价键
⑥C与H形成的化合物中只存在极性共价键
⑦Na2O2固体中的阴离子和阳离子个数比是1∶2
| A.②⑤⑥ | B.③⑤⑦ | C.②④⑤ | D.①③⑦ |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】下列关于 、
、 原子结构的分析中正确的是
原子结构的分析中正确的是
 、
、 原子结构的分析中正确的是
原子结构的分析中正确的是A.原子半径: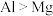 | B.基态原子未成对电子数: |
C.第一电离能: | D.电负性: |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】短周期主族元素W、X、Y、Z的原子序数依次增大,X、Y同主族,四种元素形成的一种用途广泛的单体结构如图所示。下列说法正确的是


| A.原子半径:W<X<Y<Z |
| B.常温下,X的氢化物为气体 |
| C.Y、Z的最高价氧化物对应的水化物均为强酸 |
| D.W既可形成简单阳离子又可形成简单阴离子 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】我国科学家合成了一种深紫外非线性光学晶体新材料 ,晶体中阴离子为
,晶体中阴离子为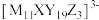 。元素M、X、Y、Z均为短周期元素,M、Y与Z同周期,M的最外层电子数比次外层电子数多1,Z为电负性最强的元素,Y是地壳中含量最高的元素,X的
。元素M、X、Y、Z均为短周期元素,M、Y与Z同周期,M的最外层电子数比次外层电子数多1,Z为电负性最强的元素,Y是地壳中含量最高的元素,X的 轨道有3个电子。下列说法中不正确的是
轨道有3个电子。下列说法中不正确的是
 ,晶体中阴离子为
,晶体中阴离子为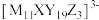 。元素M、X、Y、Z均为短周期元素,M、Y与Z同周期,M的最外层电子数比次外层电子数多1,Z为电负性最强的元素,Y是地壳中含量最高的元素,X的
。元素M、X、Y、Z均为短周期元素,M、Y与Z同周期,M的最外层电子数比次外层电子数多1,Z为电负性最强的元素,Y是地壳中含量最高的元素,X的 轨道有3个电子。下列说法中不正确的是
轨道有3个电子。下列说法中不正确的是A.电负性: |
B.简单离子半径: |
C.简单气态氢化物的稳定性: |
| D.M最高价氧化物对应水化物为强酸 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】某短周期非金属元素的原子核外最外层电子数是次外层电子数的一半,下列说法错误的是( )
| A.该元素最高价氧化物既能与酸反应,又能与碱反应,故称该氧化物为两性氧化物 |
| B.该元素在自然界中只以化合态存在 |
| C.该元素单质常用作半导体材料 |
| D.甲烷比该元素的气态氢化物稳定 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】下列化合物中,所有化学键都是共价键的是
| A.NH4Cl | B.NaOH |
| C.Na2O2 | D.CH4 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】有共价键的离子化合物是
| A.HCl | B.Ba(OH)2 | C.MgCl2 | D.H2O2 |
您最近一年使用:0次



