下列说法正确的是
①甲醛中碳的杂化方式为sp 2
②若R2-和M+的电子层结构相同,则原子序数:R>M
③F2、Cl2、Br2、I2熔、沸点随相对分子质量的增大而升高
④由于非金属性:Cl>Br>I,所以酸性:HCl>HBr>HI
⑤氨的液化会破坏共价键
⑥C与H形成的化合物中只存在极性共价键
⑦Na2O2固体中的阴离子和阳离子个数比是1∶2
①甲醛中碳的杂化方式为sp 2
②若R2-和M+的电子层结构相同,则原子序数:R>M
③F2、Cl2、Br2、I2熔、沸点随相对分子质量的增大而升高
④由于非金属性:Cl>Br>I,所以酸性:HCl>HBr>HI
⑤氨的液化会破坏共价键
⑥C与H形成的化合物中只存在极性共价键
⑦Na2O2固体中的阴离子和阳离子个数比是1∶2
| A.②⑤⑥ | B.③⑤⑦ | C.②④⑤ | D.①③⑦ |
更新时间:2023-10-24 21:53:37
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列叙述中错误的是
| A.原子半径:Na>Si>Cl | B.稳定性:HCl>H2S>SiH4 |
| C.金属性:Na>Mg>Al | D.酸性:H3PO4<H2SO3<HClO |
您最近半年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】四种短周期主族元素X、Y、Z和W,原子序数依次增大,X和Y的单质化合生成气体A,A分子中的电子数与氖原子相同,X和W的单质化合生成气体B,常温下0.1mol/L的B溶液的pH=1,气体A和气体B相遇产生白烟,X与Z可按原子个数比1:1形成离子化合物C。下列说法正确的是
| A.原子半径由大到小的顺序为 r(W)>r(Y)>r(Z)>r(X) |
| B.Z 元素最高价氧化物的水化物可与 B 发生反应 |
| C.Y 的非金属性比 X 强,其单质非常活泼 |
| D.Y 的含氧酸比 W 的含氧酸酸性强 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列有关比较正确的是
| A.键角:H2O>NH3>CH4 |
| B.晶格能:NaBr>NaCl>MgO |
| C.键的极性:N—H 键>O—H 键>F—H 键 |
| D.热稳定性:HF>H2O>NH3 |
您最近半年使用:0次
【推荐2】本维莫德可用于治疗银屑病和湿疹,结构如图所示,下列说法中不正确的是
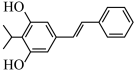

| A.分子中有2种官能团 |
| B.可发生酯化反应 |
C.分子中存在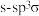 键 键 |
D.1 mol该分子与碳酸钠溶液反应,可生成1 mol  |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】分子中存在π 键,且碳原子全部以sp杂化轨道成键的是( )
| A.CH3CH3 | B.CH2=CH2 | C.CH≡CH | D.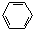 |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐2】我国自主研发对二甲苯的绿色合成路线如下图所示,有关说法不正确的是
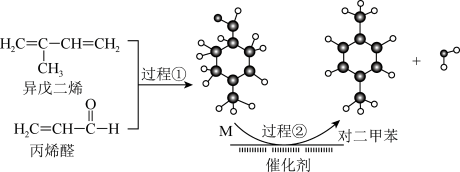
已知: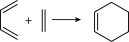 称为狄尔斯−阿德耳反应,又称为双烯合成。
称为狄尔斯−阿德耳反应,又称为双烯合成。

已知:
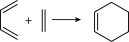 称为狄尔斯−阿德耳反应,又称为双烯合成。
称为狄尔斯−阿德耳反应,又称为双烯合成。| A.过程①发生了加成反应 |
B.过程②中六元环上C原子的杂化方式都是由 变为 变为 |
| C.该反应的副产物可能有间二甲苯 |
D.M的结构简式为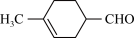 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】类推的思维方法在化学学习与研究中有时会产生错误结论,因此类推的结论最终要经过实验的检验,才能决定其正确与否。下列几种类推结论,正确的是
| A.NH3分子的空间结构为三角锥形,则BCl3分子的空间结构也为三角锥形 |
| B.CF4 的熔沸点小于CCl4,则NCl3的熔沸点小于PCl3 |
| C.N≡N由于键能大而结构稳定,则C≡ C键能也大结构也很稳定 |
| D.Cu( OH)2可以溶解在浓氨水中,则Al( OH)3也可以溶解在浓氨水中 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列说法正确的是
| A.冰熔化时,分子中化学键发生断裂 |
| B.HF、HCl、HBr、HI的热稳定性依次减弱与氢键无关 |
| C.非极性键不可能存在于离子化合物中,由非金属元素组成的化合物中一定不存在离子键 |
| D.含有阴离子的物质一定含有阳离子 |
您最近半年使用:0次

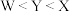



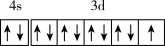
 的中心原子为
的中心原子为 杂化
杂化

