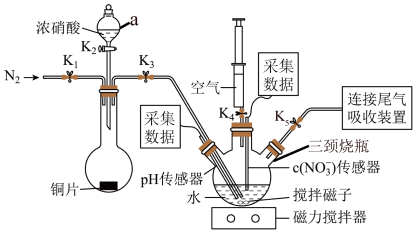
某实验小组为验证NO2与水反应的产物与课本方程式中的产物是否一致,设计如下装置进行实验(夹持装置已略去,装置气密性已检验)。
步骤Ⅰ:打开K1、K3、K5,关闭K2、K4,通入一段时间N2,关闭K1﹔
步骤Ⅱ:打开K2,加入足量浓硝酸,同时打开pH传感器和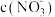 传感器,记录数据如下:[pH越小表示c(H+)越大]﹔
传感器,记录数据如下:[pH越小表示c(H+)越大]﹔
回答下列问题:
(1)仪器a的名称为_______ 。
(2)“步骤Ⅰ”中“通入一段时间N2”的目的是_______ 。
(3)“步骤Ⅱ”中“打开K2,加入足量浓硝酸”时,可观察到:圆底烧瓶中反应剧烈,铜片逐渐溶解,溶液变为蓝绿色,同时烧瓶上方有红棕色气体产生,化学方程式为_______ ;片刻后,三颈烧瓶内的导管口有气泡冒出。
(4)“步骤Ⅲ”中“用注射器将少量空气注入三颈烧瓶”的目的是检验_______ (填化学式)。
(5)根据“步骤Ⅱ”的数据采集和“步骤Ⅲ”的实验现象,得到NO2与水反应的离子方程式为_______ 。
(6)有同学认为该实验不严谨,传感器所记录的数据结果也可能是因为_______ 造成的。
步骤Ⅰ:打开K1、K3、K5,关闭K2、K4,通入一段时间N2,关闭K1﹔
步骤Ⅱ:打开K2,加入足量浓硝酸,同时打开pH传感器和
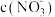 传感器,记录数据如下:[pH越小表示c(H+)越大]﹔
传感器,记录数据如下:[pH越小表示c(H+)越大]﹔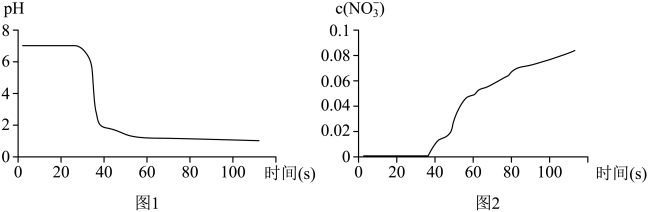
回答下列问题:
(1)仪器a的名称为
(2)“步骤Ⅰ”中“通入一段时间N2”的目的是
(3)“步骤Ⅱ”中“打开K2,加入足量浓硝酸”时,可观察到:圆底烧瓶中反应剧烈,铜片逐渐溶解,溶液变为蓝绿色,同时烧瓶上方有红棕色气体产生,化学方程式为
(4)“步骤Ⅲ”中“用注射器将少量空气注入三颈烧瓶”的目的是检验
(5)根据“步骤Ⅱ”的数据采集和“步骤Ⅲ”的实验现象,得到NO2与水反应的离子方程式为
(6)有同学认为该实验不严谨,传感器所记录的数据结果也可能是因为
更新时间:2024-04-25 20:51:38
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】原子序数由小到大排列的四种短周期元素X、Y、Z、W,四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族。
(1)X元素符号是______________________ ;
(2)Z、W形成的气态氢化物的稳定性_______ >_______ (写化学式)。
(3)由X、Y、Z、W四种元素中的三种组成的一种强酸,该强酸的稀溶液能与铜反应,离子方程式为_________________________________ 。
(4)由X、Y、Z、W和Fe五种元素组成的相对分子质量为392的化合物B,lmolB中含有6mol结晶水。对化合物B进行如下实验:
a.取B的溶液加入过量浓NaOH溶液并加热,产生白色沉淀和无色刺激性气味气体;过一段时间白色沉淀变为灰绿色,最终变为红褐色。
b.另取B的溶液,加入过量BaCl2溶液产生白色沉淀,加盐酸沉淀不溶解。
①由实验a、b推知B溶液中含有的离子为__________________ ;
②B的化学式为_________________ 。
(1)X元素符号是
(2)Z、W形成的气态氢化物的稳定性
(3)由X、Y、Z、W四种元素中的三种组成的一种强酸,该强酸的稀溶液能与铜反应,离子方程式为
(4)由X、Y、Z、W和Fe五种元素组成的相对分子质量为392的化合物B,lmolB中含有6mol结晶水。对化合物B进行如下实验:
a.取B的溶液加入过量浓NaOH溶液并加热,产生白色沉淀和无色刺激性气味气体;过一段时间白色沉淀变为灰绿色,最终变为红褐色。
b.另取B的溶液,加入过量BaCl2溶液产生白色沉淀,加盐酸沉淀不溶解。
①由实验a、b推知B溶液中含有的离子为
②B的化学式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某学习小组探究浓、稀硝酸氧化性的相对强弱,按下图装置进行实验(夹持仪器已略去)。实验表明浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO。由此得出的结论是浓硝酸的氧化性强于稀硝酸。

可选药品:浓硝酸、稀硝酸、蒸馏水、浓硫酸、氢氧化钠溶液及二氧化碳。
已知:氢氧化钠溶液不与NO反应,能与NO2反应。2NO2+2NaOH=NaNO3+NaNO2+H2O
(1)实验应避免有害气体排放到空气中。装置③④⑥中盛放的药品依次是____ 、____ 、_______ 。
(2)滴加浓硝酸之前的一系列操作依次是检验装置的气密性,加入药品,打开弹簧夹后______ 。
(3)装置①中发生反应的化学方程式是___________ 。
(5)该小组得出的结论所依据的实验现象是_________ 。

可选药品:浓硝酸、稀硝酸、蒸馏水、浓硫酸、氢氧化钠溶液及二氧化碳。
已知:氢氧化钠溶液不与NO反应,能与NO2反应。2NO2+2NaOH=NaNO3+NaNO2+H2O
(1)实验应避免有害气体排放到空气中。装置③④⑥中盛放的药品依次是
(2)滴加浓硝酸之前的一系列操作依次是检验装置的气密性,加入药品,打开弹簧夹后
(3)装置①中发生反应的化学方程式是
(5)该小组得出的结论所依据的实验现象是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】某些化学反应可用下式表示A+B→C+D+H2O。请回答下列问题(反应可以是固体之间的反应,也可以是在水溶液中进行的反应)。
(1)若A是非金属气态单质,反应后所得溶液常用于消毒、杀菌。则A为________ (填化学式,下同)。反应的化学方程式为________________ 。
(2)若A为非金属固态单质,C、D均为气体且都能使澄清石灰水变浑浊。则A为________ 。反应的化学方程式为________________________________ 。
(3)若A为紫红色金属,D为有色气体。则A为______ 。反应的离子方程式为________________________________________ 。
(4)若A为烧碱溶液,C是相对分子质量为100的白色沉淀,D为正盐。则C为________ 。反应的离子方程式为___________________ 。
(5)若A、B为固体,C的水溶液能使酚酞溶液变为红色。实验室常用此反应制备C气体。则C为________ 。反应的化学方程式为_____________________ 。
(1)若A是非金属气态单质,反应后所得溶液常用于消毒、杀菌。则A为
(2)若A为非金属固态单质,C、D均为气体且都能使澄清石灰水变浑浊。则A为
(3)若A为紫红色金属,D为有色气体。则A为
(4)若A为烧碱溶液,C是相对分子质量为100的白色沉淀,D为正盐。则C为
(5)若A、B为固体,C的水溶液能使酚酞溶液变为红色。实验室常用此反应制备C气体。则C为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】Na2O2可用作漂白剂和呼吸面具中的供氧剂。
(1)某学习小组发现:在盛有Na2O2的试管中加入足量水,固体完全溶解,并立即产生大量气泡,当气泡消失后,向其中滴入1~2滴酚酞溶液,溶液变红;将试管轻轻振荡,红色很快褪去;此时再向试管中加入少量MnO2粉末,又有气泡产生。请写出加入MnO2反应的化学方程式为__________________________ 。
(2)Na2O2有强氧化性,H2具有还原性,有同学猜想Na2O2与H2能反应.为了验证此猜想,该小组同学进行如下实验,实验步骤和现象如下。
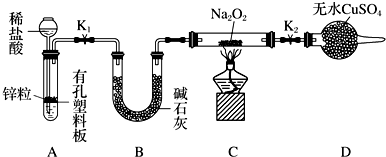
步骤1:按图组装仪器(图中夹持仪器省略),检查气密性,装入药品。
步骤2:打开K1、K2,产生的氢气流经装有Na2O2的硬质玻璃管,一段时间后,没有任何现象。
步骤3:检验H2的纯度后,开始加热,观察到硬质玻璃管内Na2O2开始熔化,淡黄色的粉末变成了白色固体,干燥管内硫酸铜未变蓝色。
步骤4:反应后撤去酒精灯,待硬质玻璃管冷却后关闭K1。
①添加稀盐酸的仪器名称是_______________ 。
②必须检验氢气纯度的原因是___________________ 。
③设置装置D的目的是_________________________________________ 。
④你得到的结论是___________________________________________________ (若能反应请用化学方程式表示)。
(1)某学习小组发现:在盛有Na2O2的试管中加入足量水,固体完全溶解,并立即产生大量气泡,当气泡消失后,向其中滴入1~2滴酚酞溶液,溶液变红;将试管轻轻振荡,红色很快褪去;此时再向试管中加入少量MnO2粉末,又有气泡产生。请写出加入MnO2反应的化学方程式为
(2)Na2O2有强氧化性,H2具有还原性,有同学猜想Na2O2与H2能反应.为了验证此猜想,该小组同学进行如下实验,实验步骤和现象如下。

步骤1:按图组装仪器(图中夹持仪器省略),检查气密性,装入药品。
步骤2:打开K1、K2,产生的氢气流经装有Na2O2的硬质玻璃管,一段时间后,没有任何现象。
步骤3:检验H2的纯度后,开始加热,观察到硬质玻璃管内Na2O2开始熔化,淡黄色的粉末变成了白色固体,干燥管内硫酸铜未变蓝色。
步骤4:反应后撤去酒精灯,待硬质玻璃管冷却后关闭K1。
①添加稀盐酸的仪器名称是
②必须检验氢气纯度的原因是
③设置装置D的目的是
④你得到的结论是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】(1)用铜与浓硫酸反应制取硫酸铜,实验装置如图所示.
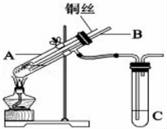
A中装置体现了浓硫酸的哪些性质?______ ;
(2)为符合绿色化学的要求,某同学进行如下设计:将铜粉在______ (填仪器名称)中反复灼烧,使铜与空气充分反应生成氧化铜,再将氧化铜与稀硫酸反应,反应后溶液经过______ 、______ 、过滤、洗涤、干燥,即可得到产品CuSO45H2O晶体,干燥时需要控制温度小于100℃,若温度过高,则会导致______ .
(3)探究小组用滴定法测定某胆矾晶体中CuSO4的含量.取ag样品配成100mL溶液,每次取20.00mL,消除干扰离子后,用c molL﹣1的EDTA(H2Y2﹣)标准溶液滴定至终点,平均消耗EDTA溶液6mL.滴定反应如下:Cu2++H2Y2﹣=CuY2﹣+2H+.
①写出计算CuSO4质量分数的计算式ω=______ ;
②下列操作会导致CuSO4含量的测定结果偏低的是______ .
a.用样品溶液润洗锥形瓶
b.滴定终点时俯视读数
c.滴定终点时滴定管尖嘴中有气泡

A中装置体现了浓硫酸的哪些性质?
(2)为符合绿色化学的要求,某同学进行如下设计:将铜粉在
(3)探究小组用滴定法测定某胆矾晶体中CuSO4的含量.取ag样品配成100mL溶液,每次取20.00mL,消除干扰离子后,用c molL﹣1的EDTA(H2Y2﹣)标准溶液滴定至终点,平均消耗EDTA溶液6mL.滴定反应如下:Cu2++H2Y2﹣=CuY2﹣+2H+.
①写出计算CuSO4质量分数的计算式ω=
②下列操作会导致CuSO4含量的测定结果偏低的是
a.用样品溶液润洗锥形瓶
b.滴定终点时俯视读数
c.滴定终点时滴定管尖嘴中有气泡
您最近一年使用:0次
【推荐3】某课题组同学查阅文献知,3(NH4)2SO4(s)  4NH3↑ +3SO2↑+N2↑+6H2O。他们拟选择下列装置检验硫酸铵分解的产物(各装置中药品足量):
4NH3↑ +3SO2↑+N2↑+6H2O。他们拟选择下列装置检验硫酸铵分解的产物(各装置中药品足量):

回答下列问题:
(1)上述方程式涉及的物质中,属于电解质的是:_______ 。(写化学式)
(2)常温下,产物混合气体的平均相对分子质量为:_______ 。
(3)仪器A的名称是_______ 。
(4)甲组同学选择上述装置证明产物中是否有NH3。气体从左至右,装置的连接顺序为C→_______ →_______ 证明有NH3的实验现象是;_______ 。
(5)乙组同学设计方案:C→G→B→D→E证明产物中有H2O和SO2。
①能证明有水生成的实验现象是_______ ,B装置的作用是_______ 。
②实验中,观察到D装置产生白色沉淀。实验完毕后,过滤D装置中混合物得白色沉淀。欲验证白色沉淀是BaSO4还是BaSO3,请你设计简单的实验方案:_______ 。
③D装置中发生的反应与硝酸钡的量有关,若硝酸钡足量,则D中反应的离子方程式为_______ 。
 4NH3↑ +3SO2↑+N2↑+6H2O。他们拟选择下列装置检验硫酸铵分解的产物(各装置中药品足量):
4NH3↑ +3SO2↑+N2↑+6H2O。他们拟选择下列装置检验硫酸铵分解的产物(各装置中药品足量):
回答下列问题:
(1)上述方程式涉及的物质中,属于电解质的是:
(2)常温下,产物混合气体的平均相对分子质量为:
(3)仪器A的名称是
(4)甲组同学选择上述装置证明产物中是否有NH3。气体从左至右,装置的连接顺序为C→
(5)乙组同学设计方案:C→G→B→D→E证明产物中有H2O和SO2。
①能证明有水生成的实验现象是
②实验中,观察到D装置产生白色沉淀。实验完毕后,过滤D装置中混合物得白色沉淀。欲验证白色沉淀是BaSO4还是BaSO3,请你设计简单的实验方案:
③D装置中发生的反应与硝酸钡的量有关,若硝酸钡足量,则D中反应的离子方程式为
您最近一年使用:0次



