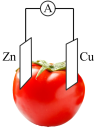
任何化学反应都伴随着能量的变化,化学能可转化为热能、电能等。回答下列有关问题:
(1)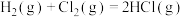 的反应过程如图所示:
的反应过程如图所示:___________ (填“放热”或“吸热”)反应,生成2molHCl(g)吸收或放出的热量为___________ 。
(2)下列变化中属于吸热反应的是___________ (填标号)。
①液态水汽化 ②生石灰与水反应
③ ④
④ 与固体
与固体 混合
混合
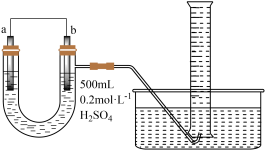
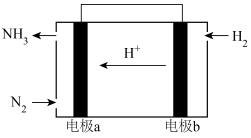
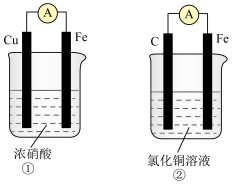
(3)用如图装置推算铜锌原电池工作时产生的电流量。供选择的电极材料有纯铜片和纯锌片。则 a 电极的电极反应式为___________ ,当量筒中收集到 336mL(标准状况下)气体时,通过导线的电子的物质的量为___________ 。___________ 极(填“正”或“负”)。___________ (填“①”或“②”)该装置中的正极的电极反应式为___________ ;电子从___________ (填电极材料)流向___________ (填电极材料)
(1)
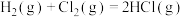 的反应过程如图所示:
的反应过程如图所示: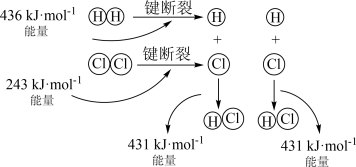
(2)下列变化中属于吸热反应的是
①液态水汽化 ②生石灰与水反应
③
 ④
④ 与固体
与固体 混合
混合(3)用如图装置推算铜锌原电池工作时产生的电流量。供选择的电极材料有纯铜片和纯锌片。则 a 电极的电极反应式为
更新时间:2024-04-30 13:14:21
|
相似题推荐
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐1】二甲醚(CH3OCH3)是一种可再生绿色新能源,被誉为“21世纪的清洁燃料”。
(1)写出二甲醚一种同分异构体的结构简式:____________ 。
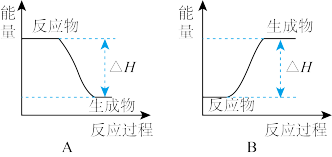
(2)CH3OCH3(g)+3O2(g)=2CO2(g)+3H2O(l)是____________ 反应(填“吸热”或“放热”),该反应过程的能量变化示意图可用下图中的____________ 表示(填“A”或“B”)。
(3)工业上可用水煤气合成二甲醚:2CO(g)+4H2(g)⇌CH3OCH3(g)+H2O(g)
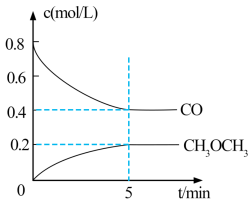
①测得CO和CH3OCH3(g)的浓度随时间变化如图所示,则反应开始至平衡时CO的平均反应速率v(CO)=________ mol/(L·min)。
②该反应在恒容密闭容器中进行,下列叙述中能表示该反应达到平衡状态的是____________ 。
A.单位时间内生成CO和H2的物质的量之比为1﹕2
B.CH3OCH3的浓度不再变化
C.容器内压强不再变化
D.CH3OCH3与H2O的物质的量相等
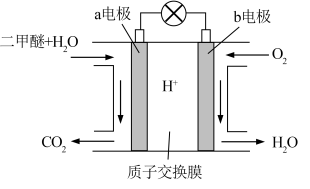
(4)二甲醚燃料电池工作原理如图所示,则a电极的电极名称为____________ 极(填“正”或“负”)。
.
(1)写出二甲醚一种同分异构体的结构简式:
(2)CH3OCH3(g)+3O2(g)=2CO2(g)+3H2O(l)是

(3)工业上可用水煤气合成二甲醚:2CO(g)+4H2(g)⇌CH3OCH3(g)+H2O(g)
①测得CO和CH3OCH3(g)的浓度随时间变化如图所示,则反应开始至平衡时CO的平均反应速率v(CO)=

②该反应在恒容密闭容器中进行,下列叙述中能表示该反应达到平衡状态的是
A.单位时间内生成CO和H2的物质的量之比为1﹕2
B.CH3OCH3的浓度不再变化
C.容器内压强不再变化
D.CH3OCH3与H2O的物质的量相等
(4)二甲醚燃料电池工作原理如图所示,则a电极的电极名称为
.

您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐2】I.扎西和央拉两位同学做如下实验,以检验反应中的能量变化。
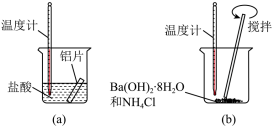
(1)实验中发现反应后(a)中温度升高,由此可以判断(a)中反应是______ 热反应;(b)中温度降低,由此可以判断(b)中反应是_______ 热反应。
(2)根据能量守恒定律,(b)中反应物的总能量应该______ 其生成物的总能量。
II.
(3)下图表示一定条件下,A、B、C三种气体物质的量浓度随时间变化的情形,回答下列问题:
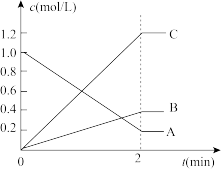
①该反应的反应物是___________ 。
②在0~2min,该反应用A表示的平均反应速率为_______ 。
③该反应的化学方程式为___________ 。

(1)实验中发现反应后(a)中温度升高,由此可以判断(a)中反应是
(2)根据能量守恒定律,(b)中反应物的总能量应该
II.
(3)下图表示一定条件下,A、B、C三种气体物质的量浓度随时间变化的情形,回答下列问题:

①该反应的反应物是
②在0~2min,该反应用A表示的平均反应速率为
③该反应的化学方程式为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
【推荐3】I、为了探究化学反应的热效应,某兴趣小组进行了如下实验:
(1)将纯固体物质X分别装入有水的锥形瓶里(发生化学反应),立即塞紧带U形管的塞子,发现U形管内红墨水的液面高度如图所示。

若如图2所示,发生的反应(假设没有气体生成)是___________ (填“放热”或“吸热”)反应,以下选项中与其能量变化相同的是___________ (填字母)。
A.CO的燃烧B.CaCO3的分解反应C.Al和Fe2O3的反应
(2)下列关于能源说法不正确的是___________ (填序号)
A.煤石油天然气是现代社会主要能源,由此获取热能的主要途径是通过物质的燃烧
B.化石燃料燃烧排放的粉尘、SO2、NOx、CO2等是大气污染物的主要来源
C.新能源有太阳能、风能、地热能、海洋能和氢能等
D.在能量利用阶段,可采取合理的措施促进能源循环利用,提高能源利用率
(3)如图所示,把试管放入盛有25℃饱和澄清石灰水的烧杯中,试管中开始放几小块铝片,再滴入5mL NaOH溶液。试回答下列问题:
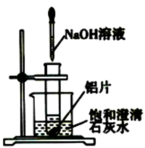
实验中观察到的现象是:铝片逐渐溶解、有大量气泡产生、__________ ,产生上述现象的原因是________ 。
II、化学电源的发明是化学对人类的一项重大贡献。
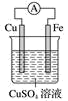
(1)将锌片、铜片按照如图所示装置连接,铜片做___________ 极(填“正”或“负”),外电路电子的流向为___________ (填“Cu→Zn”或“Zn→Cu”)。

(2)若将装置中的稀H2SO4用CuSO4溶液替代,则相应原电池的总反应的化学方程式为___________ 。
(3)下列化学反应通过原电池装置,可实现化学能直接转化为电能的是___________ (填序号)。
①NaOH+HCl=NaCl+H2O
②CH4+2O2 CO2+2H2O
CO2+2H2O
③Fe+Cu2+=Cu+Fe2+
(1)将纯固体物质X分别装入有水的锥形瓶里(发生化学反应),立即塞紧带U形管的塞子,发现U形管内红墨水的液面高度如图所示。

若如图2所示,发生的反应(假设没有气体生成)是
A.CO的燃烧B.CaCO3的分解反应C.Al和Fe2O3的反应
(2)下列关于能源说法不正确的是
A.煤石油天然气是现代社会主要能源,由此获取热能的主要途径是通过物质的燃烧
B.化石燃料燃烧排放的粉尘、SO2、NOx、CO2等是大气污染物的主要来源
C.新能源有太阳能、风能、地热能、海洋能和氢能等
D.在能量利用阶段,可采取合理的措施促进能源循环利用,提高能源利用率
(3)如图所示,把试管放入盛有25℃饱和澄清石灰水的烧杯中,试管中开始放几小块铝片,再滴入5mL NaOH溶液。试回答下列问题:

实验中观察到的现象是:铝片逐渐溶解、有大量气泡产生、
II、化学电源的发明是化学对人类的一项重大贡献。
(1)将锌片、铜片按照如图所示装置连接,铜片做

(2)若将装置中的稀H2SO4用CuSO4溶液替代,则相应原电池的总反应的化学方程式为
(3)下列化学反应通过原电池装置,可实现化学能直接转化为电能的是
①NaOH+HCl=NaCl+H2O
②CH4+2O2
 CO2+2H2O
CO2+2H2O③Fe+Cu2+=Cu+Fe2+
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
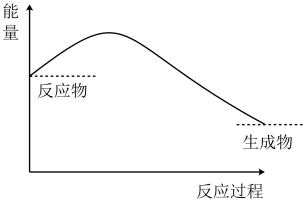
【推荐1】Ⅰ.锌片与稀硫酸反应的能量变化特征如图所示,回答下列问题。___________ 反应(填“吸热”或“放热”)。
(2)锌片和铜片用导线相连后,若将锌片和铜片浸泡在稀硫酸溶液中,可观察到铜片处的现象___________ 。
Ⅱ.以相同大小铜片和锌片为电极研究水果电池,得到的实验数据如下表所示:
(3)该实验目的是研究水果种类和___________ 对水果电池电流大小的影响。
(4)该实验装置中,正极的材料是___________ ,负极的电极反应式是___________ 。
(5)当有 参与反应,转移的电子数目为
参与反应,转移的电子数目为___________ 。
Ⅲ.某温度下,体积为 恒容密闭容器中,X、Y两种气体参与反应,物质的量随时间的变化曲线如图所示。请回答下列问题:
恒容密闭容器中,X、Y两种气体参与反应,物质的量随时间的变化曲线如图所示。请回答下列问题:___________ 。
(7)在 内,用Y表示的反应速率为
内,用Y表示的反应速率为___________ 。
(2)锌片和铜片用导线相连后,若将锌片和铜片浸泡在稀硫酸溶液中,可观察到铜片处的现象
Ⅱ.以相同大小铜片和锌片为电极研究水果电池,得到的实验数据如下表所示:
| 实验编号 | 水果种类 | 电极间距离/cm | 电流 |
|
| 1 | 番茄 | 1 | 98.7 | |
| 2 | 番茄 | 2 | 72.5 | |
| 3 | 苹果 | 2 | 27.2 |
(3)该实验目的是研究水果种类和
(4)该实验装置中,正极的材料是
(5)当有
 参与反应,转移的电子数目为
参与反应,转移的电子数目为Ⅲ.某温度下,体积为
 恒容密闭容器中,X、Y两种气体参与反应,物质的量随时间的变化曲线如图所示。请回答下列问题:
恒容密闭容器中,X、Y两种气体参与反应,物质的量随时间的变化曲线如图所示。请回答下列问题: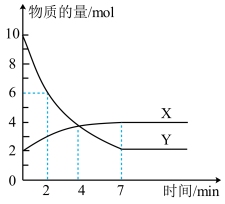
(7)在
 内,用Y表示的反应速率为
内,用Y表示的反应速率为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】某化学研究性学习小组针对原电池形成条件,设计了实验方案,进行如下探究。
(1)请填写有关实验现象并得出相关结论。
①通过实验2和3,可得出原电池的形成条件是______________________________ 。
②通过实验1和3,可得出原电池的形成条件是______________________________ 。
③若将3装置中硫酸换成乙醇,电流计指针将不发生偏转,从而可得出原电池形成条件是___________________ 。
(2)分别写出实验3中Zn棒和Cu棒上发生的电极反应式:
Zn棒:______________________________ 。
Cu棒:______________________________ 。
(3)实验3的电流是从________ 棒流出(填“Zn”或“Cu”),反应过程中若有0.4mol电子发生了转移,则Zn电极质量减轻___________ g。
(1)请填写有关实验现象并得出相关结论。
| 编号 | 实验装置 | 实验现象 |
| 1 | 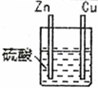 | 锌棒逐渐溶解,表面有气体生成;铜棒表面无现象 |
| 2 | 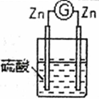 | 两锌棒逐渐溶解,表面均有气体生成;电流计指针不偏转 |
| 3 | 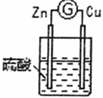 | 铜棒表面的现象是 |
①通过实验2和3,可得出原电池的形成条件是
②通过实验1和3,可得出原电池的形成条件是
③若将3装置中硫酸换成乙醇,电流计指针将不发生偏转,从而可得出原电池形成条件是
(2)分别写出实验3中Zn棒和Cu棒上发生的电极反应式:
Zn棒:
Cu棒:
(3)实验3的电流是从
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
【推荐3】某原电池装置如图所示,装置中盐桥的作用是使整个装置形成一个闭合回路,电解质溶液足量,闭合开关,观察到电流计指针发生偏转,回答下列问题。
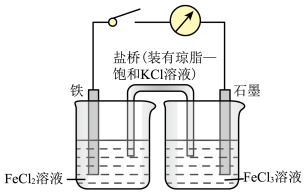
(1)该原电池工作过程中,电池的负极上的电极反应式为___________ ,石墨电极上发生了___________ (填“氧化”或“还原”)反应。
(2)该原电池工作时,下列说法正确的是___________(填标号)。
(3)当铁电极减少 时,外电路中转移的电子数目为
时,外电路中转移的电子数目为___________  ,右侧烧杯中
,右侧烧杯中 的物质的量改变了
的物质的量改变了___________  。
。
(4)原电池工作时能量转化形式为_______ ,根据原电池形成条件,下列反应理论上可以设计成原电池的是_______ (填标号)。
A. 与
与 的反应 B.
的反应 B. 和
和 的反应
的反应
C. 和
和 的反应 D.
的反应 D. 和
和 的反应
的反应
(5)以 为原理设计燃枓电池,其利用率高,装置如图所示。
为原理设计燃枓电池,其利用率高,装置如图所示。
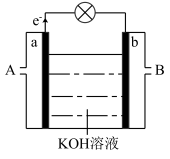
①A处加入的是___________ ,a处的电极反应式是_______ 。
②当消耗标准状况下3.36L 时,导线上转移的电子的物质的量是
时,导线上转移的电子的物质的量是___________ mol。

(1)该原电池工作过程中,电池的负极上的电极反应式为
(2)该原电池工作时,下列说法正确的是___________(填标号)。
A.电子移动的方向:石墨 铁 铁 |
B.盐桥中的 会向右侧烧杯移动 会向右侧烧杯移动 |
C. 溶液的颜色会逐渐变浅 溶液的颜色会逐渐变浅 |
D.将 盐桥换成 盐桥换成 盐桥,该装置不能长时间正常工作 盐桥,该装置不能长时间正常工作 |
 时,外电路中转移的电子数目为
时,外电路中转移的电子数目为 ,右侧烧杯中
,右侧烧杯中 的物质的量改变了
的物质的量改变了 。
。(4)原电池工作时能量转化形式为
A.
 与
与 的反应 B.
的反应 B. 和
和 的反应
的反应C.
 和
和 的反应 D.
的反应 D. 和
和 的反应
的反应(5)以
 为原理设计燃枓电池,其利用率高,装置如图所示。
为原理设计燃枓电池,其利用率高,装置如图所示。
①A处加入的是
②当消耗标准状况下3.36L
 时,导线上转移的电子的物质的量是
时,导线上转移的电子的物质的量是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】Ⅰ: 元素的金属活动性递变规律是元素周期表学习的重要内容之一。某校研究性学习小组查阅课外资料,看到第IVA族的三种金属锗、锡、铅的性质:“锗、锡在空气中不反应,铅在空气中表面生成一层氧化铅,请解释发生上述变化的原因是___________________________________________________________ 。
Ⅱ: 另一研究性学习小组欲通过实验探究Zn、Fe、Cu的金属活动性顺序,根据不同的实验条件设计了如下的几种实验方案:
(1)该小组同学根据提供的Zn片、Fe片和稀硫酸,设计成了一个原电池比较锌与铁的活动性顺序,请在下侧方框内画出原电池装置图。并写出正极的反应现象及电极反应式。
现象_______________________________ ;电极反应式___________________________ ;装置图:________________________

(2)现只有Fe片、CuO和稀硫酸这几种药品,请你帮忙设计方案比较铁与铜的活动性顺序。你的设计方法是___________________________________________________________________________
Ⅱ: 另一研究性学习小组欲通过实验探究Zn、Fe、Cu的金属活动性顺序,根据不同的实验条件设计了如下的几种实验方案:
(1)该小组同学根据提供的Zn片、Fe片和稀硫酸,设计成了一个原电池比较锌与铁的活动性顺序,请在下侧方框内画出原电池装置图。并写出正极的反应现象及电极反应式。
现象

(2)现只有Fe片、CuO和稀硫酸这几种药品,请你帮忙设计方案比较铁与铜的活动性顺序。你的设计方法是
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
【推荐2】放热反应在生产、生活中用途广泛。回答下列问题:
(1)前期的火箭曾用液态肼( )与双氧水反应来提供能量。已知0.4mol
)与双氧水反应来提供能量。已知0.4mol (l)与足量的双氧水反应,生成氮气和水蒸气,放出256.7kJ的热量。
(l)与足量的双氧水反应,生成氮气和水蒸气,放出256.7kJ的热量。
①此反应的化学方程式为_____ 。
②16g液态肼与足量的双氧水发生上述反应,放出_____ kJ热量。
(2)甲烷可以消除氮氧化物污染: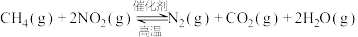 。温度为800℃的条件下,向恒容密闭的容器中通入
。温度为800℃的条件下,向恒容密闭的容器中通入 (g)和
(g)和 (g),使
(g),使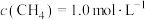 ,
,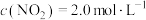 ,在不同催化剂作用下进行反应,测得
,在不同催化剂作用下进行反应,测得 随时间的变化情况如下表:
随时间的变化情况如下表:
实验1中,在10~20min内,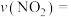
_____ ,40min时v(正)_____ (填“大于”“小于”或“等于”)v(逆)。
(3)催化效率:实验1_____ (填“>”“<”或“=”)实验2.
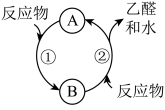
(4)乙醇( )应用于燃料电池,该电池采用可传导
)应用于燃料电池,该电池采用可传导 的固体氧化物为电解质,其工作原理如图所示。a极为原电池的
的固体氧化物为电解质,其工作原理如图所示。a极为原电池的_____ (填“正”或“负”)极;b极电极反应式为_____ 。_____ (填“催化剂”或“中间产物”)。
(1)前期的火箭曾用液态肼(
 )与双氧水反应来提供能量。已知0.4mol
)与双氧水反应来提供能量。已知0.4mol (l)与足量的双氧水反应,生成氮气和水蒸气,放出256.7kJ的热量。
(l)与足量的双氧水反应,生成氮气和水蒸气,放出256.7kJ的热量。①此反应的化学方程式为
②16g液态肼与足量的双氧水发生上述反应,放出
(2)甲烷可以消除氮氧化物污染:
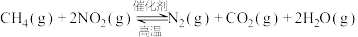 。温度为800℃的条件下,向恒容密闭的容器中通入
。温度为800℃的条件下,向恒容密闭的容器中通入 (g)和
(g)和 (g),使
(g),使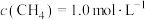 ,
,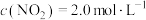 ,在不同催化剂作用下进行反应,测得
,在不同催化剂作用下进行反应,测得 随时间的变化情况如下表:
随时间的变化情况如下表:| 实验序号 |
| 10 | 20 | 30 | 40 | 50 |
| 1 | 800 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 |
| 2 | 800 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 |
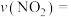
(3)催化效率:实验1
(4)乙醇(
 )应用于燃料电池,该电池采用可传导
)应用于燃料电池,该电池采用可传导 的固体氧化物为电解质,其工作原理如图所示。a极为原电池的
的固体氧化物为电解质,其工作原理如图所示。a极为原电池的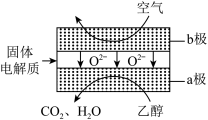
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
【推荐1】(1)根据下列信息判断氢气燃烧生成水时的热量变化:
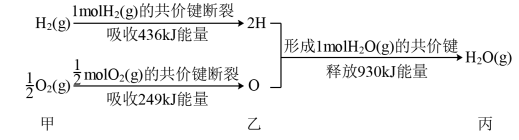
①H2(g)与O2(g)反应生成1molH2O(g)时放出的热量为_________ kJ;
②图中甲、乙、丙中物质所具有的总能量由大到小顺序为:_____________ ;
(2)铅蓄电池是最常见的二次电池,放电时的化学方程式为:Pb(s)+PbO2(s)+2H2SO4(aq)=2PbSO4(s)+2H2O。负极反应式为________ ,一段时间后,负极增重48克,转移电子_______ mol。

①H2(g)与O2(g)反应生成1molH2O(g)时放出的热量为
②图中甲、乙、丙中物质所具有的总能量由大到小顺序为:
(2)铅蓄电池是最常见的二次电池,放电时的化学方程式为:Pb(s)+PbO2(s)+2H2SO4(aq)=2PbSO4(s)+2H2O。负极反应式为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐2】电池种类丰富,发展飞速,应用广泛,为我们的生产和生活带来了非常大的便利。
(1)某兴趣小组设计了如图所示的原电池装置,该电池的负极为___________ (填“铂”或“铜”),正极的电极反应式为___________ ,盐桥中装有含氯化钾的琼脂,其中 移向
移向___________ 溶液(填“ ”或“
”或“ ”)。
”)。

(2)装置中所用到的硫酸铜是一种常用试剂,该小组尝试用以下两种方案制备硫酸铜。
方案一:直接用铜和浓硫酸制备硫酸铜;
方案二:将铜和银同时浸泡在稀硫酸中,不断通入氧气,一段时间后可以获得硫酸铜;
i.写出方案一的化学方程式___________ ;与方案二相比,该方案的不足之处是(至少写出2种)___________ 、___________ 。
ii.写出方案二的电极反应式:正极:___________ 、负极:_____________ 。
(3)甲醇是重要的化工原料,又可作为燃料使用,用 和
和 组合形成的质子交换膜燃料电池的结构示意图如下:
组合形成的质子交换膜燃料电池的结构示意图如下:

电池总反应为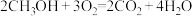 ,则C电极是
,则C电极是___________ (填“正极”或“负极”),C电极的电极反应式为___________ ;若线路中转移3mol电子,则上述 燃料电池,消耗的
燃料电池,消耗的 的质量为
的质量为___________ g
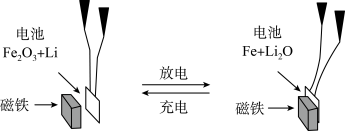
(4)某课题组以纳米 作为电极材料制备锂离子电池(另一极为金属锂和石墨的复合材料),通过在室温条件下对锂离子电池进行循环充放电,成功地实现了对磁性的可逆调控(如图)。下列说法正确的是___________。
作为电极材料制备锂离子电池(另一极为金属锂和石墨的复合材料),通过在室温条件下对锂离子电池进行循环充放电,成功地实现了对磁性的可逆调控(如图)。下列说法正确的是___________。
(1)某兴趣小组设计了如图所示的原电池装置,该电池的负极为
 移向
移向 ”或“
”或“ ”)。
”)。
(2)装置中所用到的硫酸铜是一种常用试剂,该小组尝试用以下两种方案制备硫酸铜。
方案一:直接用铜和浓硫酸制备硫酸铜;
方案二:将铜和银同时浸泡在稀硫酸中,不断通入氧气,一段时间后可以获得硫酸铜;
i.写出方案一的化学方程式
ii.写出方案二的电极反应式:正极:
(3)甲醇是重要的化工原料,又可作为燃料使用,用
 和
和 组合形成的质子交换膜燃料电池的结构示意图如下:
组合形成的质子交换膜燃料电池的结构示意图如下:
电池总反应为
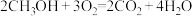 ,则C电极是
,则C电极是 燃料电池,消耗的
燃料电池,消耗的 的质量为
的质量为(4)某课题组以纳米
 作为电极材料制备锂离子电池(另一极为金属锂和石墨的复合材料),通过在室温条件下对锂离子电池进行循环充放电,成功地实现了对磁性的可逆调控(如图)。下列说法正确的是___________。
作为电极材料制备锂离子电池(另一极为金属锂和石墨的复合材料),通过在室温条件下对锂离子电池进行循环充放电,成功地实现了对磁性的可逆调控(如图)。下列说法正确的是___________。
A.放电时,正极的电极反应式为 |
| B.该电池可以用水溶液做电解质溶液 |
C.放电时,Fe作电池的负极, 作电池的正极 作电池的正极 |
| D.充电完成后,电池被磁铁吸引 |
您最近一年使用:0次