硫酸工业生产的核心阶段是转化,转化率越高,则硫的利用率越高,对环境影响也越小。
1.转化阶段发生的反应: (放热反应),上述反应中,反应物的总能量
(放热反应),上述反应中,反应物的总能量___________ (选填“大于”或“小于”)生成物的总能量。
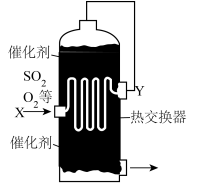
2.为合理利用反应中产生的热量,热交换器在硫酸工业中与下列___________设备合为一体。
3.如图中,Y处的气体是___________。
1.转化阶段发生的反应:
 (放热反应),上述反应中,反应物的总能量
(放热反应),上述反应中,反应物的总能量2.为合理利用反应中产生的热量,热交换器在硫酸工业中与下列___________设备合为一体。
| A.沸腾炉 | B.净化器 | C.接触室 | D.吸收塔 |
A.低温的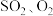 | B.低温的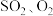 和 和 |
C.高温的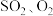 | D.高温的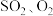 和 和 |
更新时间:2024-05-04 16:50:37
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】工业合成氨是利用氮气和氢气在一定条件下反应生成的。氨是重要的工业原料。请回答下列问题:
(1)氮元素在周期表中的位置是第_______ 周期第_______ 族;氮原子结构示意图为_______ 。
(2)写出氨分子的电子式______ ;指出分子中化学键类型是_____ 。
(3)写成合成氨的化学方程式:________________________ ;该反应是放热反应,则相同条件下“1molN2和3molH2”的能量与“2molNH3”的能量较高的是________________ 。
(1)氮元素在周期表中的位置是第
(2)写出氨分子的电子式
(3)写成合成氨的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)已知1mol石墨转化为1mol金刚石要吸收能量,则1mol石墨的能量比1mol金刚石的能量___ (填“高”或“低”),石墨比金刚石___ (填“稳定”或“不稳定”)。
(2)Ba(OH)2•8H2O和NH4Cl反应的化学方程式是___ ,该反应是 ___ (填“吸热”或“放热”)反应,反应过程能量变化的图象符合___ (填“图1”或“图2”)。
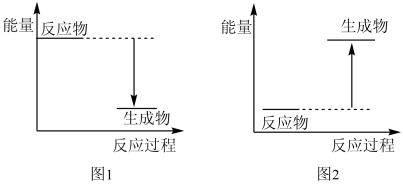
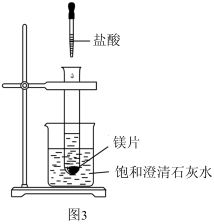
(3)如图3所示,把试管放入盛有饱和澄清石灰水(温度为25℃)的烧杯中,先在试管中放入几小块镁片,再用滴管滴入5mL盐酸。可以观察到烧杯中的石灰水逐渐由澄清变浑浊,出现这种现象的原因是___ 。
(2)Ba(OH)2•8H2O和NH4Cl反应的化学方程式是

(3)如图3所示,把试管放入盛有饱和澄清石灰水(温度为25℃)的烧杯中,先在试管中放入几小块镁片,再用滴管滴入5mL盐酸。可以观察到烧杯中的石灰水逐渐由澄清变浑浊,出现这种现象的原因是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】硫酸工业在国民经济中占有重要地位。
(1)在18世纪40年代以前,生产硫酸最古老的方法是:以绿矾( )为原料在蒸馏釜中煅烧(隔离空气),除有水蒸气生成外,还有两种气体生成,然后再冷凝至室温,得到一种液体,称之为“绿矾油”,其主要成分为
)为原料在蒸馏釜中煅烧(隔离空气),除有水蒸气生成外,还有两种气体生成,然后再冷凝至室温,得到一种液体,称之为“绿矾油”,其主要成分为___________ (填化学式)。该方法中“煅烧”反应方程式为:___________ (补全反应化学方程式)。
 ___________
___________
(2)“铅室法”[使用了大容积铅室制备硫酸(76%以下)]与“塔士法”制硫酸的主要反应有:
___________ ___________
___________ ___________+___________
___________+___________
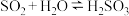
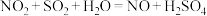


副反应: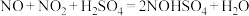
①补全反应化学方程式___________ 。
___________ ___________
___________ ___________+___________
___________+___________
② 在上述过程中作用为
在上述过程中作用为___________ 。
③上述方法生产硫酸的总反应为___________ 。
④为了适应化工生产的需求 “铅室法”、“塔式法”最终被接触法所代替,其主要原因是___________ (答出一点即可)。
(3)有关接触法制硫酸的叙述,其中错误的是___________。
(1)在18世纪40年代以前,生产硫酸最古老的方法是:以绿矾(
 )为原料在蒸馏釜中煅烧(隔离空气),除有水蒸气生成外,还有两种气体生成,然后再冷凝至室温,得到一种液体,称之为“绿矾油”,其主要成分为
)为原料在蒸馏釜中煅烧(隔离空气),除有水蒸气生成外,还有两种气体生成,然后再冷凝至室温,得到一种液体,称之为“绿矾油”,其主要成分为 ___________
___________(2)“铅室法”[使用了大容积铅室制备硫酸(76%以下)]与“塔士法”制硫酸的主要反应有:
___________
 ___________
___________ ___________+___________
___________+___________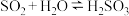
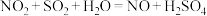


副反应:
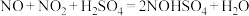
①补全反应化学方程式
___________
 ___________
___________ ___________+___________
___________+___________②
 在上述过程中作用为
在上述过程中作用为③上述方法生产硫酸的总反应为
④为了适应化工生产的需求 “铅室法”、“塔式法”最终被接触法所代替,其主要原因是
(3)有关接触法制硫酸的叙述,其中错误的是___________。
| A.用硫黄或含硫矿石均可作为原料 |
| B.尾气含有二氧化硫,在排入大气前需进行净化处理 |
| C.硫酸生产中涉及的化学反应全部是氧化还原反应 |
| D.硫酸生产中涉及的化学反应都需要使用催化剂 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】资源化利用二氧化硫,一方面能保护环境,另一方面能提高经济效益,具有深远意义。
(1)下列生产、生活活动中,不易产生SO2的是______。
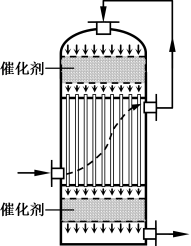
(2)工业中可用含SO2的冶炼烟气为原料生产硫酸,在右图装置中完成“SO2转化”工序。使用该装置实现了______。(双选)
(3)研究SO2的性质有利于探索其资源化利用。下列实验方案设计正确的是______。
(1)下列生产、生活活动中,不易产生SO2的是______。
| A.燃放鞭炮 | B.火力发电 | C.火山爆发 | D.海水晒盐 |
(2)工业中可用含SO2的冶炼烟气为原料生产硫酸,在右图装置中完成“SO2转化”工序。使用该装置实现了______。(双选)

| A.充分利用热能 |
| B.防止形成酸雾 |
| C.加速转化SO2 |
| D.获取纯净SO3 |
(3)研究SO2的性质有利于探索其资源化利用。下列实验方案设计正确的是______。
 |  |  |  |
| A.制取SO2 | B.收集SO2 | C.验证SO2水溶液的酸性 | D.验证SO2的还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
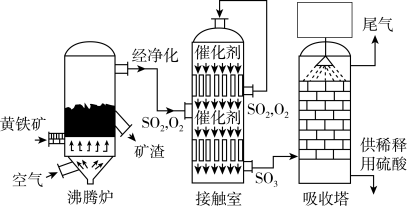
【推荐3】据图回答:
(1)将燃烧黄铁矿的化学方程式补充完整4______ 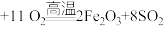
(2)沸腾炉中产生的矿渣可以用来生产_____________ (写出一种物质即可)。
(3)接触室中发生反应的化学方程是_________________ ,使用的催化剂是___________________ 。
(4)吸收塔顶部应该向下喷洒_______________ 来吸收三氧化硫,不用水吸收三氧化硫,原因是_______________ 。
(5)依据工艺流程图判断下列说法正确的是 _______________。
(6)氨酸法是一种硫酸尾气的脱硫工艺,其反应原理可表示为:① ,②
,②  ,请从绿色化学和综合利用的角度说该方案的主要优点
,请从绿色化学和综合利用的角度说该方案的主要优点_______________________________________ 。

(1)将燃烧黄铁矿的化学方程式补充完整4
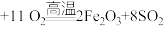
(2)沸腾炉中产生的矿渣可以用来生产
(3)接触室中发生反应的化学方程是
(4)吸收塔顶部应该向下喷洒
(5)依据工艺流程图判断下列说法正确的是 _______________。
| A.为使黄铁矿充分燃烧,需将其粉碎 | B.过量空气能提高SO2的转化率 |
| C.使用催化剂能提高SO2的反应速率和转化率 | D.接触室排出的矿渣可供炼铁 |
(6)氨酸法是一种硫酸尾气的脱硫工艺,其反应原理可表示为:①
 ,②
,②  ,请从绿色化学和综合利用的角度说该方案的主要优点
,请从绿色化学和综合利用的角度说该方案的主要优点
您最近一年使用:0次

 与水反应
与水反应 受热分解
受热分解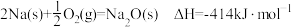
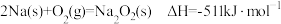
 与Na反应生成
与Na反应生成

