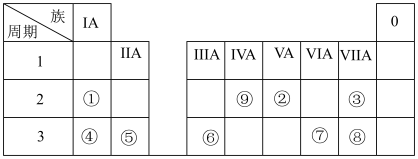
门捷列夫是俄国科学家,他发明的元素周期表是化学领域的重要里程碑。周期表的发明帮助人们更好地理解元素性质和变化规律。门捷列夫被誉为“现代化学之父”。_______ ,⑨最简单的气态氢化物的结构式为_______ 。
(2)写出④的最高价氧化物对应水化物和⑧的最高价氧化物对应水化物相互反应的化学方程式_______ 。
(3)③、④两种元素的简单离子半径大小关系_______ (填离子符号)。
(4)④、⑤和⑥中;金属性最强的元素是_______ (填元素符号);③和⑧两种元素形成的气态氢化物中,热稳定性强的是_______ (填化学式)。
(5)⑦、⑧中,非金属强的元素是_______ (填元素符号),请写出证明这一事实的化学方程式_______ 。
(6)②的最高价氧化物对应水化物的浓溶液与金属铜反应的化学方程式为_____ 。常温下,该浓溶液与金属铁、铝发生_____ 现象,体现该浓溶液的_______ 性。
(2)写出④的最高价氧化物对应水化物和⑧的最高价氧化物对应水化物相互反应的化学方程式
(3)③、④两种元素的简单离子半径大小关系
(4)④、⑤和⑥中;金属性最强的元素是
(5)⑦、⑧中,非金属强的元素是
(6)②的最高价氧化物对应水化物的浓溶液与金属铜反应的化学方程式为
更新时间:2024-05-07 11:12:24
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】A、B、C、D分别是NaNO3、NaOH、HNO3和Ba(NO3)2四种溶液中的一种。现利用另一种溶液X,用如下图所示的方法即可将它们确定。
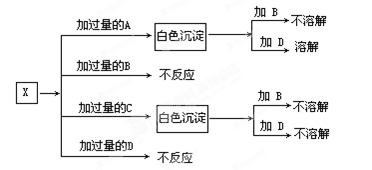
试确定A,B,C,D,X各代表何种溶液。
A:___________ B:___________ C:___________ D:___________ X:___________
写出加过量的A产生白色沉淀的化学方程式:_________________________________ 。
写出加过量的C产生白色沉淀的化学方程式:_________________________________ 。

试确定A,B,C,D,X各代表何种溶液。
A:
写出加过量的A产生白色沉淀的化学方程式:
写出加过量的C产生白色沉淀的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】某小组在实验室中探究金属钠与二氧化碳的反应。回答下列问题:
金属钠与二氧化碳反应的实验步骤及现象如下表:
(1)为检验集气瓶瓶壁上白色物质的成分。取适量滤液于2支试管中,向一支试管中滴加1滴酚酞溶液,溶液变红;向第二支试管中滴加澄清石灰水,溶液变浑浊。据此推断,白色物质的主要成分是____ (填标号)。
A.Na2O B.Na2O2 C.NaOH D.Na2CO3
(2)为检验黑色固体的成分,将其与浓硫酸反应,生成的气体具有刺激性气味。据此推断黑色固体是___ 。
(3)本实验中金属钠与二氧化碳反应的化学方程式为__________ 。
金属钠与二氧化碳反应的实验步骤及现象如下表:
| 步骤 | 现象 |
| 将一小块金属钠在燃烧匙中点燃,迅速伸入盛有CO2的集气瓶中。充分反应,放置冷却 | 产生大量白烟,集气瓶底部有黑色固体产生,瓶壁上有白色物质产生 |
| 在集气瓶中加入适量蒸馏水,振荡、过滤 | 滤纸上留下黑色固体,滤液为无色溶液 |
A.Na2O B.Na2O2 C.NaOH D.Na2CO3
(2)为检验黑色固体的成分,将其与浓硫酸反应,生成的气体具有刺激性气味。据此推断黑色固体是
(3)本实验中金属钠与二氧化碳反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】亚硝酰氯(NOCl,熔点:-64.5℃,沸点:-5.5℃)是一种黄色气体,遇水易水解。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。

(1)甲组的同学拟制备原料气NO和Cl2,制备装置如下图所示:
为制备纯净干燥的气体,下表中缺少的药品是:
(2)乙组同学利用甲组制得的NO和Cl2制备NOCl,装置如图所示:
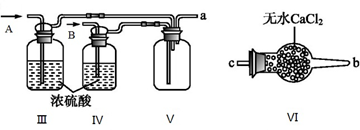
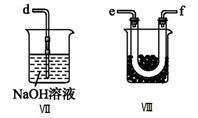
①为了使气体充分反应,从A处进入的气体是____________ (填Cl2或NO)。
②装置连接顺序为a→_______________________ (按气流自左向右方向,用小写字母表示)。
③装置Ⅲ、Ⅳ除可干燥NO、Cl2外,另一个作用是________________________ 。
④装置Ⅷ的烧杯中盛放的试剂是_____________________ (填编号①水②冰水③冰盐水)
⑤装置Ⅶ中吸收尾气时,NOCl发生反应的化学方程式为___________________________________ 。
(3)丙组同学查阅资料,查得王水是浓硝酸与浓盐酸的混酸,一定条件下混酸可生成亚硝酰氯和氯气,该反应的化学方程式为________________________________ 。

(1)甲组的同学拟制备原料气NO和Cl2,制备装置如下图所示:
为制备纯净干燥的气体,下表中缺少的药品是:
| 装置Ⅰ | 装置Ⅱ | ||
| 烧瓶中 | 分液漏斗中 | ||
| 制备纯净Cl2 | MnO2 | ① | ② |
| 制备纯净NO | Cu | ③ | ④ |


①为了使气体充分反应,从A处进入的气体是
②装置连接顺序为a→
③装置Ⅲ、Ⅳ除可干燥NO、Cl2外,另一个作用是
④装置Ⅷ的烧杯中盛放的试剂是
⑤装置Ⅶ中吸收尾气时,NOCl发生反应的化学方程式为
(3)丙组同学查阅资料,查得王水是浓硝酸与浓盐酸的混酸,一定条件下混酸可生成亚硝酰氯和氯气,该反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】A、B、C、D、E、F、G、L、I九种主族元素分布在三个不同的短周期,它们的原子序数依次增大,其中B、C、D为同一周期,A与E、B与G、D与L分别为同一主族,C、D、F三种元素的原子序数之和为28,F的质子数比D多5,D的最外层电子数是F最外层电子数的2倍,C和D的最外层电子数之和为11。请回答下列问题:
(1)以上元素中非金属所形成的最简单气态氢化物稳定性最弱的是(填化学式)____ ,E、F、L所形成的简单离子的半径由大到小的顺序为(用离子符号表示)___________ 。
(2)由L、I两元素可按原子个数比1:l组成化合物X,化合物X中各原子均满足8电子的稳定结构,则X的电子式为_____________________ 。
(3)固体化合物E2D2投入到化合物E2L的水溶液中,只观察到有沉淀产生,写出该反应的离子方程式______________________________________ 。
(4)由A、B、C、D按原子个数比4:1:1:2形成一种化合物Y,则Y的化学式为_______ ,向Y中加足量稀硫酸后,再加高锰酸钾溶液,可使酸性高锰酸钾溶液褪色,写出使酸性高锰酸钾溶液褪色的离子方程式_____________________ 。
(1)以上元素中非金属所形成的最简单气态氢化物稳定性最弱的是(填化学式)
(2)由L、I两元素可按原子个数比1:l组成化合物X,化合物X中各原子均满足8电子的稳定结构,则X的电子式为
(3)固体化合物E2D2投入到化合物E2L的水溶液中,只观察到有沉淀产生,写出该反应的离子方程式
(4)由A、B、C、D按原子个数比4:1:1:2形成一种化合物Y,则Y的化学式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐2】A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,B、W同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E地壳中含量最高的金属元素。
(1)E元素在周期表中的位置为_______ ;E的单质和氧化铁反应可用于野外焊接钢轨,写出反应的化学方程式_______ ;该反应属于_______ (填“吸热”或“放热”)反应。
(2)五种元素原子半径由大到小的顺序是(写元素符号)_______ ;W、D、E的简单离子半径由大到小的顺序是_______ (写离子符号)。
(3)由A和W组成的10电子的分子以及阴离子的化学式_______ ;由A、B、W三种元素组成的18电子微粒的分子式为_______ 。
(4)已知D2W2为淡黄色固体,将过量D2W2投入到含有Fe2+的溶液中,有红褐色沉淀生成,写出该反应的离子方程式_______ 。
(5)向含有Fe2+和淀粉KI的酸性溶液中滴入A2W2,观察到溶液呈蓝色并有红褐色沉淀生成,并且当消耗2molI-时,共转移的电子数为3mol,则该反应的离子方程式_______ 。
(6)元素D的单质在一定条件下与A单质生成DA,能与水反应生成A单质,若将1molDA和1molE的单质混合加入足量的水,充分反应,在标准状态下生成气体的体积_______ L。
(1)E元素在周期表中的位置为
(2)五种元素原子半径由大到小的顺序是(写元素符号)
(3)由A和W组成的10电子的分子以及阴离子的化学式
(4)已知D2W2为淡黄色固体,将过量D2W2投入到含有Fe2+的溶液中,有红褐色沉淀生成,写出该反应的离子方程式
(5)向含有Fe2+和淀粉KI的酸性溶液中滴入A2W2,观察到溶液呈蓝色并有红褐色沉淀生成,并且当消耗2molI-时,共转移的电子数为3mol,则该反应的离子方程式
(6)元素D的单质在一定条件下与A单质生成DA,能与水反应生成A单质,若将1molDA和1molE的单质混合加入足量的水,充分反应,在标准状态下生成气体的体积
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】有7种短周期主族元素,其中元素A、B、C、D原子序数依次减小,该四种元素原子K层电子总数为7,L层电子中总数为22,M层电子总数为12,E与B同主族,F与C同主族,短周期中G的原子半径最大,用化学用语或文字回答下列问题。
(1)A元素在周期表中的位置_____ ,画出B的原子结构示意图_____ 。
(2)A、C、F、G简单离子半径由大到小顺序_____ (用离子符号填写)。
(3)G、C按1∶1形成的化合物含化学键类型_____ ,写出该化合物的电子式_____ 。
(4)下列事实能说明A元素的非金属性比F元素的非金属性强的是____ 。
a.A单质与Na2S溶液反应溶液变混浊
b.F氢化物的酸性比A的氢化物酸性弱
c.A和F两元素的简单氢化物受热分解,前者的分解温度高
(5)在微电子工业中,E的简单气态氢化物的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为_____ 。
(1)A元素在周期表中的位置
(2)A、C、F、G简单离子半径由大到小顺序
(3)G、C按1∶1形成的化合物含化学键类型
(4)下列事实能说明A元素的非金属性比F元素的非金属性强的是
a.A单质与Na2S溶液反应溶液变混浊
b.F氢化物的酸性比A的氢化物酸性弱
c.A和F两元素的简单氢化物受热分解,前者的分解温度高
(5)在微电子工业中,E的简单气态氢化物的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】有A、B、C、D、E、F六种元素,原子序数依次增大,A、B、C、D、E均为短周期元素,D、F为常见金属元素。A元素原子核内只有一个质子,元素A与B形成的气态化合物甲在标准状况下的密度为0.759 g·L-1,C元素原子的最外层电子数是其电子层数的3倍,E与C同主族。均含D元素的乙(金属阳离子)、丙、丁微粒间的转化全为非氧化还原反应,均含F元素的乙(单质)、丙、丁微粒间的转化全为氧化还原反应。请回答下列问题:

(1)单质B的结构式:_____ ____。
(2)F元素周期表中的位置:_____ _____。
(3)均含有F元素的乙与丁在溶液中发生反应的离子方程式 。均含有D元素的乙与丁在溶液中发生反应的离子方程式_______ 。
(4)由A、C元素组成的化合物庚和A、E元素组成的化合物辛,相对分子质量均为34。其中庚的熔沸点比辛_________(填“高”或“低”),原因是___________________。

(1)单质B的结构式:_____ ____。
(2)F元素周期表中的位置:_____ _____。
(3)均含有F元素的乙与丁在溶液中发生反应的离子方程式 。均含有D元素的乙与丁在溶液中发生反应的离子方程式_______ 。
(4)由A、C元素组成的化合物庚和A、E元素组成的化合物辛,相对分子质量均为34。其中庚的熔沸点比辛_________(填“高”或“低”),原因是___________________。
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐2】分A、B、C是由周期表中短周期元素组成的三种常见化合物,甲、乙、丙是三种单质,这些单质和化合物之间存在如图1所示的关系,完成下列空白:
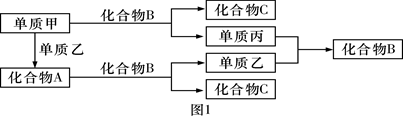
(1)向酚酞试液中加入化合物A的粉末,现象为 。
(2) 单质甲与化合物B反应的离子方程式为 。5.05 g单质甲—钾合金溶于200 mL水生成0.075 mol氢气,确定该合金的化学式为__ __。
(3)向20 mL某浓度的化合物C的溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.1 mol/L盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系如图2图示两种情况。

①由A确定滴加前60 mL的盐酸时,发生反应的离子方程式为 。
②由B表明,原溶液通入CO2气体后,所得溶液中的溶质的化学式为__ __。
③由A、B可知,两次实验通入的CO2的体积比为__ __。

(1)向酚酞试液中加入化合物A的粉末,现象为 。
(2) 单质甲与化合物B反应的离子方程式为 。5.05 g单质甲—钾合金溶于200 mL水生成0.075 mol氢气,确定该合金的化学式为__ __。
(3)向20 mL某浓度的化合物C的溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.1 mol/L盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系如图2图示两种情况。

①由A确定滴加前60 mL的盐酸时,发生反应的离子方程式为 。
②由B表明,原溶液通入CO2气体后,所得溶液中的溶质的化学式为__ __。
③由A、B可知,两次实验通入的CO2的体积比为__ __。
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】Ⅰ.几种短周期元素的原子半径及主要化合价如下表:已知X是短周期中最活泼的金属,且与R同周期。(请用化学用语答题)
(1)R的元素符号为_______ ; M在元素周期表中的位置为___________________ 。
(2)X与Y按原子个数比1:1构成的物质的电子式为________ ;所含化学键类型________ 。
(3)X+, Y2‾,M2‾ 离子半径大小顺序为________________________________ 。
(4)将YM2通入FeCl3溶液中的离子方程式_________________________________ 。
(5)用Cu单质作阳极,石墨作阴极,X的最高价氧化物对应的水化物溶液作电解液进行电解,写出阳极的反应式_________________________ 。
Ⅱ.如下图转化关系

①若B为白色胶状不溶物,则A与C反应的离子方程式为____________________________ 。
②若向B溶液中滴加铁氰化钾溶液会产生特征蓝色沉淀,则A与C反应的离子方程式为______________________________ 。
元素代号 | X | Y | Z | M | R |
原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
主要化合价 | +1 | +6 -2 | +5 -3 | -2 | +3 |
(2)X与Y按原子个数比1:1构成的物质的电子式为
(3)X+, Y2‾,M2‾ 离子半径大小顺序为
(4)将YM2通入FeCl3溶液中的离子方程式
(5)用Cu单质作阳极,石墨作阴极,X的最高价氧化物对应的水化物溶液作电解液进行电解,写出阳极的反应式
Ⅱ.如下图转化关系

①若B为白色胶状不溶物,则A与C反应的离子方程式为
②若向B溶液中滴加铁氰化钾溶液会产生特征蓝色沉淀,则A与C反应的离子方程式为
您最近一年使用:0次



