我国的冶金工业十分发达,钢铁年产量已达到十亿吨,占世界产量的一半以上,同时有色金属产量也超过了七千万吨。
(1)铜是人类最早使用的金属,其电阻率小、延展性好,常用于制作电路板,在使用氯化铁溶液蚀刻铜制电路板时,发生反应的化学方程式为___________ 。
(2)铝与 溶液反应的化学方程式为
溶液反应的化学方程式为___________ ;铝的化学性质较活泼,但在空气中不会完全锈蚀,其原因是___________ 。
(3)电镀是一种常见的金属处理工艺,然而在生产过程中,电镀厂会产生大量的高毒性废水,将其直接排放会造成严重的污染。因此,废水的处理是电镀行业面临的主要问题之一。
①在电镀之前,镀件需要用酸性 溶液浸泡清洗。清洗废液的处理需要去除其中的悬浮颗粒物,并加入足量的
溶液浸泡清洗。清洗废液的处理需要去除其中的悬浮颗粒物,并加入足量的 固体,将
固体,将 还原为
还原为 ,则还原过程中发生反应的离子方程式为
,则还原过程中发生反应的离子方程式为___________ ,当有 被完全处理时,理论上需要加入
被完全处理时,理论上需要加入 的质量为
的质量为___________ 。
②为了减缓镀件表面的金属沉积速率,得到均匀、光滑的镀层,电解液中除重金属盐外,还需要加入剧毒的 。已知
。已知 中各原子均满足8电子稳定结构,则
中各原子均满足8电子稳定结构,则 的电子式为
的电子式为___________ 。在碱性的废电解液中通入氯气可以将 氧化,并生成两种无毒的氧化产物(其中一种为大气中占比最多的成分),则反应的离子方程式为
氧化,并生成两种无毒的氧化产物(其中一种为大气中占比最多的成分),则反应的离子方程式为___________ 。
(1)铜是人类最早使用的金属,其电阻率小、延展性好,常用于制作电路板,在使用氯化铁溶液蚀刻铜制电路板时,发生反应的化学方程式为
(2)铝与
 溶液反应的化学方程式为
溶液反应的化学方程式为(3)电镀是一种常见的金属处理工艺,然而在生产过程中,电镀厂会产生大量的高毒性废水,将其直接排放会造成严重的污染。因此,废水的处理是电镀行业面临的主要问题之一。
①在电镀之前,镀件需要用酸性
 溶液浸泡清洗。清洗废液的处理需要去除其中的悬浮颗粒物,并加入足量的
溶液浸泡清洗。清洗废液的处理需要去除其中的悬浮颗粒物,并加入足量的 固体,将
固体,将 还原为
还原为 ,则还原过程中发生反应的离子方程式为
,则还原过程中发生反应的离子方程式为 被完全处理时,理论上需要加入
被完全处理时,理论上需要加入 的质量为
的质量为②为了减缓镀件表面的金属沉积速率,得到均匀、光滑的镀层,电解液中除重金属盐外,还需要加入剧毒的
 。已知
。已知 中各原子均满足8电子稳定结构,则
中各原子均满足8电子稳定结构,则 的电子式为
的电子式为 氧化,并生成两种无毒的氧化产物(其中一种为大气中占比最多的成分),则反应的离子方程式为
氧化,并生成两种无毒的氧化产物(其中一种为大气中占比最多的成分),则反应的离子方程式为
更新时间:2024-05-08 21:35:09
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】工业上常用电解 溶液制备
溶液制备 ,反应方程式如下:
,反应方程式如下: 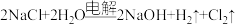
回答下列问题:
(1)用电子式表示 的形成过程:
的形成过程:_______ ;
(2) 属于
属于_______ 化合物(填“离子”或“共价”),用电子式表示 的形成过程
的形成过程_______ ;
(3) 中含有的化学键类型是
中含有的化学键类型是_______ ,其电子式为_______ ;
(4)用含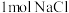 的溶液进行电解制备
的溶液进行电解制备 。
。
①该 溶液中
溶液中 的物质的量是
的物质的量是_______ 
②标准状况下,理论上最多能产生
_______ L;
③当 完全被电解消耗完时,产生的
完全被电解消耗完时,产生的 的质量为
的质量为_______ g;
④两种气体产物相同条件下的密度比是_______ 。
 溶液制备
溶液制备 ,反应方程式如下:
,反应方程式如下: 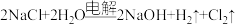
回答下列问题:
(1)用电子式表示
 的形成过程:
的形成过程:(2)
 属于
属于 的形成过程
的形成过程(3)
 中含有的化学键类型是
中含有的化学键类型是(4)用含
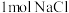 的溶液进行电解制备
的溶液进行电解制备 。
。①该
 溶液中
溶液中 的物质的量是
的物质的量是
②标准状况下,理论上最多能产生

③当
 完全被电解消耗完时,产生的
完全被电解消耗完时,产生的 的质量为
的质量为④两种气体产物相同条件下的密度比是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】回答下列问题:
(1)写出下列物质的电子式CO2_______ 、HF_______ 、KCl_______ 、NaOH_______ 、
(2)用电子式表示下列物质的形成过程
H2O:_______ 。
Na2O:_______ 。
(1)写出下列物质的电子式CO2
(2)用电子式表示下列物质的形成过程
H2O:
Na2O:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】如图是元素周期表的一部分,针对表中的①~⑩中元素,填写下列空格:
(1)在这10种元素中,原子半径较小的是__ (填元素符号,稀有气体除外),化学性质最不活泼的元素是__ (填“元素名称”)。
(2)元素⑧的离子结构示意图为__ ,请用电子式表示化合物④和⑧的形成过程__ 。
(3)元素⑤的单质与氢氧化钠溶液反应的化学方程式为:__ 。
(4)元素⑧单质的水溶液中通入元素⑦的某种氧化物,该氧化物被氧化为元素⑦的最高价氧化物的水化物,反应的化学方程式为__ 。
| ① | ⑩ | ② | ③ | ||||||||||||||
| ④ | ⑤ | ⑦ | ⑧ | ⑨ | |||||||||||||
| ⑥ | |||||||||||||||||
(1)在这10种元素中,原子半径较小的是
(2)元素⑧的离子结构示意图为
(3)元素⑤的单质与氢氧化钠溶液反应的化学方程式为:
(4)元素⑧单质的水溶液中通入元素⑦的某种氧化物,该氧化物被氧化为元素⑦的最高价氧化物的水化物,反应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】写出下列反应的离子方程式。
(1)氢氧化钠溶液与硫酸溶液:______________________________________________ ;
(2)氯化钠溶液与硝酸银溶液:________________________________________________ ;
(3)氢氧化钡溶液和硫酸溶液:____________________________________________ ;
(4)碳酸钠溶液与稀硫酸反应:_______________________________________________ ;
(5)铁与稀盐酸反应:________________________________________________________ 。
(1)氢氧化钠溶液与硫酸溶液:
(2)氯化钠溶液与硝酸银溶液:
(3)氢氧化钡溶液和硫酸溶液:
(4)碳酸钠溶液与稀硫酸反应:
(5)铁与稀盐酸反应:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】(1)①Cu ②CO2 ③K2SO3 ④液氨 ⑤液态H2SO4 ⑥熔融Ba(OH)2 ⑦蔗糖 ⑧NaOH溶液。上述物质中属于电解质的是____________ (填序号,下同),属于非电解质的是___________ ,能导电的是_______________ 。
(2)写出下列反应的离子方程式
①向Ba(OH)2溶液中滴入NaHSO4至溶液呈中性____________________________________ 。
②足量的NaHCO3溶液与少量Ca(OH)2的溶液反应__________________________________ 。
(2)写出下列反应的离子方程式
①向Ba(OH)2溶液中滴入NaHSO4至溶液呈中性
②足量的NaHCO3溶液与少量Ca(OH)2的溶液反应
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】完成下列问题。
(1)按要求写出方程式:
①Fe2(SO4)3的电离方程式___________ 。
②用一种试剂除去BaCl2(HCl)中的杂质(括号内的物质为杂质),写出反应的离子方程式___________
③过量的二氧化碳通入澄清石灰水中的离子方程式___________ 。
(2)写出下列反应方程式。
①铁在氯气中燃烧___________ ;
②钠和水的反应___________ ;
(3)用单线桥法表示反应2H2S+SO2=3S↓+2H2O电子得失的方向和数目:___________ 。
(1)按要求写出方程式:
①Fe2(SO4)3的电离方程式
②用一种试剂除去BaCl2(HCl)中的杂质(括号内的物质为杂质),写出反应的离子方程式
③过量的二氧化碳通入澄清石灰水中的离子方程式
(2)写出下列反应方程式。
①铁在氯气中燃烧
②钠和水的反应
(3)用单线桥法表示反应2H2S+SO2=3S↓+2H2O电子得失的方向和数目:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】阅读有关硫代硫酸钠(Na2S2O3)的相关资料:
硫代硫酸钠是一种白色的晶体,可用作冲洗照相底片的定影剂、棉织物漂白后的脱氯剂及定量分析中的还原剂。它在碱性环境中能稳定存在,在酸性条件下发生反应生成SO2和S。制备Na2S2O3的方法很多,常用的方法有:Ⅰ.将纯碱溶解后,与二氧化硫作用生成亚硫酸钠,再加入硫磺沸腾反应,经过滤、浓缩、结晶,制得五水硫代硫酸钠(Na2S2O3·5H2O)。Ⅱ.硫化碱法:利用碳酸钠、硫化钠和废气中的二氧化硫反应,经吸硫、蒸发、结晶,制得硫代硫酸钠。Ⅲ.氧化、亚硫酸钠和重结晶法:由含硫化钠、亚硫酸钠和烧碱的液体经加硫氧化……。
回答下列问题:
(1)Na2S2O3和HCl反应的离子方程式___ 。
(2)方法Ⅰ中所包含的反应___ (写方程式)。
(3)方法Ⅱ中做氧化剂的物质是___ (化学式),做还原剂的是__ (化学式)。
硫代硫酸钠是一种白色的晶体,可用作冲洗照相底片的定影剂、棉织物漂白后的脱氯剂及定量分析中的还原剂。它在碱性环境中能稳定存在,在酸性条件下发生反应生成SO2和S。制备Na2S2O3的方法很多,常用的方法有:Ⅰ.将纯碱溶解后,与二氧化硫作用生成亚硫酸钠,再加入硫磺沸腾反应,经过滤、浓缩、结晶,制得五水硫代硫酸钠(Na2S2O3·5H2O)。Ⅱ.硫化碱法:利用碳酸钠、硫化钠和废气中的二氧化硫反应,经吸硫、蒸发、结晶,制得硫代硫酸钠。Ⅲ.氧化、亚硫酸钠和重结晶法:由含硫化钠、亚硫酸钠和烧碱的液体经加硫氧化……。
回答下列问题:
(1)Na2S2O3和HCl反应的离子方程式
(2)方法Ⅰ中所包含的反应
(3)方法Ⅱ中做氧化剂的物质是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】(1)配平下列化学方程式________ :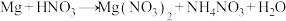 。
。
(2)上述反应中硝酸表现出来的性质是____________ (填序号)。
①还原性 ②酸性 ③氧化性
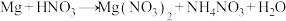 。
。(2)上述反应中硝酸表现出来的性质是
①还原性 ②酸性 ③氧化性
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】(1)写出下列物质在水溶液中的电离方程式:
①H2SO4__________ ;
②NH4NO3_________ 。
(2)写出下列反应的离子方程式
①氢氧化钡和稀硫酸反应:__________________ ;
②碳酸氢钠溶液和稀盐酸反应:______________ ;
(3)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式并用双线桥法表示电子转移的方向和数目:______________ 。
(4)将氯气溶于一定浓度的氢氧化钠溶液可制得“84消毒液”,反应的离子方程式为______
(5)有以下物质:①铁红②Al③C④稀硫酸⑤浓硫酸⑥NaOH溶液⑦Al2(SO4)3既能跟④又能跟⑥反应的是______ (填序号),写出它与⑥反应的化学方程式________ 。
①H2SO4
②NH4NO3
(2)写出下列反应的离子方程式
①氢氧化钡和稀硫酸反应:
②碳酸氢钠溶液和稀盐酸反应:
(3)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式并用双线桥法表示电子转移的方向和数目:
(4)将氯气溶于一定浓度的氢氧化钠溶液可制得“84消毒液”,反应的离子方程式为
(5)有以下物质:①铁红②Al③C④稀硫酸⑤浓硫酸⑥NaOH溶液⑦Al2(SO4)3既能跟④又能跟⑥反应的是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】现有下列10种物质:①H2O②Cl2③Al④P2O5⑤稀硫酸⑥NaOH⑦AgNO3⑧碘酒⑨Ca⑩Ba(HCO3)2。
(1)其中属于电解质的是___________ (填序号)。
(2)②在元素周期表中的位置是___________ ,写出⑨的原子结构示意图___________ 。
(3)请写出③⑥反应的化学方程式___________ 。
(4)请写出足量⑤与⑩反应的离子方程式___________ 。
(1)其中属于电解质的是
(2)②在元素周期表中的位置是
(3)请写出③⑥反应的化学方程式
(4)请写出足量⑤与⑩反应的离子方程式
您最近一年使用:0次



