利用图所示装置进行铜与硝酸反应的实验。 ___________ 。
(2)使用稀硝酸进行实验:反应开始后,铜丝逐渐变细,有气泡产生,溶液变蓝。
① 铜与稀硝酸反应的离子方程式为___________ 。
② 实验中观察到试管中的气体略有红棕色,其原因是___________ (用化学方程式表示)。
(3)使用浓硝酸进行实验:反应剧烈进行,铜丝逐渐变细,溶液变绿,试管上方出现红棕色气体。 铜与浓硝酸反应的化学方程式为___________ 。

(2)使用稀硝酸进行实验:反应开始后,铜丝逐渐变细,有气泡产生,溶液变蓝。
① 铜与稀硝酸反应的离子方程式为
② 实验中观察到试管中的气体略有红棕色,其原因是
(3)使用浓硝酸进行实验:反应剧烈进行,铜丝逐渐变细,溶液变绿,试管上方出现红棕色气体。 铜与浓硝酸反应的化学方程式为
更新时间:2024-05-11 09:13:53
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】请写出下列反应的化学方程式或离子方程式:
(1)过量二氧化碳通入偏铝酸钠溶液的离子方程式:______________ ;
(2)向氯化铝溶液中加入过量的氢氧化钠溶液的离子方程式:__________ ;
(3)浓硝酸见光分解的化学方程式:__________ ;
(4)氨的催化氧化的化学方程式:______________ 。
(1)过量二氧化碳通入偏铝酸钠溶液的离子方程式:
(2)向氯化铝溶液中加入过量的氢氧化钠溶液的离子方程式:
(3)浓硝酸见光分解的化学方程式:
(4)氨的催化氧化的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下列说法不正确的是____________________ 。
A.用100mL的容量瓶准确量取100mL液体
B.分液时,分液漏斗中下层液体从下口流出,上层液体从上口倒出
C.用托盘天平称量NaCl时,NaCl放在纸上;称量NaOH时,NaOH放在小烧杯里
D.用加热的方法提取NH4C1固体中含有的少量碘单质
E.浓硝酸与浓盐酸均易挥发,故都必须保存在棕色试剂瓶中,并置于阴凉处
A.用100mL的容量瓶准确量取100mL液体
B.分液时,分液漏斗中下层液体从下口流出,上层液体从上口倒出
C.用托盘天平称量NaCl时,NaCl放在纸上;称量NaOH时,NaOH放在小烧杯里
D.用加热的方法提取NH4C1固体中含有的少量碘单质
E.浓硝酸与浓盐酸均易挥发,故都必须保存在棕色试剂瓶中,并置于阴凉处
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】研究氮及其化合物的性质,可以有效改善人类的生存环境。氮元素化合价—物质类别关系图如图。

回答下列问题:
(1)在催化剂和加热的条件下,物质A生成 是工业制硝酸的重要反应,化学方程式是
是工业制硝酸的重要反应,化学方程式是________________ 。
(2)在加热条件下,物质C的浓溶液与碳单质反应,写出反应的化学方程式:________________________ 。
(3)实验室中,检验溶液中含有 的操作方法是
的操作方法是___________________________________________ 。
(4)物质B为红棕色气体,写出该物质与水反应的离子方程式:________________________ ,当反应消耗 (标准状况)物质B时,转移电子的物质的量为
(标准状况)物质B时,转移电子的物质的量为________ mol。
(5)在加热条件下,物质C的稀溶液与铜反应,写出反应的化学方程式:________________________ 。

回答下列问题:
(1)在催化剂和加热的条件下,物质A生成
 是工业制硝酸的重要反应,化学方程式是
是工业制硝酸的重要反应,化学方程式是(2)在加热条件下,物质C的浓溶液与碳单质反应,写出反应的化学方程式:
(3)实验室中,检验溶液中含有
 的操作方法是
的操作方法是(4)物质B为红棕色气体,写出该物质与水反应的离子方程式:
 (标准状况)物质B时,转移电子的物质的量为
(标准状况)物质B时,转移电子的物质的量为(5)在加热条件下,物质C的稀溶液与铜反应,写出反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】Ⅰ.(1)在100 mL 0.8mol/L硝酸溶液中加入足量铜粉,则被溶解的铜的质量为_______ g。
(2)在上述溶液中再加入足量稀硫酸,又有_______ g铜溶解。
Ⅱ. 请回答下列问题:25℃时,浓度均为0.10mol • L﹣1的 ①氨水 ②NH4Cl溶液
(1)NH4Cl溶液显_________ (酸、碱、中)性,原因是(用离子方程式表示)____________________________________ ,若加入少量的氨水,使溶液中c(NH4+)=c(Cl﹣),则溶液的pH_____ 7 (填“>”、“<”或“=”).
(2)氨水显碱性的原因(用离子方程式表示)______________________ ,向氨水中加入NH4Cl固体,氨水的电离程度________ (填“增大”、“减小”或“不变”),溶液的pH将________ (填“增大”、“减小”或“不变”).
(2)在上述溶液中再加入足量稀硫酸,又有
Ⅱ. 请回答下列问题:25℃时,浓度均为0.10mol • L﹣1的 ①氨水 ②NH4Cl溶液
(1)NH4Cl溶液显
(2)氨水显碱性的原因(用离子方程式表示)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】在化学课上围绕浓硫酸的化学性质进行如下实验探究,将适量的蔗糖放入烧杯中,加几滴水,搅拌均匀,然后加入浓硫酸,生成黑色物质。请回答下列问题:
(1)这种黑色物质继续与浓硫酸作用会产生两种气体,其中一种气体有刺激性气味,是大气的污染物之一,反应的化学方程式为______ 。
(2)根据蔗糖与浓硫酸反应的实验现象,说明浓硫酸具有(填字母)_____ 。
(3)将(2)中产生的有刺激性气味的气体通入品红溶液中,可以看到品红溶液______ ,说明这种气体有_____ 性;将(2)中产生的有刺激性气味的气体通入氯水中,发生反应的化学方程式为_____ 。
(4)能否用澄清石灰水鉴别(2)中产生的两种气体(填“能”或“不能”)_____ ,若不能,请写出两种可以鉴别这两种气体的试剂:_____ 。
(1)这种黑色物质继续与浓硫酸作用会产生两种气体,其中一种气体有刺激性气味,是大气的污染物之一,反应的化学方程式为
(2)根据蔗糖与浓硫酸反应的实验现象,说明浓硫酸具有(填字母)
| A.酸性 | B.吸水性 | C.脱水性 | D.强氧化性 |
(4)能否用澄清石灰水鉴别(2)中产生的两种气体(填“能”或“不能”)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】硫酸铜可用于消毒、制杀虫剂、镀铜等。实验小组制取CuSO4·5H2O晶体并进行热分解的探究。请回答以下问题:
探究Ⅰ:制取CuSO4·5H2O晶体
小组同学设计了如下两种方案:
甲:将铜片加入足量浓硫酸中并加热
乙:将铜片加入稀硫酸,控温40~50℃,滴加双氧水
(1)方案甲发生反应的化学方程式为____________ ,反应结束后有大量白色固体析出。简述从中提取CuSO4·5H2O晶体的方法:倒出剩余液体,____________ 。
(2)方案乙发生反应:Cu+H2SO4+H2O2=CuSO4+2H2O,该实验控温40~50℃的原因是________ ;与方案甲相比,方案乙的主要优点有_________ 、___________ 。(写出2种)
探究Ⅱ:用以下装置(加热装置省略)探究CuSO4·5H2O晶体热分解产物
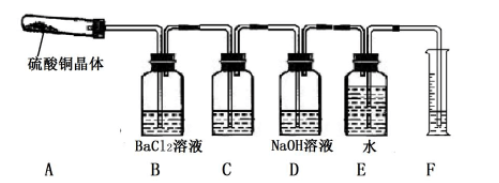
已知:CuSO4·5H2O脱水后升高温度,会继续分解成CuO 和气体产物,气体产物可能含有SO3、SO2、O2中的1~3 种。
(3)称5.00gCuSO4·5H2O于A 中加热,当观察到A中出现_____________ ,可初步判断晶体已完全脱水并发生分解。加热一段时间后,A中固体质量为3.00g,则此时A中固体的成分为___________ 。
(4)装置B中迅速生成白色沉淀,说明分解产物中有__________ ,C装置的作用是____________ 。
(5)理论上E中应收集到VmL气体,事实上体积偏少,可能的原因是______________ 。(不考虑泄漏等仅器与操作原因)。
探究Ⅰ:制取CuSO4·5H2O晶体
小组同学设计了如下两种方案:
甲:将铜片加入足量浓硫酸中并加热
乙:将铜片加入稀硫酸,控温40~50℃,滴加双氧水
(1)方案甲发生反应的化学方程式为
(2)方案乙发生反应:Cu+H2SO4+H2O2=CuSO4+2H2O,该实验控温40~50℃的原因是
探究Ⅱ:用以下装置(加热装置省略)探究CuSO4·5H2O晶体热分解产物

已知:CuSO4·5H2O脱水后升高温度,会继续分解成CuO 和气体产物,气体产物可能含有SO3、SO2、O2中的1~3 种。
(3)称5.00gCuSO4·5H2O于A 中加热,当观察到A中出现
(4)装置B中迅速生成白色沉淀,说明分解产物中有
(5)理论上E中应收集到VmL气体,事实上体积偏少,可能的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ.根据下表左边的“实验操作”,从右边的“实验现象”中选择正确的字母代号,填入对应“答案”的空格中。
Ⅱ.某校化学兴趣小组,通过下列装置探究Na2CO3和NaHCO3的热稳定性,设计如下的探究方案,请你参与并完成该探究方案。
(1)提出假设:Na2CO3或NaHCO3加热分解时可能有CO2生成。
(2)设计实验:①利用下图装置分别对一定量的Na2CO3和NaHCO3进行加热;②为了检验CO2的生成,试管B中应加入的物质是_____________ 。
(3)现象与结论:同学们发现只有在加热NaHCO3时,试管B中才有气泡产生且有_______________ 沉淀生成(填沉淀的颜色),说明Na2CO3和NaHCO3的热稳定性是:Na2CO3_______ NaHCO3(填“>”或“<”)。
(4)某同学在探究NaHCO3的热稳定性时,称取了8.4gNaHCO3,充分加热,请你计算理论上可产生CO2气体的体积为__________ L(标准状况)。
| 实验操作 | 答案 | 实验现象 |
| (1)让一束光线通过Fe(OH)3胶体 | A.呈蓝色 B.生成白色胶状沉淀 C.呈现光亮“通路” D.产生红褐色沉淀 | |
| (2)向盛有FeCl3溶液的试管中加入NaOH溶液 | ||
| (3)向Al2(SO4)3溶液中滴加氨水 | ||
| (4)向土豆片上滴加碘水 |
Ⅱ.某校化学兴趣小组,通过下列装置探究Na2CO3和NaHCO3的热稳定性,设计如下的探究方案,请你参与并完成该探究方案。
(1)提出假设:Na2CO3或NaHCO3加热分解时可能有CO2生成。
(2)设计实验:①利用下图装置分别对一定量的Na2CO3和NaHCO3进行加热;②为了检验CO2的生成,试管B中应加入的物质是
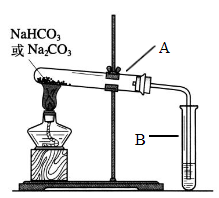
(3)现象与结论:同学们发现只有在加热NaHCO3时,试管B中才有气泡产生且有
(4)某同学在探究NaHCO3的热稳定性时,称取了8.4gNaHCO3,充分加热,请你计算理论上可产生CO2气体的体积为
您最近一年使用:0次



