下列说法中正确的是
| A.反应热指的是反应过程中放出的热量 |
| B.热化学方程式中各物质前的化学计量数的意义之一是表示分子的个数 |
| C.在热化学方程中生成物必须标明聚集状态,反应物不需标明 |
| D.所有的化学反应都伴随着能量变化 |
更新时间:2024-05-12 12:55:40
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】关于化学反应,下列说法正确的是
| A.化学反应除了生成新物质外,还伴随着能量的变化,且均表现为吸热 |
| B.能量守恒定律说明,必须从外界吸收能量后才表现出放热 |
| C.石墨完全转化为金刚石时,要吸收热量,说明金刚石比石墨更稳定 |
| D.化学反应是吸热还是放热取决于生成物具有的总能量和反应物具有的总能量的相对大小 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列反应中既是氧化还原反应又是吸热反应的是
| A.钾与水的反应 |
| B.灼热的木炭与CO2反应 |
| C.酒精的燃烧反应 |
| D.Ba(OH)2·8H2O晶体与NH4Cl晶体的反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】下列关于反应能量的说法正确的是
A.已知: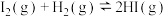 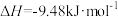 。若将1mol 。若将1mol  (g)和1mol (g)和1mol  (g)置于密闭容器中充分反应后,放出热量为9.48kJ (g)置于密闭容器中充分反应后,放出热量为9.48kJ |
B.已知: 的燃烧热为285.8 的燃烧热为285.8 。表示氢气燃烧热的热化学方程式为 。表示氢气燃烧热的热化学方程式为 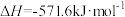 |
C.同温同压下, 在光照和点燃条件下的 在光照和点燃条件下的 不同 不同 |
D.已知中和热为57.3 , ,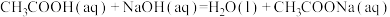 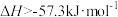 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列与化学反应能量变化相关的叙述中,正确的是
| A.热化学方程式的ΔH大小与化学计量数无关 |
| B.利用盖斯定律,可计算某些难以直接测量的反应焓变 |
| C.H2(g)的燃烧热ΔH=-285.8kJ·mol-1,则反应2H2O(g)=2H2(g)+O2(g)的反应热ΔH=+571.6kJ·mol-1 |
| D.测定中和反应反应热的时候,测量盐酸和NaOH混合溶液刚开始的温度,记为反应前体系的温度 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】工业生产硫酸过程中,SO2在接触室中被催化氧化为SO3,已知该反应为一放热反应。现将2 mol SO2、1 mol O2充入一密闭容器中充分反应后,放出热量98.3 kJ,此时测得SO2的物质的量为1 mol。则下列热化学方程式正确的是
| A.2SO2(g)+O2(g)=2SO3(g) ΔH=-196.6 kJ·mol-1 |
| B.2SO2(g)+O2(g)=2SO3(g) ΔH=-98.3 kJ·mol-1 |
C.SO2(g)+ O2(g) =SO3(g) ΔH=+98.3 kJ·mol-1 O2(g) =SO3(g) ΔH=+98.3 kJ·mol-1 |
D.SO2(g)+ O2(g)=SO3(g) ΔH=+196.6 kJ·mol-1 O2(g)=SO3(g) ΔH=+196.6 kJ·mol-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列热化学方程式书写正确的是(△H的绝对值均正确)
| A.C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g) △H= -1367.0kJ/mol (△H代表乙醇燃烧热) |
| B.H2SO4 (aq)+2NaOH(aq)=Na2SO4(aq)+2H2O(l) △H=-114.6kJ/mol (△H代表中和热) |
| C.2H2(g)+O2(g)=2H2O(g) ΔH=- 483.6 kJ/mol (反应热) |
| D.C+O2=CO2 ΔH=-393.5 kJ/mol (反应热) |
您最近一年使用:0次



