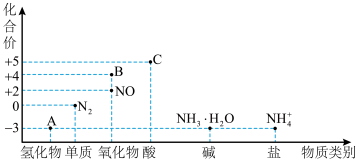
研究氮及其化合物的性质,可以有效改善人类的生存环境。氮元素化合价—物质类别关系图如图。
(1)实验室制备A的化学方程式为___________ 。
(2)在催化剂和加热的条件下,物质A生成NO是工业制硝酸的重要反应,化学方程式是___________ 。
(3)实验室中C的浓溶液通常保存在棕色瓶中,请用化学方程式解释原因:___________ 。
(4)实验室中,检验溶液中含有 的操作方法是
的操作方法是___________ 。
(5)物质B为红棕色气体,写出该物质与水反应的离子方程式:___________ ,当反应消耗3.36L(标准状况)物质B时,转移电子的物质的量为___________ mol。
(6)物质C的稀溶液与铜反应,写出反应的离子方程式:___________ 。
(1)实验室制备A的化学方程式为
(2)在催化剂和加热的条件下,物质A生成NO是工业制硝酸的重要反应,化学方程式是
(3)实验室中C的浓溶液通常保存在棕色瓶中,请用化学方程式解释原因:
(4)实验室中,检验溶液中含有
 的操作方法是
的操作方法是(5)物质B为红棕色气体,写出该物质与水反应的离子方程式:
(6)物质C的稀溶液与铜反应,写出反应的离子方程式:
更新时间:2024/05/09 12:59:53
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】我们通过高中化学课的学习已经掌握了元素周期律、周期表部分的相关内容,下面我们试着检测一下自己的学习效果吧。如表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语 回答下列问题:
(1)④、⑤、⑥的原子半径由大到小的顺序为____ 。
(2)②、③、⑧的最高价含氧酸的酸性由强到弱的顺序是____ 。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式____ 。
(4)由表中两种元素的原子按1︰1组成的常见液态化合物的稀液易被催化分解,可使用的催化剂为(填序号)____ 。
a.MnO2 b.Na2SO3 c.KMnO4
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:____ ,N→⑥的单质的化学方程式为____ 。
(6)铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两种气体均由上表中两种元素组成,气体的相对分子质量都小于50。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗1L 2.2mol/L NaOH溶液和1mol O2,则两种气体分子式及物质的量分别为____ 。
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(2)②、③、⑧的最高价含氧酸的酸性由强到弱的顺序是
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式
(4)由表中两种元素的原子按1︰1组成的常见液态化合物的稀液易被催化分解,可使用的催化剂为(填序号)
a.MnO2 b.Na2SO3 c.KMnO4
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:

(6)铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两种气体均由上表中两种元素组成,气体的相对分子质量都小于50。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗1L 2.2mol/L NaOH溶液和1mol O2,则两种气体分子式及物质的量分别为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】下图是中学化学中常见物质的转化关系,部分物质和反应条件略去。
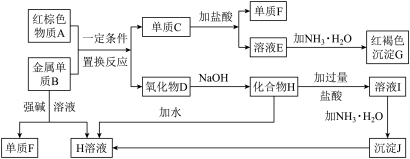
(1)单质F的化学式是_______________ 。
(2)写出单质B与强碱溶液反应的离子方程式___________________________ ,写出由沉淀J生成H溶液的离子方程式______________________________________ 。
(3)溶液E中加入氨水时,先生成白色沉淀L,写出生成L的离子方程式:____________________________________________ ,白色沉淀L最终变为红褐色沉淀G,写出L变为G的化学反应方程式______________________________ 。
(4)溶液I中所含金属离子是__________________ 。

(1)单质F的化学式是
(2)写出单质B与强碱溶液反应的离子方程式
(3)溶液E中加入氨水时,先生成白色沉淀L,写出生成L的离子方程式:
(4)溶液I中所含金属离子是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】为探究矿石样品X(仅有两种元素)的组成和性质,设计了如下实验:
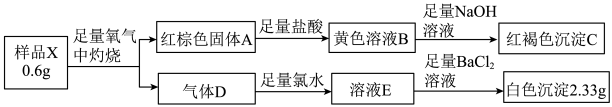
已知:气体D可以使品红溶液褪色。请回答下列问题:
(1)红褐色沉淀C的化学成分___________ (写化学式)。
(2)X中所含元素有___________ (写元素符号)。
(3)X在O2中灼烧的化学方程式___________ 。
(4)气体D和溶液B反应的离子方程式___________ 。
(5)假设气体D和氯水恰好完全反应,请设计实验方案检验溶液E中所含的阴离子________ 。

已知:气体D可以使品红溶液褪色。请回答下列问题:
(1)红褐色沉淀C的化学成分
(2)X中所含元素有
(3)X在O2中灼烧的化学方程式
(4)气体D和溶液B反应的离子方程式
(5)假设气体D和氯水恰好完全反应,请设计实验方案检验溶液E中所含的阴离子
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某学生欲通过实验方法验证Fe2+的性质。
(1)该同学在实验前,依据Fe2+的_______ 性,填写下表。
依照表中操作,该同学进行实验。观察到液面上方气体逐渐变为红棕色,但试管中溶液颜色却变为深棕色。为了进一步探究溶液变成深棕色的原因,该同学进行如下实验。
(2)向原新制FeSO4溶液和反应后溶液中均加入KSCN溶液,前者不变红色,后者(加了数滴浓硝酸的FeSO4溶液)变红。该现象的结论是_______ 。
(3)该同学通过查阅资料,认为溶液的深棕色可能是NO2或NO与溶液中Fe2+或Fe3+发生反应而得到的。为此他利用如图装置(气密性已检验,尾气处理装置略)进行探究。
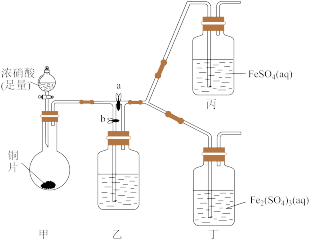
ⅰ.打开活塞a、关闭b,并使甲装置中反应开始后,观察到丙中溶液逐渐变为深棕色,而丁中溶液无明显变化。
ⅱ.打开活塞b、关闭a,一段时间后再停止甲中反应。
ⅲ.为与ⅰ中实验进行对照,更换丙、丁后(溶质不变),使甲中反应继续,观察到的现象与步骤ⅰ中相同。
①铜与足量浓硝酸反应的离子方程式是_______ ;
②装置乙的作用是_______ ;
③步骤ⅱ的目的是_______ ;
④该实验可得出的结论是_______ 。
(1)该同学在实验前,依据Fe2+的
| 实验操作 | 预期现象 | 反应的离子方程式 |
| 向盛有新制FeSO4溶液的试管中滴入数滴浓硝酸,振荡 | 试管中产生红棕色气体,溶液颜色逐渐变黄 | Fe2++ +2H+=Fe3++NO2↑+H2O +2H+=Fe3++NO2↑+H2O |
(2)向原新制FeSO4溶液和反应后溶液中均加入KSCN溶液,前者不变红色,后者(加了数滴浓硝酸的FeSO4溶液)变红。该现象的结论是
(3)该同学通过查阅资料,认为溶液的深棕色可能是NO2或NO与溶液中Fe2+或Fe3+发生反应而得到的。为此他利用如图装置(气密性已检验,尾气处理装置略)进行探究。

ⅰ.打开活塞a、关闭b,并使甲装置中反应开始后,观察到丙中溶液逐渐变为深棕色,而丁中溶液无明显变化。
ⅱ.打开活塞b、关闭a,一段时间后再停止甲中反应。
ⅲ.为与ⅰ中实验进行对照,更换丙、丁后(溶质不变),使甲中反应继续,观察到的现象与步骤ⅰ中相同。
①铜与足量浓硝酸反应的离子方程式是
②装置乙的作用是
③步骤ⅱ的目的是
④该实验可得出的结论是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】高纯度硝酸高铈铵主要用作有机合成的催化剂和氧化剂、集成电路的腐蚀剂等。它的化学式为(NH4)2[Ce(NO3)6] ,是一种橙红色单斜细粒结晶,易溶于水,几乎不溶于浓硝酸。实验室由9.99%的碳酸铈制备硝酸高铈铵时的主要步骤如下:
I.取适量碳酸铈[Ce2(CO3)3]于铂皿中,用硝酸溶解,配成一定浓度的硝酸铈溶液,过滤后待用。在搅拌条件下,向硝酸铈溶液中加入双氧水、氨水进行氧化沉淀,加热后过滤、洗涤、烘干得到Ce(OH)4(黄色难溶物)。
II.将Ce(OH)4于一定温度下加入硝酸加热至浆状,生成H2[Ce(NO3)6],再加入稍过量的NH4NO3晶体,二者反应生成硝酸高铈铵沉淀,经过滤、洗涤、自然烘干后得到产品。
回答下列问题:
(1)①步骤I中使用铂皿而不使用铁质容器的原因是___________ ,写出生成Ce(OH)4的离子方程式:___________ 。
②步骤I中进行“氧化沉淀”时,加热的温度不宜过高,原因是___________ 。
(2)步骤I中的Ce(OH)4在实验室中可由Ce(OH)3制取,某同学设计了如下装置: 。
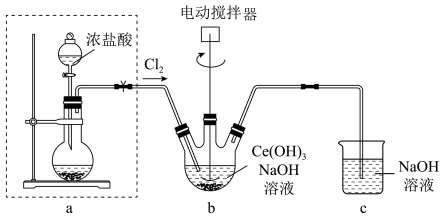
①装置a圆底烧瓶中盛放的固体药品为___________ (填化学式)。
②当装置b中沉淀完全变为黄色后,停止通Cl2后改通空气(图中框内改为通空气装置)的目的是_____ ;将装置b中的反应混合物过滤、洗涤,能说明沉淀已洗涤干净的实验方法是___________ 。
(3)步骤II中H2[Ce(NO3)6]与NH4NO3反应的化学方程式为___________ 。
I.取适量碳酸铈[Ce2(CO3)3]于铂皿中,用硝酸溶解,配成一定浓度的硝酸铈溶液,过滤后待用。在搅拌条件下,向硝酸铈溶液中加入双氧水、氨水进行氧化沉淀,加热后过滤、洗涤、烘干得到Ce(OH)4(黄色难溶物)。
II.将Ce(OH)4于一定温度下加入硝酸加热至浆状,生成H2[Ce(NO3)6],再加入稍过量的NH4NO3晶体,二者反应生成硝酸高铈铵沉淀,经过滤、洗涤、自然烘干后得到产品。
回答下列问题:
(1)①步骤I中使用铂皿而不使用铁质容器的原因是
②步骤I中进行“氧化沉淀”时,加热的温度不宜过高,原因是
(2)步骤I中的Ce(OH)4在实验室中可由Ce(OH)3制取,某同学设计了如下装置: 。

①装置a圆底烧瓶中盛放的固体药品为
②当装置b中沉淀完全变为黄色后,停止通Cl2后改通空气(图中框内改为通空气装置)的目的是
(3)步骤II中H2[Ce(NO3)6]与NH4NO3反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某化学兴趣小组为验证铜与稀硝酸反应生成的气体是NO,设计了如图甲和图乙两套装置。
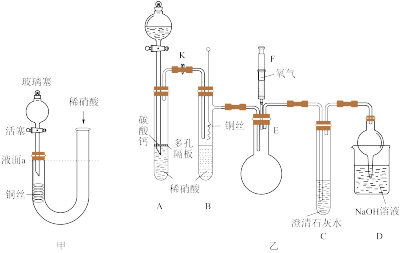
(1)图甲装置中玻璃塞在实验过程中一直处于打开状态。实验过程如下:
①先打开活塞,从右端向U形管中加入稀硝酸至液面a;
②_______ (填实验操作和气体的现象);
③_______ (填实验操作和气体的现象)。
根据实验过程中的现象,证明铜与稀硝酸生成的气体为NO。
(2)用图乙装置进行实验:
①装置E的名称是_______
②B中发生反应的离子方程式是_______
③C中澄清石灰水的作用是_______
④实验过程中通过注射器向装置E中推入氧气(过量),若NaOH过量,实验结束后,D中溶液中含有的阴离子可能有OH−、_______
(3)用图丙装置验证浓硝酸与银反应的产物中是否含有NO。
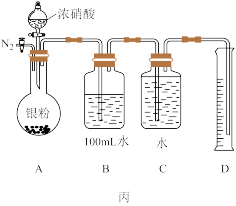
组装好仪器,检验装置气密性,排尽装置中的干扰气体后,向A中滴入适量浓硝酸。实验结束后恢复到室温,B中的溶液体积仍然为100mL,用中和滴定的方法测定B中硝酸浓度为0.04mol/L,量筒D中液体体积为48.0mL(体积已折算为标况)。
试通过计算确定实验中浓硝酸与银反应是否有NO生成_______ (若无NO生成,填“否”,若有NO生成,计算NO的体积为多少,不考虑残留在装置中的气体)。

(1)图甲装置中玻璃塞在实验过程中一直处于打开状态。实验过程如下:
①先打开活塞,从右端向U形管中加入稀硝酸至液面a;
②
③
根据实验过程中的现象,证明铜与稀硝酸生成的气体为NO。
(2)用图乙装置进行实验:
①装置E的名称是
②B中发生反应的离子方程式是
③C中澄清石灰水的作用是
④实验过程中通过注射器向装置E中推入氧气(过量),若NaOH过量,实验结束后,D中溶液中含有的阴离子可能有OH−、
(3)用图丙装置验证浓硝酸与银反应的产物中是否含有NO。

组装好仪器,检验装置气密性,排尽装置中的干扰气体后,向A中滴入适量浓硝酸。实验结束后恢复到室温,B中的溶液体积仍然为100mL,用中和滴定的方法测定B中硝酸浓度为0.04mol/L,量筒D中液体体积为48.0mL(体积已折算为标况)。
试通过计算确定实验中浓硝酸与银反应是否有NO生成
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某化学研究性学习小组利用以下装置制取并探究氨气的性质。在A装置中发生反应的化学方程式为2NH4Cl+Ca(OH)2 CaCl2+2NH3↑+2H2O。
CaCl2+2NH3↑+2H2O。
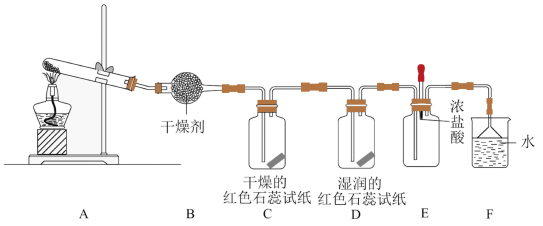
(1)B装置中的干燥剂是_________________ (填“碱石灰”或“浓硫酸”)。
(2)C、D 装置中试纸颜色会发生变化的是___________ (填”C”或“D”)。
(3)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1-2滴浓盐酸,可观察到 E装置中的现象是产生_____________ (填” 白烟”或“白雾”)。
(4)烧杯F中水的作用是________________________ 。
(5)欲制得标准状况下11.2 LNH3,至少需要Ca(OH)2的质量为____________ g。
 CaCl2+2NH3↑+2H2O。
CaCl2+2NH3↑+2H2O。
(1)B装置中的干燥剂是
(2)C、D 装置中试纸颜色会发生变化的是
(3)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1-2滴浓盐酸,可观察到 E装置中的现象是产生
(4)烧杯F中水的作用是
(5)欲制得标准状况下11.2 LNH3,至少需要Ca(OH)2的质量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某同学在实验室探究硝酸的制备和性质,设计了如图所示装置。
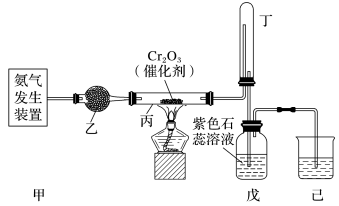
(1)某同学想用下列装置及试剂方便快速地制取少量氨气。
化学试剂:①NH4Cl固体、②浓氨水、③CaO固体。
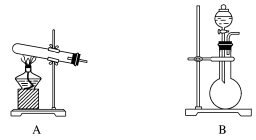
应选择的装置是______ (填字母),选用的试剂是______ (填序号)。
简述快速制取氨气的原理___________ 。
实验过程中,制气时的实验操作是_________ 。
(2)乙装置的作用是______ ;写出受热时丙装置中发生反应的化学方程式:____ 。
(3)当戊中观察到_______ 现象,则说明已制得硝酸。某同学按上图组装仪器并检验装置气密性后进行实验,没有观察到此现象,请分析实验失败的可能原因是:____ ,如何改进装置:___________ 。
(4)改进后待反应结束,将丁装置倒立在盛水的水槽中,会观察到的现象是_____ 。

(1)某同学想用下列装置及试剂方便快速地制取少量氨气。
化学试剂:①NH4Cl固体、②浓氨水、③CaO固体。

应选择的装置是
简述快速制取氨气的原理
实验过程中,制气时的实验操作是
(2)乙装置的作用是
(3)当戊中观察到
(4)改进后待反应结束,将丁装置倒立在盛水的水槽中,会观察到的现象是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某校研究性学习小组的同学在学习了氨的性质后讨论:运用类比的思想,既然氨气具有还原性,能否像H2那样还原CuO呢?他们设计实验制取氨气并探究上述问题。请你参与该小组的活动并完成下列研究:
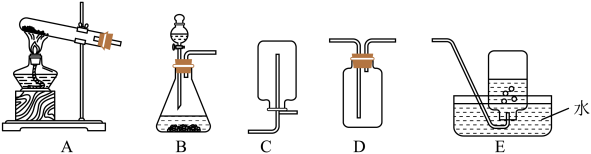
(1)实验室常用加热氯化铵和氢氧化钙固体混合物的方法来制取氨气,该方法制备氨气的装置为_____ (填字母,下同),收集氨气的装置可以是__________ 。
【实验探究】
该小组设计实验探究氨气的还原性及其产物,实验装置图(夹持装置未画出)如下:
(2)通入的NH3必须干燥的原因是__________________ 。
(3)实验中观察到CuO变为红色物质,无水CuSO4变蓝,同时生成一种无污染的气体。请写出NH3与CuO反应的化学方程式:_____________________ 。
【问题讨论】
(4)有同学认为:NH3与CuO反应生成的红色物质中可能含有Cu2O.已知Cu2O是红色粉末,是一种碱性氧化物,在酸性溶液中,Cu+能自身发生氧化还原反应生成Cu2+和Cu。请你设计一个简单的实验检验该红色物质中是否含有Cu2O:____________________ 。
(1)实验室常用加热氯化铵和氢氧化钙固体混合物的方法来制取氨气,该方法制备氨气的装置为
【实验探究】
该小组设计实验探究氨气的还原性及其产物,实验装置图(夹持装置未画出)如下:
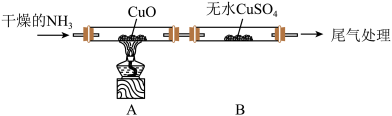
(2)通入的NH3必须干燥的原因是
(3)实验中观察到CuO变为红色物质,无水CuSO4变蓝,同时生成一种无污染的气体。请写出NH3与CuO反应的化学方程式:
【问题讨论】
(4)有同学认为:NH3与CuO反应生成的红色物质中可能含有Cu2O.已知Cu2O是红色粉末,是一种碱性氧化物,在酸性溶液中,Cu+能自身发生氧化还原反应生成Cu2+和Cu。请你设计一个简单的实验检验该红色物质中是否含有Cu2O:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】含氮化合物在工农业有着重要的用途。
(1)氨气的发生装置可以选择上图中的A,反应的化学方程式为___________ 。
(2)请写出氨气的检验方法:___________ 。
Ⅱ. 经一系列反应可以得到
经一系列反应可以得到 。
。
(3)①中, 和
和 在催化剂作用下反应,其化学方程式是
在催化剂作用下反应,其化学方程式是___________ 。
(4)NO的检验方法是:___________ 。
Ⅲ.研究 、
、 、CO等大气污染气体的处理具有重要现实意义。
、CO等大气污染气体的处理具有重要现实意义。
(5)选择性催化还原技术(SCR)可使NOx与 直接反应,实现无害转化。当NO与
直接反应,实现无害转化。当NO与 的物质的量之比为2∶1时,写出发生反应的化学方程式:
的物质的量之比为2∶1时,写出发生反应的化学方程式:___________ 。
(6)大气污染物中的氮氧化物也可用NaOH吸收,先后发生如下反应: ;
; 。若33.6mL(标况下)氮氧化物(只含NO和
。若33.6mL(标况下)氮氧化物(只含NO和 )与VmL
)与VmL NaOH溶液恰好完全反应,则V=
NaOH溶液恰好完全反应,则V=___________ mL。
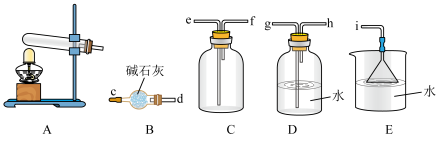
(1)氨气的发生装置可以选择上图中的A,反应的化学方程式为
(2)请写出氨气的检验方法:
Ⅱ.
 经一系列反应可以得到
经一系列反应可以得到 。
。
(3)①中,
 和
和 在催化剂作用下反应,其化学方程式是
在催化剂作用下反应,其化学方程式是(4)NO的检验方法是:
Ⅲ.研究
 、
、 、CO等大气污染气体的处理具有重要现实意义。
、CO等大气污染气体的处理具有重要现实意义。(5)选择性催化还原技术(SCR)可使NOx与
 直接反应,实现无害转化。当NO与
直接反应,实现无害转化。当NO与 的物质的量之比为2∶1时,写出发生反应的化学方程式:
的物质的量之比为2∶1时,写出发生反应的化学方程式:(6)大气污染物中的氮氧化物也可用NaOH吸收,先后发生如下反应:
 ;
; 。若33.6mL(标况下)氮氧化物(只含NO和
。若33.6mL(标况下)氮氧化物(只含NO和 )与VmL
)与VmL NaOH溶液恰好完全反应,则V=
NaOH溶液恰好完全反应,则V=
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】已知有关物质的转化关系如图所示。其中A是常见的气态氢化物,B是能使带火星的木条复燃的无色无味的气体,E的摩尔质量比D大17,G是常见的紫红色金属单质。请回答:
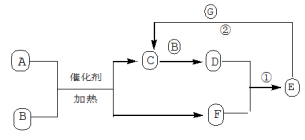
(1)A的电子式为_______ 、B的化学式为_______ 。
(2)A+B→C+F的化学方程式为_______ 。
(3)反应①的离子方程式为_______ ;该反应中氧化剂与还原剂之比为:_______ 。

(1)A的电子式为
(2)A+B→C+F的化学方程式为
(3)反应①的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】已知 A 是单质,A、B、C、D、E 五种物质均含同一种元素,X 是地壳中含量最多的元素形成的单质,相互转化关系如图所示.回答下列问题:
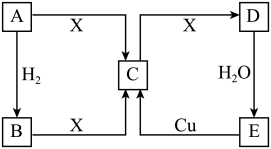
(1)通常情况下,若A为气体,C、D都是大气污染物;
①写出下列反应的化学方程式
B C
C_________________
E C
C_________________
②实验室中检验B的操作方法是_________________ 。
③标准状况下,将盛满D的试管倒扣在盛满水的水槽中,一段时间后,假定溶质不扩散,则试管中所得溶液的物质的量浓度为____________ 。
(2)通常情况下,若A为淡黄色固体:
①写出B与C反应的化学方程式:_______________________ 。
②将C通入溴水中的现象是______ ,发生反应的离子方程式是_______________________ 。

(1)通常情况下,若A为气体,C、D都是大气污染物;
①写出下列反应的化学方程式
B
 C
CE
 C
C②实验室中检验B的操作方法是
③标准状况下,将盛满D的试管倒扣在盛满水的水槽中,一段时间后,假定溶质不扩散,则试管中所得溶液的物质的量浓度为
(2)通常情况下,若A为淡黄色固体:
①写出B与C反应的化学方程式:
②将C通入溴水中的现象是
您最近一年使用:0次



