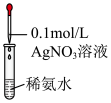
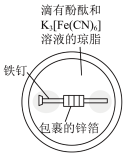
由下列实验事实得出的结论中错误的是
| 选项 | 实验目的 | 实验事实 | 结论 |
| A | 验证牺牲阳极的阴极保护法 | 将锌片与铁片用导线相连,插入酸化的3%NaCl溶液,一段时间后在铁电极区滴入2滴K3[Fe(CN)6]溶液,出现蓝色沉淀 | 铁不一定被腐蚀 |
| B | 麦芽糖水解产物的检验 | 麦芽糖与稀硫酸共热后,加NaOH溶液调至碱性再加入新制Cu(OH)2并加热,有砖红色沉淀生成 | 麦芽糖水解生成葡萄糖 |
| C | 探究Mg和水反应 | 取一小段镁条,用砂纸除去表面氧化膜,放入试管中,加入2mL水,并滴入2滴酚酞溶液,无明显现象;再加热试管至液体沸腾,溶液变红 | Mg可以与热水反应 |
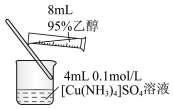
| D | 制备一水合硫酸四氨合铜 | 向[Cu(NH3)4]SO4溶液中加入无水乙醇,并用玻璃棒摩擦试管壁,有深蓝色晶体析出 | 乙醇极性小,降低了[Cu(NH3)4]SO4的溶解度 |
| A.A | B.B | C.C | D.D |
更新时间:2024-05-28 08:33:37
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】对如下装置描述错误的是
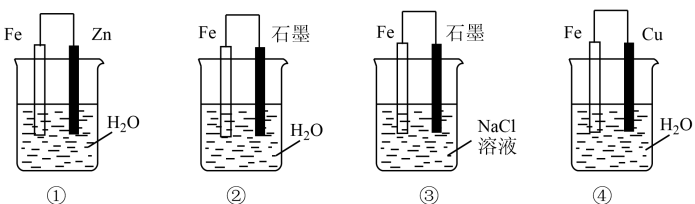

| A.①中的铁被保护 | B.②中铁的腐蚀为吸氧腐蚀 |
| C.③中比②中Fe的腐蚀速率快 | D.④中Cu上的反应式为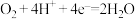 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】化学与生产、生活密切相关。下列说法不正确的是
| A.氨气与氯化氢反应生成氯化铵的过程属于氮的固定 |
| B.煤的气化、煤的液化和煤的干馏均属于化学变化 |
| C.淀粉在稀硫酸催化作用下转化为葡萄糖的过程属于多糖水解 |
| D.将钢铁闸门与电源负极相连的防腐措施属于外加电流保护法 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】能正确表示下列反应的化学方程式是
| A.蔗糖水解方程式:C12H22O11(蔗糖)+H2O→2C6H12O6(葡萄糖) |
B.乙烯通入Br2的CCl4溶液中,橙红色褪去:CH2=CH2+Br2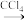 CH2BrCH2Br CH2BrCH2Br |
C.碳酸氢钠溶液与水杨酸反应: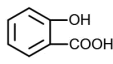 +2HCO +2HCO → → +2H2O+2CO2 +2H2O+2CO2 |
D.AgNO3溶液中加入过量浓氨水:Ag++NH3·H2O=AgOH↓+NH |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列关于糖类的说法中正确的是
| A.葡萄糖能发生酯化反应 |
| B.糖类都能与新制Cu(OH)2反应 |
| C.葡萄糖与果糖是同分异构体,淀粉与纤维素也是同分异构体 |
| D.糖类都能发生水解反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】根据下列实验操作和现象所得到的结论正确的是( )
| 选项 | 实验操作和现象 | 实验结论 |
| A | 将乙醇与浓硫酸混合加热,产生的气体通入酸性KMnO4溶液,溶液紫红色褪去 | 产生的气体中一定含有乙烯 |
| B | 向20%麦芽糖溶液中加入少量稀硫酸,加热,再加入NaOH溶液调至碱性,再加入银氨溶液,水浴加热,出现银镜 | 麦芽糖水解产物具有还原性 |
| C | 取5 mL 0.1 mol·L-1 FeCl3溶液,向其中滴加1 mL 0.1 mol·L-1 KI溶液,取上层清液滴加KSCN溶液,溶液变成血红色 | 该反应是可逆反应 |
| D | 向等体积AgCl与AgBr的饱和溶液中分别加入足量的浓AgNO3溶液,析出沉淀的物质的量AgCl多于AgBr | Ksp(AgCl)>Ksp(AgBr) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列叙述与Mg、Al的金属性无关的是
| A.反应中Al比Mg失去的电子数多 | B.Mg(OH)2的碱性比Al(OH)3的强 |
| C.Mg可将Al2(SO4)3溶液中的Al置换出来 | D.相同大小的Mg、Al与同浓度盐酸反应,Mg反应更剧烈 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列各项正确的是
A.钠与水反应的离子方程式: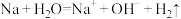 |
B.铁与水蒸气反应的化学方程式: |
| C.镁、铝与沸水不反应 |
| D.金属单质与水反应都生成对应的碱和氢气 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】有四种不同堆积方式的金属晶体的晶胞如图所示,有关说法正确的是

| A.①为简单立方堆积,③为面心立方最密堆积 |
| B.每个晶胞含有的原子数分别为:①1个,②2个,③2个,④4个 |
| C.晶胞中原子的配位数分别为:①6,②8,③8,④12 |
| D.空间利用率的大小关系为:①<②<③<④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】NH3是重要的化工原料,可用于某些配合物的制备,如NiSO4溶于氨水形成[Ni(NH3)6]SO4。工业上常采用氨氧化法制硝酸,其流程是将氨和空气混合后通入灼热的铂铑合金网,反应生成NO(g),生成的一氧化氮与残余的氧气继续反应生成二氧化氮:2NO(g)+O2(g)=2NO2(g);ΔH=-116.4kJ·mol-1。随后将二氧化氮通入水中制取硝酸。工业上一般用石灰乳吸收硝酸工业尾气(NO和NO2),由于NO不能被碱吸收,一般控制NO和NO2约为1∶1通入石灰乳,净化尾气的同时又可制得混凝土添加剂Ca(NO2)2。下列有关[Ni(NH3)6]SO4的说法正确的是
| A.配体为NH3,其空间构型为平面三角形 |
| B.1mol[Ni(NH3)6]2+中σ键的数目为18mol |
| C.[Ni(NH3)6]2+中H—N—H的键角大于NH3中的键角 |
| D.由于[Ni(NH3)6]SO4是配合物,故向其中滴加BaCl2溶液不会生成沉淀 |
您最近一年使用:0次

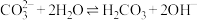
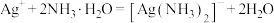


 是否沉淀完全
是否沉淀完全