A、B、C是与生命运动密切相关的三种化合物,它们所含的元素不超过三种,并有下列转化关系:
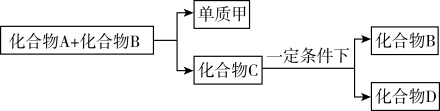
其中化合物D也是日常生活中常见的化合物,在一定条件下可与单质甲进一步发生如下变化:
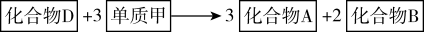
回答下列有关问题:
(1)在A、B、C、D四种化合物中,所含元素相同的是_______ 、_______ (填物质名称)。
(2)常温下,A和B是通过什么途径转化为C的?_______ 。
(3)目前,化合物B在自然界中的含量呈上升趋势,对环境产生了不良的影响,发生这种变化的主要原因是_______ 。
(4)化合物D另有一种同分异构体,这种同分异构体的结构简式是_______ 。

其中化合物D也是日常生活中常见的化合物,在一定条件下可与单质甲进一步发生如下变化:
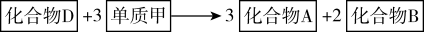
回答下列有关问题:
(1)在A、B、C、D四种化合物中,所含元素相同的是
(2)常温下,A和B是通过什么途径转化为C的?
(3)目前,化合物B在自然界中的含量呈上升趋势,对环境产生了不良的影响,发生这种变化的主要原因是
(4)化合物D另有一种同分异构体,这种同分异构体的结构简式是
14-15高二上·吉林·期中 查看更多[5]
(已下线)2014-2015学年吉林市一中高二上学期期中考试化学卷2015届四川省成都市高三4月模拟考理综化学试卷2015届浙江省宁波市高三4月模拟练习化学试卷鲁教版2018-2019学年高一化学必修二第3章 重要的有机化合物 章末综合检测(已下线)4.1.1 糖类的组成和分类 单糖-2021-2022学年高二化学课后培优练(人教版2019选择性必修3)
更新时间:2016-12-09 06:41:19
|
相似题推荐
解答题-有机推断题
|
适中
(0.65)
名校
【推荐1】某制糖厂以甘蔗为原料制糖,并对剩余的甘蔗渣进行综合利用:

回答下列问题:
(1)A的名称是_______ ;检验A水解液中含有B的试剂是_______ 。
(2)下图中仪器a的名称为_______ 。上述流程获得的乙醇纯度一般较低,采用_______ (填操作名称)可提高纯度,实验室进行该操作需用到下列仪器中的_______ (填代号)。

(3)某小组在实验室制取少量乙酸乙酯,装置如图:
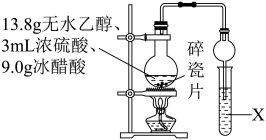
①碎瓷片的作用是_______ ;若加热后发现未加碎瓷片,应采取的措施是_______ (填代号)。
a.立即补加 b.冷却后补加 c.无需补加 d.重新配料
②试管中加入的X试剂为_______ ;球形干燥管除起冷凝作用外,另一重要作用是_______ 。
③反应结束后,下列从混合物中分离出乙酸乙酯的操作错误的是_______ (填代号)。
a.分液漏斗使用前应洗涤干净并检查是否漏水
b.振荡时,分液漏斗下口应向上倾斜
c.振荡过程中,应打开分液漏斗上口玻璃塞放气
d.静置分层后,打开分液漏斗活塞依次从下口放出液体并盛放在不同的烧杯中
④若最终收集到8.8g乙酸乙酯,则产品的产率为_______ (产率 )
)
(4)工业上还可以 为载体、杂多酸金属盐为催化剂,将乙烯和气态乙酸一步反应合成乙酸乙酯,该反应的反应类型为
为载体、杂多酸金属盐为催化剂,将乙烯和气态乙酸一步反应合成乙酸乙酯,该反应的反应类型为_______ 。

回答下列问题:
(1)A的名称是
(2)下图中仪器a的名称为

(3)某小组在实验室制取少量乙酸乙酯,装置如图:

①碎瓷片的作用是
a.立即补加 b.冷却后补加 c.无需补加 d.重新配料
②试管中加入的X试剂为
③反应结束后,下列从混合物中分离出乙酸乙酯的操作错误的是
a.分液漏斗使用前应洗涤干净并检查是否漏水
b.振荡时,分液漏斗下口应向上倾斜
c.振荡过程中,应打开分液漏斗上口玻璃塞放气
d.静置分层后,打开分液漏斗活塞依次从下口放出液体并盛放在不同的烧杯中
④若最终收集到8.8g乙酸乙酯,则产品的产率为
 )
)(4)工业上还可以
 为载体、杂多酸金属盐为催化剂,将乙烯和气态乙酸一步反应合成乙酸乙酯,该反应的反应类型为
为载体、杂多酸金属盐为催化剂,将乙烯和气态乙酸一步反应合成乙酸乙酯,该反应的反应类型为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】以淀粉为原料合成具有水果香味的物质E(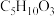 )和F(
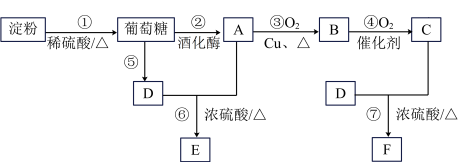
)和F(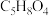 )的合成路线如下图所示。已知D分子中含有一个甲基(
)的合成路线如下图所示。已知D分子中含有一个甲基( ),在哺乳动物体内或自然界中都可最终降解为
),在哺乳动物体内或自然界中都可最终降解为 和
和 。
。
(1)F的结构简式为___________ ,D中含有的官能团名称为___________ ,纯净的C俗称为___________ 。
(2)反应②的化学方程式为___________ 。
(3)反应⑥的化学方程式为___________ ,反应类型为___________ 。
(4)检验反应①中淀粉是否水解的操作为___________ 。
(5)物质G是A的同系物,其分子式为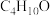 ,G的同分异构体有
,G的同分异构体有___________ 种,其中不能发生催化氧化反应的同分异构体的结构简式为___________ 。
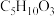 )和F(
)和F(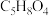 )的合成路线如下图所示。已知D分子中含有一个甲基(
)的合成路线如下图所示。已知D分子中含有一个甲基( ),在哺乳动物体内或自然界中都可最终降解为
),在哺乳动物体内或自然界中都可最终降解为 和
和 。
。
(1)F的结构简式为
(2)反应②的化学方程式为
(3)反应⑥的化学方程式为
(4)检验反应①中淀粉是否水解的操作为
(5)物质G是A的同系物,其分子式为
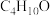 ,G的同分异构体有
,G的同分异构体有
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】某同学称取9 g淀粉溶于水,测定淀粉的水解百分率。其程序如下:
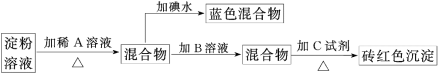
(1)各步加入的试剂为(写化学式):A________ 、B________ 、C________ 。
(2)若加入A溶液不加入B溶液_______ (填“是”或“否”)合理,其理由是_______________ 。
(3)已知1 mol葡萄糖与新制Cu(OH)2悬浊液反应生成1 mol Cu2O,当生成1.44 g砖红色沉淀时,淀粉的水解率是________ 。
(4)某淀粉的相对分子质量为13 932,则它是由________ 个葡萄糖分子缩合而成的。

(1)各步加入的试剂为(写化学式):A
(2)若加入A溶液不加入B溶液
(3)已知1 mol葡萄糖与新制Cu(OH)2悬浊液反应生成1 mol Cu2O,当生成1.44 g砖红色沉淀时,淀粉的水解率是
(4)某淀粉的相对分子质量为13 932,则它是由
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C是与植物生命活动密切相关的三种常见化合物,每种物质所含元素种类均不超过三种,甲是单质,有机物D也是生活中常见的物质,在一定条件下可发生如下反应: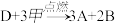 。它们之间有如图所示的转化关系:
。它们之间有如图所示的转化关系:
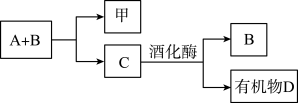
(1)在化合物A、B、C、D中所含元素种类完全相同的是________ (填序号,下同)和________ 。
(2)在常温下,A和B通过________ 转化为C。该过程中________ 能转化为________ 能。
(3)写出由C生成D的化学方程式:________________ 。
(4)目前化合物B在大气中的含量呈上升趋势,其对环境造成的影响是________________ 。
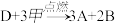 。它们之间有如图所示的转化关系:
。它们之间有如图所示的转化关系:
(1)在化合物A、B、C、D中所含元素种类完全相同的是
(2)在常温下,A和B通过
(3)写出由C生成D的化学方程式:
(4)目前化合物B在大气中的含量呈上升趋势,其对环境造成的影响是
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
【推荐2】以淀粉或以石油裂解产物F(其产量常用来衡量一个国家的石油化工发展水平)为原料制备一种具有果香味的物质E的生产流程如下。
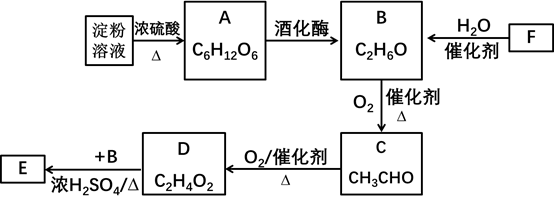
请回答下列问题:
(1)淀粉的化学式为_______ 。
(2)写出F→B反应的化学方程式:_______ 。
(3)写出A→B反应的化学方程式:_______ 。

请回答下列问题:
(1)淀粉的化学式为
(2)写出F→B反应的化学方程式:
(3)写出A→B反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】葡萄是一种常见水果,可以生食或制作葡萄干,除此之外,葡萄还可用于酿酒。
(1)检验葡萄汁含有葡萄糖的方法是:向其中加碱调至碱性,再加入新制的Cu(OH)2并加热,其现象是________ 。
(2)葡萄在酿酒过程中,葡萄糖转化为酒精的过程如下,补充完成下列化学方程式:C6H12O6(葡萄糖) 2
2_________ + 2 C2H5OH
(3)葡萄酒密封储存过程中会生成有香味的酯类,酯类也可以通过化学实验来制备,实验室可用如图所示装置制备乙酸乙酯:
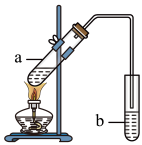
①试管a中生成乙酸乙酯的化学方程式是__________ 。
②试管b中盛放的试剂是饱和____________ 溶液。
③实验开始时,试管b中的导管不伸入液面下的原因是________ 。
④若要分离出试管b中的乙酸乙酯,需要用到的仪器是_______ (填字母)。
A.普通漏斗 B.分液漏斗 C.长颈漏斗
(1)检验葡萄汁含有葡萄糖的方法是:向其中加碱调至碱性,再加入新制的Cu(OH)2并加热,其现象是
(2)葡萄在酿酒过程中,葡萄糖转化为酒精的过程如下,补充完成下列化学方程式:C6H12O6(葡萄糖)
 2
2(3)葡萄酒密封储存过程中会生成有香味的酯类,酯类也可以通过化学实验来制备,实验室可用如图所示装置制备乙酸乙酯:

①试管a中生成乙酸乙酯的化学方程式是
②试管b中盛放的试剂是饱和
③实验开始时,试管b中的导管不伸入液面下的原因是
④若要分离出试管b中的乙酸乙酯,需要用到的仪器是
A.普通漏斗 B.分液漏斗 C.长颈漏斗
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】汽车等交通工具为出行、物流带来方便。然而燃油车排放的尾气中含有大量有害物质,对人体和环境造成危害。
(1)汽油在不同空燃比(空气与燃油气的体积比)时尾气的主要成分不同,空燃比较小的时候有毒气体主要是___________ 。
(2)辛烷(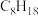 )是汽油的主要成分之一,已知辛烷的燃烧热
)是汽油的主要成分之一,已知辛烷的燃烧热 ,请写出表示辛烷燃烧热的热化学方程式
,请写出表示辛烷燃烧热的热化学方程式___________ 。
(3)空气中的氮气和氧气在气缸内高温环境下,通过电火花放电生成有毒气体NO,反应的热化学方程式为: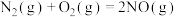
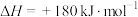 。已知:
。已知: 、
、 分子中化学键的键能分别为946kJ/mol、497 kJ/mol,则NO分子中化学键的键能为
分子中化学键的键能分别为946kJ/mol、497 kJ/mol,则NO分子中化学键的键能为___________ 。
(4)为减轻污染,现在汽车上都安装三元催化转化器,可实现反应: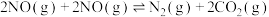
 ,该反应在
,该反应在___________ (填“高温”、“低温”或“任意温度”)下能自发进行。
(1)汽油在不同空燃比(空气与燃油气的体积比)时尾气的主要成分不同,空燃比较小的时候有毒气体主要是
(2)辛烷(
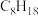 )是汽油的主要成分之一,已知辛烷的燃烧热
)是汽油的主要成分之一,已知辛烷的燃烧热 ,请写出表示辛烷燃烧热的热化学方程式
,请写出表示辛烷燃烧热的热化学方程式(3)空气中的氮气和氧气在气缸内高温环境下,通过电火花放电生成有毒气体NO,反应的热化学方程式为:
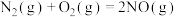
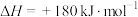 。已知:
。已知: 、
、 分子中化学键的键能分别为946kJ/mol、497 kJ/mol,则NO分子中化学键的键能为
分子中化学键的键能分别为946kJ/mol、497 kJ/mol,则NO分子中化学键的键能为(4)为减轻污染,现在汽车上都安装三元催化转化器,可实现反应:
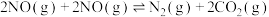
 ,该反应在
,该反应在
您最近一年使用:0次
【推荐2】化学既能指导人们科学生活,也能指导人们治理环境污染等。
(1)没有擦干的铸铁锅易生锈,是因为发生了______________ (填“吸氧”或“析氢”)腐蚀。
(2)下列金属的防护方法中,正确的是_____________ (填字母)。
A.在铁制的下水道上焊上铜块
B.衣架和电线的外面包上一层塑料层
C.在自行车的钢圈上刷油漆,以防生锈
(3)汽车尾气中含有CO和NO等有毒气体,在催化剂的作用下,使CO和NO反应转化成 和一种无毒的单质气体,该反应的化学方程式是
和一种无毒的单质气体,该反应的化学方程式是__________________________ 。
(4)钢铁厂、电镀厂在生产过程中会产生酸性废水,一般用_____________(填字母)来进行中和处理。
(5)近几年冬季,雾霾天气有所减少.导致雾霾出现的主要原因是____________ (填字母)。
A. B.
B. C.PM2.5
C.PM2.5
(6)垃圾的再生利用是垃圾资源化的最佳途径,以下垃圾处理方法中正确的是_____________(填字母)。
(1)没有擦干的铸铁锅易生锈,是因为发生了
(2)下列金属的防护方法中,正确的是
A.在铁制的下水道上焊上铜块
B.衣架和电线的外面包上一层塑料层
C.在自行车的钢圈上刷油漆,以防生锈
(3)汽车尾气中含有CO和NO等有毒气体,在催化剂的作用下,使CO和NO反应转化成
 和一种无毒的单质气体,该反应的化学方程式是
和一种无毒的单质气体,该反应的化学方程式是(4)钢铁厂、电镀厂在生产过程中会产生酸性废水,一般用_____________(填字母)来进行中和处理。
A. | B. | C. | D. |
A.
 B.
B. C.PM2.5
C.PM2.5(6)垃圾的再生利用是垃圾资源化的最佳途径,以下垃圾处理方法中正确的是_____________(填字母)。
| A.废旧电池无须处理,集中深埋即可 | B.厨余垃圾直接倒入下水道 |
| C.废旧玻璃可回收熔炼,再生利用 | D.废旧纸张可直接露天焚烧 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.氮元素在地球上含量丰富,氮及其化合物在工农业生产和生活中有着重要作用,氮氧化物也是主要的大气污染物。
(1)汽车尾气中的NO和CO气体,可以利用催化剂转化为对环境无害的两种气体,请写出该过程的化学方程式___________ ;
(2)含有NO和NO2的工业尾气可以利用NaOH溶液吸收处理。主要反应为NO+NO2+2OH-=2NO +H2O、2NO2+2OH-=NO
+H2O、2NO2+2OH-=NO +NO
+NO +H2O。
+H2O。
①下列措施不能提高尾气中NO和NO2去除率的有___________ (填标号)。
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气的过程中定期补加适量NaOH溶液
D.将尾气通入NaOH溶液的同时通入氧气
②若将NO和NO2组成的混合气体通入1L0.5mol/LNaOH溶液中,NaOH和气体恰好完全反应,吸收后的溶液经浓缩、结晶、过滤、洗涤、干燥后,得到晶体36.9g,则原混合气体中NO和NO2的物质的量之比为___________ 。
(3)用HClO也可以吸收工业尾气中的NO,HClO氧化NO生成Cl-和NO ,其离子方程式为
,其离子方程式为___________ 。
Ⅱ.该研究性学习小组同学还认为NO易与O2发生反应,应该更易被氧化。查阅资料:2NO+Na2O2=2NaNO2;2NaNO2+2HCl=2NaCl+NO2↑+NO↑+H2O;酸性条件下,NO能与MnO 反应生成NO
反应生成NO 和Mn2+。
和Mn2+。
(4)丙同学用下图所示装置(部分夹持装置略)探究NO与Na2O2的反应。___________ ;
②C中所装试剂可以是___________ ;
③充分反应后,检验D装置中产物的方法是:取D装置中产物少许,___________ ,则产物是NaNO2。
(1)汽车尾气中的NO和CO气体,可以利用催化剂转化为对环境无害的两种气体,请写出该过程的化学方程式
(2)含有NO和NO2的工业尾气可以利用NaOH溶液吸收处理。主要反应为NO+NO2+2OH-=2NO
 +H2O、2NO2+2OH-=NO
+H2O、2NO2+2OH-=NO +NO
+NO +H2O。
+H2O。①下列措施不能提高尾气中NO和NO2去除率的有
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气的过程中定期补加适量NaOH溶液
D.将尾气通入NaOH溶液的同时通入氧气
②若将NO和NO2组成的混合气体通入1L0.5mol/LNaOH溶液中,NaOH和气体恰好完全反应,吸收后的溶液经浓缩、结晶、过滤、洗涤、干燥后,得到晶体36.9g,则原混合气体中NO和NO2的物质的量之比为
(3)用HClO也可以吸收工业尾气中的NO,HClO氧化NO生成Cl-和NO
 ,其离子方程式为
,其离子方程式为Ⅱ.该研究性学习小组同学还认为NO易与O2发生反应,应该更易被氧化。查阅资料:2NO+Na2O2=2NaNO2;2NaNO2+2HCl=2NaCl+NO2↑+NO↑+H2O;酸性条件下,NO能与MnO
 反应生成NO
反应生成NO 和Mn2+。
和Mn2+。(4)丙同学用下图所示装置(部分夹持装置略)探究NO与Na2O2的反应。
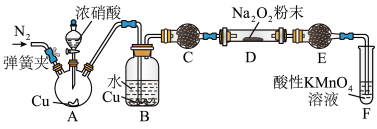
②C中所装试剂可以是
③充分反应后,检验D装置中产物的方法是:取D装置中产物少许,
您最近一年使用:0次



