实验室需要0.5 mol·L-1硫酸溶液450 mL。可供选择的仪器有:
①玻璃棒 ②烧瓶 ③烧杯 ④胶头滴管 ⑤量筒 ⑥容量瓶 ⑦托盘天平 ⑧分液漏斗
实验室现有质量分数为98%、密度为1.84 g·cm-3的浓H2SO4提供,根据这种溶液的配制情况回答下列问题:
(1)上述仪器中,一直用不到的有___________ (填序号)。
(2)下列操作中,容量瓶不具备的功能有___________ (填序号)。
A.配制一定体积准确浓度的标准溶液
B.长期贮存溶液
C.用来加热溶解固体溶质
D.作为反应容器
(3)配制时应量取浓硫酸___________ mL。
(4)实验中,玻璃棒的作用有___________ 。
(5)配制溶液时,下列操作中引起误差偏高的有___________ 。(填序号)
①洗涤量取浓H2SO4后的量筒,并将洗涤液转移到容量瓶中
②未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
③将溶液转移至容量瓶后,未洗涤烧杯和玻璃棒
④定容时,加蒸馏水超过标线,又用胶头滴管吸出
⑤定容时,仰视标线
①玻璃棒 ②烧瓶 ③烧杯 ④胶头滴管 ⑤量筒 ⑥容量瓶 ⑦托盘天平 ⑧分液漏斗
实验室现有质量分数为98%、密度为1.84 g·cm-3的浓H2SO4提供,根据这种溶液的配制情况回答下列问题:
(1)上述仪器中,一直用不到的有
(2)下列操作中,容量瓶不具备的功能有
A.配制一定体积准确浓度的标准溶液
B.长期贮存溶液
C.用来加热溶解固体溶质
D.作为反应容器
(3)配制时应量取浓硫酸
(4)实验中,玻璃棒的作用有
(5)配制溶液时,下列操作中引起误差偏高的有
①洗涤量取浓H2SO4后的量筒,并将洗涤液转移到容量瓶中
②未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
③将溶液转移至容量瓶后,未洗涤烧杯和玻璃棒
④定容时,加蒸馏水超过标线,又用胶头滴管吸出
⑤定容时,仰视标线
更新时间:2016-12-09 06:59:33
|
相似题推荐
解答题-实验探究题
|
适中
(0.64)
【推荐1】实验室用密度为1.84g/mL质量分数为98%的浓H2SO4来配制100mL 3.0mol•L﹣1稀H2SO4溶液,请回答下列问题:
(1)计算所需浓H2SO4体积为_______
(2)量取所需浓H2SO4,应选用_______ 量筒(选填5mL、10mL、20mL)。
(3)稀释浓H2SO4的方法(简要操作)_______
(4)配制所需仪器,除量筒和胶头滴管外,还必须用到的玻璃仪器有_______
(5)定容时的正确操作方法是:_______
(6)下列操作结果使溶液物质的量浓度偏高的是_______
A.没有将洗涤液转入容量瓶中B.容量瓶用蒸馏水洗涤后,未干燥
C.定容时,俯视容量瓶的刻度线D.加水定容时,加水超过了刻度线
E.浓H2SO4稀释后立即转移至容量瓶中并定容.
(1)计算所需浓H2SO4体积为
(2)量取所需浓H2SO4,应选用
(3)稀释浓H2SO4的方法(简要操作)
(4)配制所需仪器,除量筒和胶头滴管外,还必须用到的玻璃仪器有
(5)定容时的正确操作方法是:
(6)下列操作结果使溶液物质的量浓度偏高的是
A.没有将洗涤液转入容量瓶中B.容量瓶用蒸馏水洗涤后,未干燥
C.定容时,俯视容量瓶的刻度线D.加水定容时,加水超过了刻度线
E.浓H2SO4稀释后立即转移至容量瓶中并定容.
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】实验室用固体烧碱配制0.5mol/L的NaOH溶液490mL,用质量分数为98%,密度为1.84 g/cm3的浓硫酸配制0.6mol/L的硫酸溶液500mL。请回答下列问题:
(1)计算需要NaOH固体质量_________ g。
(2)有以下仪器:①烧杯 ②药匙 ③250mL容量瓶 ④500mL容量瓶 ⑤玻璃棒⑥托盘天平 ⑦量筒。配制以上两种溶液必须使用的玻璃仪器_________ (填序号),还缺少的仪器是_________ 。
(3)定容的具体操作方法是:________
(4)根据计算得知,需用量筒量取质量分数为98%、密度为1.84g/cm3的浓硫酸的体积为______ mL,如果实验室有15mL、20mL、50mL量筒,应选用__________ mL量筒最好。
(5)配制过程中,下列操作会引起结果偏高的是__________ (填序号)
①未洗涤烧杯、玻璃棒
②称量NaOH的时间太长
③定容时俯视刻度
④容量瓶不干燥,含有少量蒸馏水
⑤NaOH溶液未冷却至室温就转移到容量瓶
⑥量取浓硫酸时,仰视量筒刻度线
(1)计算需要NaOH固体质量
(2)有以下仪器:①烧杯 ②药匙 ③250mL容量瓶 ④500mL容量瓶 ⑤玻璃棒⑥托盘天平 ⑦量筒。配制以上两种溶液必须使用的玻璃仪器
(3)定容的具体操作方法是:
(4)根据计算得知,需用量筒量取质量分数为98%、密度为1.84g/cm3的浓硫酸的体积为
(5)配制过程中,下列操作会引起结果偏高的是
①未洗涤烧杯、玻璃棒
②称量NaOH的时间太长
③定容时俯视刻度
④容量瓶不干燥,含有少量蒸馏水
⑤NaOH溶液未冷却至室温就转移到容量瓶
⑥量取浓硫酸时,仰视量筒刻度线
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.为则定Na2CO3和NaHCO3混合样品中Na2CO3的含量。甲同学通过加热固体样品中碳酸氢钠分解得到的CO2质量进行计算,设计实验装置示意图如下:
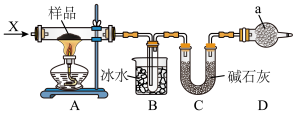
(1)装置A中发生反应的化学方程式_______ 。
(2)装置B中冰水的作用是_______ 。
(3)仪器a的名称是_______ 。装置D的作用_______ 。
(4)该同学设计的实验装置存在缺陷,有关该实验装置及实验过程中,下列因素可能使碳酸钠的含量偏高的是_______ 。
a.装置A样品分解不完全
b.B、C之间缺少CO2的干燥装置
c.产生CO2气体的速率太快,没有被碱石灰完全吸收
d.反应完全后停止加热,通入过量的空气
(5)下列实验方案中,不能测定Na2CO3和NaHCO3混合物中Na2CO3质量分数的是_______ 。
A.取m克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重n克
B.取m克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得n克固体
C.取m克混合物充分加热,减重n克
D.取m克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得n克固体
Ⅱ.乙同学通过样品溶液与稀盐酸反应得到的CO2体积进行计算,加入稀盐酸的体积与标准状况下产生气体体积的关系如下图所示。
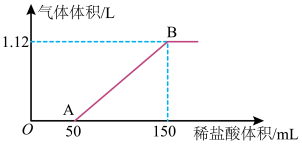
(6)稀盐酸的物质的量浓度_______ 。
(7)样品中Na2CO3和NaHCO3的物质的量之比_______ 。

(1)装置A中发生反应的化学方程式
(2)装置B中冰水的作用是
(3)仪器a的名称是
(4)该同学设计的实验装置存在缺陷,有关该实验装置及实验过程中,下列因素可能使碳酸钠的含量偏高的是
a.装置A样品分解不完全
b.B、C之间缺少CO2的干燥装置
c.产生CO2气体的速率太快,没有被碱石灰完全吸收
d.反应完全后停止加热,通入过量的空气
(5)下列实验方案中,不能测定Na2CO3和NaHCO3混合物中Na2CO3质量分数的是
A.取m克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重n克
B.取m克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得n克固体
C.取m克混合物充分加热,减重n克
D.取m克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得n克固体
Ⅱ.乙同学通过样品溶液与稀盐酸反应得到的CO2体积进行计算,加入稀盐酸的体积与标准状况下产生气体体积的关系如下图所示。

(6)稀盐酸的物质的量浓度
(7)样品中Na2CO3和NaHCO3的物质的量之比
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
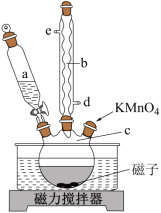
【推荐1】氧化石墨烯具有稳定的网状结构,在能源、材料等领域有着重要的应用前景,通过氧化剥离石墨制备氧化石墨烯的一种方法如下(装置如图所示): 、
、 、石墨粉末在c中混合,置于冰水浴中,剧烈搅拌下,分批缓慢加入
、石墨粉末在c中混合,置于冰水浴中,剧烈搅拌下,分批缓慢加入 粉末,塞好瓶口。
粉末,塞好瓶口。
Ⅱ.转至油浴中,35℃搅拌1小时,缓慢滴加一定量的蒸馏水。升温至98℃并保持1小时。
Ⅲ.转移至大烧杯中,静置冷却至室温。加入大量蒸馏水,而后滴加 至悬浊液由紫色变为土黄色。
至悬浊液由紫色变为土黄色。
Ⅳ.离心分离,稀盐酸洗涤沉淀。
Ⅴ.蒸馏水洗涤沉淀。
Ⅵ.冷冻干燥,得到土黄色的氧化石墨烯。
回答下列问题:
(1)步骤Ⅰ中,需分批缓慢加入 粉末并使用冰水浴,原因是
粉末并使用冰水浴,原因是_______ 。
(2)步骤Ⅱ中的加热方式采用油浴,不使用热水浴,原因是_______ 。
 、
、 、石墨粉末在c中混合,置于冰水浴中,剧烈搅拌下,分批缓慢加入
、石墨粉末在c中混合,置于冰水浴中,剧烈搅拌下,分批缓慢加入 粉末,塞好瓶口。
粉末,塞好瓶口。Ⅱ.转至油浴中,35℃搅拌1小时,缓慢滴加一定量的蒸馏水。升温至98℃并保持1小时。
Ⅲ.转移至大烧杯中,静置冷却至室温。加入大量蒸馏水,而后滴加
 至悬浊液由紫色变为土黄色。
至悬浊液由紫色变为土黄色。Ⅳ.离心分离,稀盐酸洗涤沉淀。
Ⅴ.蒸馏水洗涤沉淀。
Ⅵ.冷冻干燥,得到土黄色的氧化石墨烯。
回答下列问题:
(1)步骤Ⅰ中,需分批缓慢加入
 粉末并使用冰水浴,原因是
粉末并使用冰水浴,原因是(2)步骤Ⅱ中的加热方式采用油浴,不使用热水浴,原因是
您最近半年使用:0次
【推荐2】已知三氯化铁的熔点为306℃,沸点为315℃,易溶于水并且有强烈的吸水性,能吸收空气里的水分而潮解,并可作为过氧化氢分解的催化剂。某学习小组的同学对氯气与铁的反应及产物做了如图探究实验:

(1)装碱石灰的仪器名称是____ 。
(2)碱石灰的作用是____ 。
(3)本实验中,装置从左向右合理的连接顺序为:____
a→__________→__________→__________→__________→__________→__________→__________。
(4)反应一段时间后熄灭酒精灯,冷却后将硬质玻璃管及收集器中的物质一并快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(反应过程中不振荡)。充分反应后,进行如图实验:
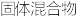








已知红色褪去的同时有气体生成,经检验为O2。
该小组内的同学们对红色褪去的原因提出了三种假设:
假设Ⅰ:H2O2还原Fe3+,使其转变为Fe2+;
假设Ⅱ:H2O2分解生成O2,O2氧化试剂X;
假设Ⅲ:____ 。
并对假设进行了以下实验探究:
实验①:取褪色后溶液三份,第一份滴加FeCl3溶液无明显变化;第二份滴加试剂X,溶液出现红色;第三份滴加稀盐酸和BaCl2溶液,产生白色沉淀。
实验②:另取同浓度的FeCl3溶液滴加2滴试剂X,溶液变红,再通入O2,无明显变化。
回答下列问题:实验①说明假设____ 不正确;实验②的目的是____ ;由实验①②得出假设____ 是正确的。

(1)装碱石灰的仪器名称是
(2)碱石灰的作用是
(3)本实验中,装置从左向右合理的连接顺序为:
a→__________→__________→__________→__________→__________→__________→__________。
(4)反应一段时间后熄灭酒精灯,冷却后将硬质玻璃管及收集器中的物质一并快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(反应过程中不振荡)。充分反应后,进行如图实验:
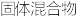








已知红色褪去的同时有气体生成,经检验为O2。
该小组内的同学们对红色褪去的原因提出了三种假设:
假设Ⅰ:H2O2还原Fe3+,使其转变为Fe2+;
假设Ⅱ:H2O2分解生成O2,O2氧化试剂X;
假设Ⅲ:
并对假设进行了以下实验探究:
实验①:取褪色后溶液三份,第一份滴加FeCl3溶液无明显变化;第二份滴加试剂X,溶液出现红色;第三份滴加稀盐酸和BaCl2溶液,产生白色沉淀。
实验②:另取同浓度的FeCl3溶液滴加2滴试剂X,溶液变红,再通入O2,无明显变化。
回答下列问题:实验①说明假设
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】通常二价铬的化合物非常不稳定,在空气中迅速被氧化为三价铬,只有 的卤素化合物、磷酸盐、碳酸盐和醋酸盐可存在于干燥状态。
的卤素化合物、磷酸盐、碳酸盐和醋酸盐可存在于干燥状态。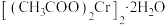 (醋酸亚铬晶体)为红棕色,不溶于冷水和乙醚,微溶于乙醇,能吸收空气中的氧气而变质,需无氧环境制备。实验室可用如图装置在氢气氛围中制备
(醋酸亚铬晶体)为红棕色,不溶于冷水和乙醚,微溶于乙醇,能吸收空气中的氧气而变质,需无氧环境制备。实验室可用如图装置在氢气氛围中制备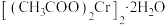 (相对分子质量为376),制备原理如下所示。
(相对分子质量为376),制备原理如下所示。



回答下列问题:
(1)仪器X的名称为___________ ;按图组装好仪器后,应先进行的操作为___________ 。
(2)制备醋酸亚铬时,仪器X中盛放用去氧水配制的醋酸钠溶液,抽滤瓶中放入4.8g锌粒(过量),3.0g (相对分子质量为266.5),3.0mL去氧水,摇动抽滤瓶得到深绿色混合物,再迅速加入3.0mL浓盐酸,立即用胶塞密封。慢慢摇动抽滤瓶,直至
(相对分子质量为266.5),3.0mL去氧水,摇动抽滤瓶得到深绿色混合物,再迅速加入3.0mL浓盐酸,立即用胶塞密封。慢慢摇动抽滤瓶,直至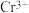 被充分还原为
被充分还原为 。
。
①去氧水由蒸馏水去除溶解氧制得,去除溶解氧常用的物理方法是___________ 法。
②抽滤瓶中加入浓盐酸后能与锌粒反应产生氢气,其目的是___________ 。
③当抽滤瓶中的溶液逐渐从蓝绿色完全变为___________ 色时,可判断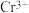 被充分还原为
被充分还原为 。
。
(3)将抽滤瓶中的液体经支管口倾倒进入仪器X中与醋酸钠溶液混合,析出红棕色沉淀,过滤,用冷去氧水洗涤数次,再用无水乙醇洗涤2~3次,最后用___________ 洗涤2~3次;洗涤沉淀的具体操作方法是___________ 。
(4)将滤渣薄薄一层铺在表面皿上,在室温下干燥,称量后密封保存。若所得产物质量为1.5g,则产率为___________ 。
 的卤素化合物、磷酸盐、碳酸盐和醋酸盐可存在于干燥状态。
的卤素化合物、磷酸盐、碳酸盐和醋酸盐可存在于干燥状态。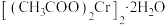 (醋酸亚铬晶体)为红棕色,不溶于冷水和乙醚,微溶于乙醇,能吸收空气中的氧气而变质,需无氧环境制备。实验室可用如图装置在氢气氛围中制备
(醋酸亚铬晶体)为红棕色,不溶于冷水和乙醚,微溶于乙醇,能吸收空气中的氧气而变质,需无氧环境制备。实验室可用如图装置在氢气氛围中制备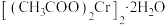 (相对分子质量为376),制备原理如下所示。
(相对分子质量为376),制备原理如下所示。


回答下列问题:
(1)仪器X的名称为
(2)制备醋酸亚铬时,仪器X中盛放用去氧水配制的醋酸钠溶液,抽滤瓶中放入4.8g锌粒(过量),3.0g
 (相对分子质量为266.5),3.0mL去氧水,摇动抽滤瓶得到深绿色混合物,再迅速加入3.0mL浓盐酸,立即用胶塞密封。慢慢摇动抽滤瓶,直至
(相对分子质量为266.5),3.0mL去氧水,摇动抽滤瓶得到深绿色混合物,再迅速加入3.0mL浓盐酸,立即用胶塞密封。慢慢摇动抽滤瓶,直至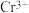 被充分还原为
被充分还原为 。
。①去氧水由蒸馏水去除溶解氧制得,去除溶解氧常用的物理方法是
②抽滤瓶中加入浓盐酸后能与锌粒反应产生氢气,其目的是
③当抽滤瓶中的溶液逐渐从蓝绿色完全变为
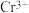 被充分还原为
被充分还原为 。
。(3)将抽滤瓶中的液体经支管口倾倒进入仪器X中与醋酸钠溶液混合,析出红棕色沉淀,过滤,用冷去氧水洗涤数次,再用无水乙醇洗涤2~3次,最后用
(4)将滤渣薄薄一层铺在表面皿上,在室温下干燥,称量后密封保存。若所得产物质量为1.5g,则产率为
您最近半年使用:0次



