实验室用密度为1.84g/mL质量分数为98%的浓H2SO4来配制100mL 3.0mol•L﹣1稀H2SO4溶液,请回答下列问题:
(1)计算所需浓H2SO4体积为_______
(2)量取所需浓H2SO4,应选用_______ 量筒(选填5mL、10mL、20mL)。
(3)稀释浓H2SO4的方法(简要操作)_______
(4)配制所需仪器,除量筒和胶头滴管外,还必须用到的玻璃仪器有_______
(5)定容时的正确操作方法是:_______
(6)下列操作结果使溶液物质的量浓度偏高的是_______
A.没有将洗涤液转入容量瓶中B.容量瓶用蒸馏水洗涤后,未干燥
C.定容时,俯视容量瓶的刻度线D.加水定容时,加水超过了刻度线
E.浓H2SO4稀释后立即转移至容量瓶中并定容.
(1)计算所需浓H2SO4体积为
(2)量取所需浓H2SO4,应选用
(3)稀释浓H2SO4的方法(简要操作)
(4)配制所需仪器,除量筒和胶头滴管外,还必须用到的玻璃仪器有
(5)定容时的正确操作方法是:
(6)下列操作结果使溶液物质的量浓度偏高的是
A.没有将洗涤液转入容量瓶中B.容量瓶用蒸馏水洗涤后,未干燥
C.定容时,俯视容量瓶的刻度线D.加水定容时,加水超过了刻度线
E.浓H2SO4稀释后立即转移至容量瓶中并定容.
更新时间:2016-12-09 11:05:27
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某食用白醋是由醋酸与纯水配制而成,科技活动周中某同学拟用学过的酸碱中和滴定知识来测定其中醋酸的物质的量浓度。已知标准液c(NaOH)=0.1020mol/L。
(1)查阅白醋包装:醋酸含量约为6g/100mL,换算成物质的浓度约为_______  ,滴定前要先将白醋稀释10倍。
,滴定前要先将白醋稀释10倍。
(2)滴定前,有关滴定管的正确操作为(选出正确操作并按序排列):检漏→蒸馏水洗涤→_______ →开始滴定。
A.烘干 B.装入滴定液至零刻度以上 C.调整滴定液液面至零刻度或零刻度以下 D.用洗耳球吹出润洗液 E.排除气泡 F.用滴定液润洗2至3次 G.记录起始读数
(3)准确量取稀释后的白醋25.00mL,置于锥形瓶中,用_______ 作指示剂,当上述NaOH标准溶液滴定至_______ 即为终点。
(4)为了减小实验误差,该同学一共进行了三次实验,三次实验结果记录如下:
从上表可以看出,第一次实验中记录消耗NaOH溶液的体积明显多于后两次,其原因可能是_______。
(5)根据所给数据,计算该品牌白醋中醋酸的物质的量浓度:_______ 。
(1)查阅白醋包装:醋酸含量约为6g/100mL,换算成物质的浓度约为
 ,滴定前要先将白醋稀释10倍。
,滴定前要先将白醋稀释10倍。(2)滴定前,有关滴定管的正确操作为(选出正确操作并按序排列):检漏→蒸馏水洗涤→
A.烘干 B.装入滴定液至零刻度以上 C.调整滴定液液面至零刻度或零刻度以下 D.用洗耳球吹出润洗液 E.排除气泡 F.用滴定液润洗2至3次 G.记录起始读数
(3)准确量取稀释后的白醋25.00mL,置于锥形瓶中,用
(4)为了减小实验误差,该同学一共进行了三次实验,三次实验结果记录如下:
| 滴定次数 | 待测液体积(mL) | 标准NaOH溶液体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 25.00 | 0.50 | 21.40 |
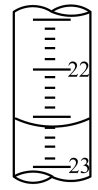
| 第二次 | 25.00 | 2.50 | (见图) |
| 第三次 | 25.00 | 1.20 | 21.10 |

从上表可以看出,第一次实验中记录消耗NaOH溶液的体积明显多于后两次,其原因可能是_______。
| A.滴定前滴定管尖嘴有气泡,滴定结束无气泡 |
| B.盛装标准液的滴定管装液前用蒸馏水润洗过,未用标准液润洗 |
| C.第一次滴定用的锥形瓶未润洗 |
| D.滴定结束时,俯视读数 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】白醋是生活中常见的调味剂之一,国家标准规定,酿造的白醋中醋酸的含量不得低于3.5g/100mL。某化学兴趣小组想要测定某品牌白醋中 的含量,请回答下列问题:
的含量,请回答下列问题:
(1)请写出 在水中电离的方程式:
在水中电离的方程式:_______ 。
(2)甲同学准确量取10.00mL该品牌白醋,用容量瓶配制成100mL稀溶液,下列说法中正确的是_______(填标号)。
(3)乙同学准确量取20.00mL甲同学配制的白醋溶液于锥形瓶中,滴入2滴酚酞溶液,再用 的NaOH标准溶液进行滴定,进行3次平行实验后的情况如下表:
的NaOH标准溶液进行滴定,进行3次平行实验后的情况如下表:
①滴定终点的现象:滴入最后半滴NaOH标准溶液后,锥形瓶内溶液_______ 。
②请在下图中画出该实验的pH-V(NaOH)曲线,并在曲线上用“·”标出滴定终点。__________

③在滴定过程中,下列操作会使测得的白醋中 含量偏高的是
含量偏高的是_______ (填标号)。
A.锥形瓶在使用前用待测的白醋润洗
B.滴定过程中,锥形瓶内有液体溅出
C.滴定前碱式滴定管内有气泡,滴定后气泡消失
D.碱式滴定管在滴定前平视读数,滴定后俯视读数
(4)由滴定结果可知,该品牌白醋中 的含量为
的含量为_______ g/100mL,_______ (填“符合”或“不符合”)国家标准。
 的含量,请回答下列问题:
的含量,请回答下列问题:(1)请写出
 在水中电离的方程式:
在水中电离的方程式:(2)甲同学准确量取10.00mL该品牌白醋,用容量瓶配制成100mL稀溶液,下列说法中正确的是_______(填标号)。
| A.量取白醋所用的酸式滴定管要先用该白醋润洗 |
| B.加入白醋前,容量瓶必须保持干燥,以防产生误差 |
| C.定容时,为防止容量瓶中液体飞溅,胶头滴管应伸进容量瓶中 |
| D.摇匀后,发现容量瓶液面略低于刻度线时,无需进行其他操作 |
 的NaOH标准溶液进行滴定,进行3次平行实验后的情况如下表:
的NaOH标准溶液进行滴定,进行3次平行实验后的情况如下表:| 实验序号 | 量取的白醋体积/mL | 消耗的NaOH标准溶液体积/mL |
| 1 | 20.00 | 19.98 |
| 2 | 20.00 | 20.00 |
| 3 | 20.00 | 20.02 |
②请在下图中画出该实验的pH-V(NaOH)曲线,并在曲线上用“·”标出滴定终点。

③在滴定过程中,下列操作会使测得的白醋中
 含量偏高的是
含量偏高的是A.锥形瓶在使用前用待测的白醋润洗
B.滴定过程中,锥形瓶内有液体溅出
C.滴定前碱式滴定管内有气泡,滴定后气泡消失
D.碱式滴定管在滴定前平视读数,滴定后俯视读数
(4)由滴定结果可知,该品牌白醋中
 的含量为
的含量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】葡萄糖酸钙是一种可促进骨骼生长的营养物质。制取葡萄糖酸钙的流程如图。
葡萄糖溶液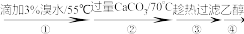 悬浊液
悬浊液 Ca(C6H11O7)2
Ca(C6H11O7)2
已知:a.CH2OH(CHOH)4CHO+Br2+H2O→C6H12O7(葡萄糖酸)+2HBr;
b.2C6H12O7(葡萄糖酸)+CaCO3→Ca(C6H11O7)2(葡萄糖酸钙)+H2O+CO2↑;
c.相关物质的溶解性见表:
d.酸性:盐酸>葡萄糖酸>碳酸。
请回答下列问题:
(1)制备葡萄糖酸钙涉及的反应类型有___ 。
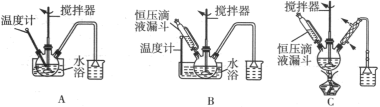
(2)第①步中溴水氧化葡萄糖时,下列装置最合适的是___ (填序号)。
(3)第②步反应CaCO3需过量的原因是____ 。
(4)本实验中不宜用CaCl2替代CaCO3,理由是___ 。
(5)第③步需趁热过滤,其原因是__ 。
(6)若制备时葡萄糖溶液中含有9.0g葡萄糖,步骤⑦后得到8.2g葡萄糖酸钙,则葡萄糖酸钙的产率为___ 。
葡萄糖溶液
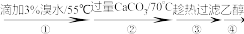 悬浊液
悬浊液 Ca(C6H11O7)2
Ca(C6H11O7)2已知:a.CH2OH(CHOH)4CHO+Br2+H2O→C6H12O7(葡萄糖酸)+2HBr;
b.2C6H12O7(葡萄糖酸)+CaCO3→Ca(C6H11O7)2(葡萄糖酸钙)+H2O+CO2↑;
c.相关物质的溶解性见表:
| 物质名称 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 | 氯化钙 |
| 在水中的溶解性 | 可溶于冷水,易溶于热水 | 可溶 | 易溶 | 易溶 |
| 在乙醇中的溶解性 | 微溶 | 微溶 | 可溶 | 可溶 |
d.酸性:盐酸>葡萄糖酸>碳酸。
请回答下列问题:
(1)制备葡萄糖酸钙涉及的反应类型有
(2)第①步中溴水氧化葡萄糖时,下列装置最合适的是

(3)第②步反应CaCO3需过量的原因是
(4)本实验中不宜用CaCl2替代CaCO3,理由是
(5)第③步需趁热过滤,其原因是
(6)若制备时葡萄糖溶液中含有9.0g葡萄糖,步骤⑦后得到8.2g葡萄糖酸钙,则葡萄糖酸钙的产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】硫酰氯(SO2Cl2)常作氯化剂或氯磺化剂,用于制作药品、染料、表面活性剂等。有关物质的部分性质如下表:

实验室用干燥而纯净的二氧化硫和氯气合成硫酰氯,反应的热化学方程式为:SO2(g)+Cl2(g) SO2Cl2(l) △H=—97.3 kJ·mol-1反应装置如图所示(夹持仪器已省略),请回答有关问题:
SO2Cl2(l) △H=—97.3 kJ·mol-1反应装置如图所示(夹持仪器已省略),请回答有关问题:

(1)仪器A的名称为___________________ ;
(2)仪器B的作用是_____________________ ;
(3)装置丙中盛放的试剂为____________ ,在实验室用氢氧化钠吸收多余硫酰氯的离子反应方程式为___________________ ;
(4)为提高本实验中硫酰氯的产率,在实验操作中需要注意的事项有_________ (填序号)
①先通冷凝水,再通气体
②控制气流速率,宜慢不宜快
③若三颈烧瓶发烫,可适当降温
④加热三颈烧瓶
(5)少量硫酰氯也可用氯磺酸(ClSO3H)分解获得,该反应的化学方程式为:
2ClSO3H=H2SO4+SO2Cl2,此方法得到的产品中会混有硫酸。
①从分解产物中分离出硫酰氯的实验操作名称为__________________ ,
②请设计实验方案检验氯磺酸分解制取硫酰氯产品中混有硫酸(可选试剂:稀盐酸、稀硝酸、BaCl2溶液、蒸馏水、紫色石蕊溶液)__________________________ 。

实验室用干燥而纯净的二氧化硫和氯气合成硫酰氯,反应的热化学方程式为:SO2(g)+Cl2(g)
 SO2Cl2(l) △H=—97.3 kJ·mol-1反应装置如图所示(夹持仪器已省略),请回答有关问题:
SO2Cl2(l) △H=—97.3 kJ·mol-1反应装置如图所示(夹持仪器已省略),请回答有关问题:
(1)仪器A的名称为
(2)仪器B的作用是
(3)装置丙中盛放的试剂为
(4)为提高本实验中硫酰氯的产率,在实验操作中需要注意的事项有
①先通冷凝水,再通气体
②控制气流速率,宜慢不宜快
③若三颈烧瓶发烫,可适当降温
④加热三颈烧瓶
(5)少量硫酰氯也可用氯磺酸(ClSO3H)分解获得,该反应的化学方程式为:
2ClSO3H=H2SO4+SO2Cl2,此方法得到的产品中会混有硫酸。
①从分解产物中分离出硫酰氯的实验操作名称为
②请设计实验方案检验氯磺酸分解制取硫酰氯产品中混有硫酸(可选试剂:稀盐酸、稀硝酸、BaCl2溶液、蒸馏水、紫色石蕊溶液)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】葡萄糖酸亚铁[(C6H11O7)2Fe]是医疗上常用的补铁剂,易溶于水,几乎不溶于乙醇。某实验小组同学拟用下图装置先制备FeCO3,再用FeCO3与葡萄糖酸反应进一步制得葡萄糖酸亚铁。

请回答下列问题:
(1)与普通漏斗比较,a漏斗的优点是___ 。
(2)按如图连接好装置,检查气密性后加入药品,打开K1和K3,关闭K2。
①b中的实验现象___ 。
②一段时间后,关闭___ ,打开___ (选填“K1”“K2”或“K3”),观察到b中的溶液会流入c中,同时c中析出FeCO3沉淀。
③b中产生的气体的作用是___ 。
(3)将c中制得的碳酸亚铁在空气中过滤时间较长时,表面会变为红褐色,用化学方程式说明其原因:___ 。
(4)将葡萄糖酸与碳酸亚铁混合,须将溶液的pH调节至5.8,其原因是___ 。向上述溶液中加入乙醇即可析出产品,加入乙醇的目的是___ 。
(5)有同学提出用NaHCO3溶液代替Na2CO3溶液制得的碳酸亚铁纯度更高,其可能的原因是___ 。

请回答下列问题:
(1)与普通漏斗比较,a漏斗的优点是
(2)按如图连接好装置,检查气密性后加入药品,打开K1和K3,关闭K2。
①b中的实验现象
②一段时间后,关闭
③b中产生的气体的作用是
(3)将c中制得的碳酸亚铁在空气中过滤时间较长时,表面会变为红褐色,用化学方程式说明其原因:
(4)将葡萄糖酸与碳酸亚铁混合,须将溶液的pH调节至5.8,其原因是
(5)有同学提出用NaHCO3溶液代替Na2CO3溶液制得的碳酸亚铁纯度更高,其可能的原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】过氧化钠常作漂白剂、杀菌剂、消毒剂.过氧化钠保存不当会变质.某课外活动小组为了粗略测定过氧化钠的纯度,他们称取a g样品,并设计用如图装置来测定过氧化钠的质量分数.

(1)将仪器连接好以后,必须进行的第一步操作是_______ .
(2)装置B的作用是_______ (用化学反应方程式表示).
(3)D中NaOH溶液的作用_______ .
(4)装置C中发生反应的化学方程式有_______ 、_______ .
(5)实验结束时,读取实验中生成气体的体积时,不合理的是_______ (填字母).
a.直接读取气体体积,不需冷却到室温
b.上下移动量筒,使得E、F中液面高度相同
c.视线与量筒凹液面的最低点相平,读取量筒中水的体积
(6)读出量筒内水的体积后,折算成标准状况下氧气的体积为V mL,已知标准状况下氧气的密度为ρ g/L,则样品中过氧化钠的质量分数为_______ .
(7)实验完成后,E到F之间导管内残留水的体积会使测量结果_______ (填“偏大”、“偏小”或“不影响”).

(1)将仪器连接好以后,必须进行的第一步操作是
(2)装置B的作用是
(3)D中NaOH溶液的作用
(4)装置C中发生反应的化学方程式有
(5)实验结束时,读取实验中生成气体的体积时,不合理的是
a.直接读取气体体积,不需冷却到室温
b.上下移动量筒,使得E、F中液面高度相同
c.视线与量筒凹液面的最低点相平,读取量筒中水的体积
(6)读出量筒内水的体积后,折算成标准状况下氧气的体积为V mL,已知标准状况下氧气的密度为ρ g/L,则样品中过氧化钠的质量分数为
(7)实验完成后,E到F之间导管内残留水的体积会使测量结果
您最近一年使用:0次



