某学生设计了一个“黑笔写红字”的趣味实验,如图所示。滤纸先用氯化钠、无色酚酞的混合液浸湿,接通电源后,用铅笔在滤纸上写字,会出现红色字迹.据此,回答下列问题:

(1)①a端是_______ 极; ②铂片是_______ 极。
(2)①铅笔端除了出现红色字迹,还有的现象是_______ 。
②检验铂片的产物的方法是_______ 。

(1)①a端是
(2)①铅笔端除了出现红色字迹,还有的现象是
②检验铂片的产物的方法是
更新时间:2016-12-09 06:59:35
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】电解是最强有力的氧化还原手段,在化工生产中有着重要的应用。请回答下列问题:
(1) 以铜为阳极,以石墨为阴极,用NaCl溶液作电解液进行电解,得到半导体材料Cu2O和一种清洁能源,则阳极反应式为________ ,阴极反应式为________ 。
(2)某同学设计如图所示的装置探究金属的腐蚀情况。下列判断合理的是_____ (填序号)。
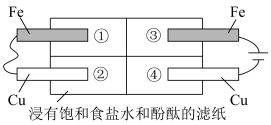
a.②区铜片上有气泡产生
b.③区铁片的电极反应式为2Cl--2e-=Cl2↑
c.最先观察到变成红色的区域是②区
d.②区和④区中铜片的质量均不发生变化
(3)最新研究发现,用隔膜电解法处理高浓度乙醛废水的工艺具有流程简单、能耗较低等优点,其原理是使乙醛分别在阴、阳极发生反应生成乙醇和乙酸,总反应式为2CH3CHO+H2O=CH3CH2OH+CH3COOH。实验室中,以一定浓度 乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如图所示。
乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如图所示。

①若以甲烷碱性燃料电池为直流电源,则燃料电池中b极应通入________ (填化学式),电极反应式为________ 。电解过程中,阴极区Na2SO4的物质的量________ (填“增大”、“减小”或“不变”)。
②若电解精炼镍则阳极材料为_______ ,铁钉镀锌时连接电源负极的是_______ (填名称)
(1) 以铜为阳极,以石墨为阴极,用NaCl溶液作电解液进行电解,得到半导体材料Cu2O和一种清洁能源,则阳极反应式为
(2)某同学设计如图所示的装置探究金属的腐蚀情况。下列判断合理的是

a.②区铜片上有气泡产生
b.③区铁片的电极反应式为2Cl--2e-=Cl2↑
c.最先观察到变成红色的区域是②区
d.②区和④区中铜片的质量均不发生变化
(3)最新研究发现,用隔膜电解法处理高浓度乙醛废水的工艺具有流程简单、能耗较低等优点,其原理是使乙醛分别在阴、阳极发生反应生成乙醇和乙酸,总反应式为2CH3CHO+H2O=CH3CH2OH+CH3COOH。实验室中,以一定浓度
 乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如图所示。
乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如图所示。
①若以甲烷碱性燃料电池为直流电源,则燃料电池中b极应通入
②若电解精炼镍则阳极材料为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】下图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极。

(1)接通电源,经过一段时间后,测得e电极上收集到气体在标准状况下体积为4.48L,乙中c电极质量增加。据此回答问题:
①电源的N端为___________ 极。
②电极b上发生的电极反应为___________ 。
③电解前后甲溶液pH___________ ;乙溶液pH___________ ;丙溶液pH___________ 。(填“变大”、“变小”或“不变”)。
(2)写出乙溶液中的电解反应方程式:___________ 需加入___________ g___________ (填物质名称)恢复原溶液。

(1)接通电源,经过一段时间后,测得e电极上收集到气体在标准状况下体积为4.48L,乙中c电极质量增加。据此回答问题:
①电源的N端为
②电极b上发生的电极反应为
③电解前后甲溶液pH
(2)写出乙溶液中的电解反应方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)熔融盐燃料电池具有高的发电效率,因而受到重视。可用熔融的碳酸盐作为电解质,向负极充入燃料气CH4,用空气与CO2的混合气作为正极的助燃气,以石墨为电极材料,制得燃料电池。工作过程中,CO32-移向__ 极(填“正”或“负”),负极的电极反应式为__ ,正极的电极反应式为___ 。
(2)某实验小组同学对电化学原理进行了一系列探究活动。
①如图为某实验小组依据的氧化还原反应:__ (用离子方程式表示)设计的原电池装置。
②其他条件不变,若将CuCl2溶液换为HCl溶液,石墨的电极反应式为___ 。
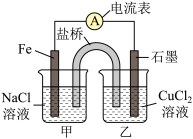
(3)如图为相互串联的甲、乙两电解池,其中甲池为电解精炼铜的装置。试回答下列问题:

①A极材料是___ ,电极反应为___ ,B极材料是__ ,主要电极反应为__ ,电解质溶液为___ 。
②乙池中若滴入少量酚酞溶液,电解一段时间后Fe极附近溶液呈___ 色。
③常温下,若甲池中阴极增重12.8g,则乙池中阳极放出的气体在标准状况下的体积为___ ,若此时乙池剩余液体为400mL,则电解后溶液pH为___ 。
(2)某实验小组同学对电化学原理进行了一系列探究活动。
①如图为某实验小组依据的氧化还原反应:
②其他条件不变,若将CuCl2溶液换为HCl溶液,石墨的电极反应式为

(3)如图为相互串联的甲、乙两电解池,其中甲池为电解精炼铜的装置。试回答下列问题:

①A极材料是
②乙池中若滴入少量酚酞溶液,电解一段时间后Fe极附近溶液呈
③常温下,若甲池中阴极增重12.8g,则乙池中阳极放出的气体在标准状况下的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】汽车尾气中的氮氧化物(NOx)对环境有危害,可利用化学方法实现氮的转化,从而降低氮氧化物排放。
(1)CO、HC(碳氢化合物)和NH3等均可在催化剂作用下,将NOx转化为N2。
①CO在氮的转化过程中体现了___ 性。
②NH3和NO反应的化学方程式为__ 。
(2)利用电解装置可以将尾气中的NO转化为尿素[CO(NH2)2,其中碳的化合价为+4价,属于非电解质],工作原理如图。

①阴极的电极反应式为___ 。
②反应一段时间后,阳极区的pH基本不变,结合化学用语解释原因为___ 。
③用NO 代替NO进行电化学反应,研究表明阴极反应的历程如下:
代替NO进行电化学反应,研究表明阴极反应的历程如下:
I.CO2(g)+2H++2e-=CO(pre)+H2O
II.……
III.CO(pre)+2NH2(pre)=CO(NH2)2
其中,CO(pre)表示CO前体,NH2(pre)表示NH2前体。用化学用语表示步骤II的反应:__ 。
(1)CO、HC(碳氢化合物)和NH3等均可在催化剂作用下,将NOx转化为N2。
①CO在氮的转化过程中体现了
②NH3和NO反应的化学方程式为
(2)利用电解装置可以将尾气中的NO转化为尿素[CO(NH2)2,其中碳的化合价为+4价,属于非电解质],工作原理如图。

①阴极的电极反应式为
②反应一段时间后,阳极区的pH基本不变,结合化学用语解释原因为
③用NO
 代替NO进行电化学反应,研究表明阴极反应的历程如下:
代替NO进行电化学反应,研究表明阴极反应的历程如下:I.CO2(g)+2H++2e-=CO(pre)+H2O
II.……
III.CO(pre)+2NH2(pre)=CO(NH2)2
其中,CO(pre)表示CO前体,NH2(pre)表示NH2前体。用化学用语表示步骤II的反应:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】能源是人类生存和发展的重要支柱,化学在能源的开发与利用方面起着十分重要的作用。某学习小组按如下图所示装置探究化学能与电能的相互转化:
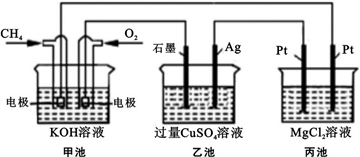
(1) 甲池是_____ 装置,通入CH4气体的电极上的反应式为_____ 。乙池中SO42- 移向_____ 电极(填“石墨”或“Ag”)
(2) 当甲池消耗标况下33.6LO2时,电解质KOH的物质的量变化_____ mol,乙池若要恢复电解前的状态则需要加入_____ g _____ (填物质名称)。
(3) 丙池中发生的电解反应的离子方程式为_____ 。

(1) 甲池是
(2) 当甲池消耗标况下33.6LO2时,电解质KOH的物质的量变化
(3) 丙池中发生的电解反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)以甲烷、空气、氢氧化钾溶液为原料,石墨为电极可以构成燃料电池。该电池的负极反应式为___________________________________________ 。
(2)用如图所示装置进行电解①若A、B均为石墨电极,C为足量CuSO4溶液,则电解的总反应方程式为___________________________________________ 。
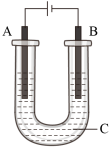
电解一段时间后,取出电极,向电解液中加入适量的___ (填化学式)可使C溶液恢复到电解前的成分和浓度。
②若A、B均为铂电极,C为Na2SO4溶液(含酚酞),电解一段时间后,___ (填“A”或“B”)极附近显红色;将电极取出,搅拌使溶液混合均匀,测得溶液的pH ____ 7(填“<”、“=”或“>”)。
③若A、B为同一材料的电极,C为CuCl2溶液,电解过程中CuCl2溶液的浓度始终 保持不变,则A、B为___ (填化学式)电极;当电路中有0.04 mol电子通过时,阴极增重___ g。
(2)用如图所示装置进行电解①若A、B均为石墨电极,C为足量CuSO4溶液,则电解的总反应方程式为

电解一段时间后,取出电极,向电解液中加入适量的
②若A、B均为铂电极,C为Na2SO4溶液(含酚酞),电解一段时间后,
③若A、B为同一材料的电极,C为CuCl2溶液,电解过程中CuCl2溶液的浓度始终 保持不变,则A、B为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】如下图所示,某研究性学习小组利用上述燃烧原理设计一个肼(N2H4)─空气燃料电池(如图甲)并探究某些工业原理,其中乙装置中X为阳离子交换膜(即只允许阳离子通过)。
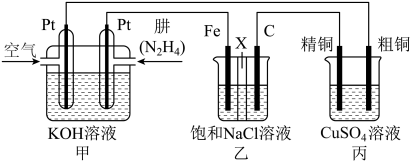
根据要求回答相关问题:
(1)甲装置中通入____ 气体的一极为正极,其电极反应式为:__________ 。
(2)乙装置中石墨电极为_____ 极(填“阳”或“阴”,其电极反应式为_____ ;可以用_____ 检验该反应产物,电解一段时间后,乙池中的溶液呈_________ 性。
(3)图中用丙装置模拟工业中的_________ 原理,如果电解后丙装置精铜质量增加3.2g,则理论上甲装置中肼消耗质量为_________ g。
(4)如果将丙中的粗铜电极换为Pt电极,则丙中总化学方程式为________ 。

根据要求回答相关问题:
(1)甲装置中通入
(2)乙装置中石墨电极为
(3)图中用丙装置模拟工业中的
(4)如果将丙中的粗铜电极换为Pt电极,则丙中总化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】纳米级Cu2O由于具有优良的催化性能而受到科学家的不断关注,下列为制取Cu2O的三种方法:
(1)工业上常用方法Ⅱ和方法Ⅲ制取Cu2O而很少用方法Ⅰ,其原因是_________________________ 。
(2)方法Ⅱ利用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,该电池的阳极反应式为______________________________ ;电解一段时间,当阴极产生的气体体积为112mL(标准状况)时,停止电解,通过离子交换膜的阴离子的物质的量为________ mol。(离子交换膜只允许OH-通过)
(3)方法Ⅲ为加热条件下用液态肼(N2H4)还原新制的Cu(OH)2来制备纳米级Cu2O,同时放出N2。生成1molN2时,生成Cu2O的物质的量为________________ 。
(4)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。写出肼-空气燃料电池放电时负极的电极反应式:___________________________ 。
| 方法Ⅰ | 用碳粉在高温条件下还原CuO |
| 方法Ⅱ | 电解法,原理为2Cu+H2O Cu2O+H2↑ Cu2O+H2↑ |
| 方法Ⅲ | 用肼(N2H4)还原新制的Cu(OH)2 |
(1)工业上常用方法Ⅱ和方法Ⅲ制取Cu2O而很少用方法Ⅰ,其原因是
(2)方法Ⅱ利用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,该电池的阳极反应式为

(3)方法Ⅲ为加热条件下用液态肼(N2H4)还原新制的Cu(OH)2来制备纳米级Cu2O,同时放出N2。生成1molN2时,生成Cu2O的物质的量为
(4)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。写出肼-空气燃料电池放电时负极的电极反应式:
您最近一年使用:0次




