分别用一种试剂将下列物质中混入的少量杂质除去(括号内为混入的杂质)
| 物质 | 需加入的试剂 | 有关离子方程式 |
| FeSO4 (Fe2(SO4) 3) | ||
| Mg(Al) | ||
| CO2 (HCl) | ||
| SiO2(CaCO3) |
更新时间:2019-01-30 18:14:09
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】食盐是日常生活的必需品,也是重要的化工原料。粗盐常含有少量Ca2+、Mg2+、 等杂质,实验室提纯NaCl的流程如图:
等杂质,实验室提纯NaCl的流程如图:
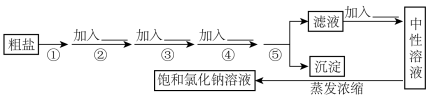
提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、稀盐酸、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、75%乙醇、四氧化碳、蒸馏水等。
回答下列问题:
(1)操作①为_______ 。
(2)欲除去粗盐中的Ca2+、Mg2+、 离子,从提供的试剂中选择,操作②③④⑥依次加入的试剂为:
离子,从提供的试剂中选择,操作②③④⑥依次加入的试剂为:_______ 、_______ 、_______ 、_______ (只填化学式)。为证明 已沉淀完全。请你写出检验方法
已沉淀完全。请你写出检验方法_______ 。
(3)上述流程中,①⑤两个过程均要用到玻璃棒,⑤处玻璃棒的作用是_______ 。
(4)食盐是无机化工生产之母,电解饱和食盐水的装置如图。
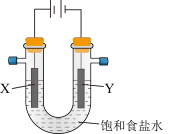
电解饱和食盐水的化学方程式为_______ ;若电解时消耗了117g氯化钠,理论上得到气体的体积为_______ (标准状况)。
 等杂质,实验室提纯NaCl的流程如图:
等杂质,实验室提纯NaCl的流程如图:
提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、稀盐酸、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、75%乙醇、四氧化碳、蒸馏水等。
回答下列问题:
(1)操作①为
(2)欲除去粗盐中的Ca2+、Mg2+、
 离子,从提供的试剂中选择,操作②③④⑥依次加入的试剂为:
离子,从提供的试剂中选择,操作②③④⑥依次加入的试剂为: 已沉淀完全。请你写出检验方法
已沉淀完全。请你写出检验方法(3)上述流程中,①⑤两个过程均要用到玻璃棒,⑤处玻璃棒的作用是
(4)食盐是无机化工生产之母,电解饱和食盐水的装置如图。

电解饱和食盐水的化学方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】用一种试剂除去下列各物质中的杂质(括号内为杂质),并写出离子方程式。
(1)BaCl2(HCl)试剂_______ ,离子方程式:____________________________________ 。
(2)CO2(HCl)试剂___________ ,离子方程式:__________________________________ 。
(3)O2(CO2)试剂__________ ,离子方程式:____________________________________ 。
(4)SO42-(CO32-)试剂_______ ,离子方程式:__________________________________ 。
(1)BaCl2(HCl)试剂
(2)CO2(HCl)试剂
(3)O2(CO2)试剂
(4)SO42-(CO32-)试剂
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)物质的量相等的 CO 和 CO2 中,同温同压下所占的体积比为____ ,原子个数之比为______ ;
(2)1.8g水与_______ mol硫酸所含的分子数相等,它们所含氧原子数之比是________ ,其中氢原子数之比是___________ 。
(3)3.2g某气体中含有的分子数约为3.01×1022,此气体的摩尔质量为________ 。
(4)可用于分离或提纯物质的方法有:
A 过滤 B 萃取 C 渗析 D 蒸馏 E 灼热氧化 F 分液.
如欲分离或提纯下列各组混合物,请选择上述方法中最合适者,并将相应字母填入题后空格内:
①除去淀粉溶液中的少量碘化钠________ ; ②提取溴水中的溴单质______ ;
③除去水中的Na+、 、Cl-等杂质
、Cl-等杂质________ ; ④除去CuO中的Cu ______ ;
(2)1.8g水与
(3)3.2g某气体中含有的分子数约为3.01×1022,此气体的摩尔质量为
(4)可用于分离或提纯物质的方法有:
A 过滤 B 萃取 C 渗析 D 蒸馏 E 灼热氧化 F 分液.
如欲分离或提纯下列各组混合物,请选择上述方法中最合适者,并将相应字母填入题后空格内:
①除去淀粉溶液中的少量碘化钠
③除去水中的Na+、
 、Cl-等杂质
、Cl-等杂质
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】在上海召开的第七届全球人类基因大会上,我国科学家第一次提出可以用砒霜(As2O3)来治疗早期幼粒白血病。
(1)完成并配平下列化学方程式:_____________
As2O3+ Zn+ H2SO4 → AsH3+ ZnSO4+ ______
(2)As2O3在上述反应中显示出来的性质是_____________ 。
A.氧化性 B.还原性 C.酸性 D.碱性
(3)若生成0.1 mol AsH3,则转移电子的物质的量为___________ mol。
(1)完成并配平下列化学方程式:
As2O3+ Zn+ H2SO4 → AsH3+ ZnSO4+ ______
(2)As2O3在上述反应中显示出来的性质是
A.氧化性 B.还原性 C.酸性 D.碱性
(3)若生成0.1 mol AsH3,则转移电子的物质的量为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】完成下列填空:
I.(1)呼吸面具中,Na2O2起反应的化学方程式为_____________ 。
(2)印刷电路板由高分子材料和铜箔复合而成,用FeCl3溶液刻制印刷电路时,发生的反应离子方程式为__________________ 。
(3)把一定量铁粉放入氯化铁溶液中,完全反应后,所得溶液中Fe2+和Fe3+的物质的量浓度之比为3:2,则已反应的Fe3+和未反应的Fe3+的物质的量之比为_____________ 。
II.某一反应体系中有反应物和生成物共6种: HCl、H2SO4、SnCl2、SnCl4、FeSO4、Fe(SO4)3,反应前在溶液中滴加KSCN 溶液显红色,反应后红色消失。
(1)该反应中的还原剂是_____________ 。
(2)写出该反应的化学方程式_____________ 。
I.(1)呼吸面具中,Na2O2起反应的化学方程式为
(2)印刷电路板由高分子材料和铜箔复合而成,用FeCl3溶液刻制印刷电路时,发生的反应离子方程式为
(3)把一定量铁粉放入氯化铁溶液中,完全反应后,所得溶液中Fe2+和Fe3+的物质的量浓度之比为3:2,则已反应的Fe3+和未反应的Fe3+的物质的量之比为
II.某一反应体系中有反应物和生成物共6种: HCl、H2SO4、SnCl2、SnCl4、FeSO4、Fe(SO4)3,反应前在溶液中滴加KSCN 溶液显红色,反应后红色消失。
(1)该反应中的还原剂是
(2)写出该反应的化学方程式
您最近半年使用:0次
【推荐3】(1)将SO2通入氯化钡溶液中无现象;若将SO2通入硝酸钡溶液中,有白色沉淀产生,其化学反应方程式如下(未配平):SO2+Ba(NO3)2+H2O→BaSO4↓+HNO3+NO↑
①配平上述化学反应方程式:___ 。
②该反应中,___ 元素发生氧化反应,氧化剂是___ (写化学式)。氧化产物与还原产物的物质的量之比为___ 。
③当反应消耗19.2gSO2时,反应中转移电子____ mol。
(2)维生素C又称“抗坏血酸”,能帮助人体将食物中摄取的不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有___ (填氧化性或还原性)。
①配平上述化学反应方程式:
②该反应中,
③当反应消耗19.2gSO2时,反应中转移电子
(2)维生素C又称“抗坏血酸”,能帮助人体将食物中摄取的不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】欲除去下列物质中的杂质(括号内为杂质),请选择合适的试剂并写出有关的化学方程式:
①SiO2(Al2O3)____________________ ;
②Na2CO3固体(NaHCO3)_______________________ ;
③FeCl3溶液(FeCl2)___________________ 。
①SiO2(Al2O3)
②Na2CO3固体(NaHCO3)
③FeCl3溶液(FeCl2)
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如下的反应关系:
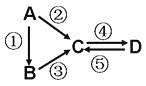
(1)若D物质具有两性,②③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体,写出②反应的离子方程式_____________ ;④反应的离子方程式______________ ;
(2)若A是应用最广泛的金属,④反应用到A,②⑤反应均用到同一种黄绿色气体单质。写出A与水反应的化学方程式__________________ 。④反应的离子方程式___________________ ;
D中加入氢氧化钠的现象是_____________________ 。
(3)若A是太阳能电池用的光伏材料。C、D为钠盐,且溶液均显碱性,④反应也是通入一种引起温室效应的主要气体。写出②反应的化学方程式______________________________________ 。
⑤反应用到B,反应条件为高温,则⑤的化学方程式为________________________________ 。

(1)若D物质具有两性,②③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体,写出②反应的离子方程式
(2)若A是应用最广泛的金属,④反应用到A,②⑤反应均用到同一种黄绿色气体单质。写出A与水反应的化学方程式
D中加入氢氧化钠的现象是
(3)若A是太阳能电池用的光伏材料。C、D为钠盐,且溶液均显碱性,④反应也是通入一种引起温室效应的主要气体。写出②反应的化学方程式
⑤反应用到B,反应条件为高温,则⑤的化学方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】化学是在原子、分子水平上研究物质的组成、结构、性质、转化及其应用的基础自然科学。
(1)根据下列物质的组成和性质完成填空。
a.铁 b.硫酸铜溶液 c.熔融氯化钠 d.过氧化钠固体 e.石墨 f.氨气
①属于电解质的是___________ (填字母序号,下同)。
②上述状态下能导电的物质有___________ 。
③写出硫酸铜的电离方程式___________ 。
(2)向一定量的 和
和 混合溶液中逐滴滴加氢氧化钠溶液至过量(体积变化忽略不计)。下列图像不能正确反映对应变化关系的是___________。
混合溶液中逐滴滴加氢氧化钠溶液至过量(体积变化忽略不计)。下列图像不能正确反映对应变化关系的是___________。
(3)经检测,某酸性废水中存在大量的 、
、 、
、 、
、 。现进行以下实验:
。现进行以下实验:
①取100 mL该废水于烧杯中,逐滴滴加NaOH溶液至呈碱性,原废水中离子的数目会发生变化的是___________ (用离子符号表示)。
②欲除去其中的 、
、 ,并得到中性溶液,设计的工艺流程如图所示。
,并得到中性溶液,设计的工艺流程如图所示。

操作X的名称是___________ ,试剂b中溶质的化学式为___________ 。
③测得100 mL废水中 、
、 、
、 、
、 的物质的量浓度分别为0.5 mol/L、0.5 mol/L、0.1 mol/L、0.2 mol/L,则该废水中
的物质的量浓度分别为0.5 mol/L、0.5 mol/L、0.1 mol/L、0.2 mol/L,则该废水中
___________ 。
(1)根据下列物质的组成和性质完成填空。
a.铁 b.硫酸铜溶液 c.熔融氯化钠 d.过氧化钠固体 e.石墨 f.氨气
①属于电解质的是
②上述状态下能导电的物质有
③写出硫酸铜的电离方程式
(2)向一定量的
 和
和 混合溶液中逐滴滴加氢氧化钠溶液至过量(体积变化忽略不计)。下列图像不能正确反映对应变化关系的是___________。
混合溶液中逐滴滴加氢氧化钠溶液至过量(体积变化忽略不计)。下列图像不能正确反映对应变化关系的是___________。A.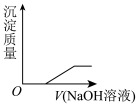 | B.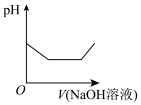 |
C.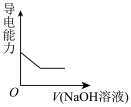 | D. |
(3)经检测,某酸性废水中存在大量的
 、
、 、
、 、
、 。现进行以下实验:
。现进行以下实验:①取100 mL该废水于烧杯中,逐滴滴加NaOH溶液至呈碱性,原废水中离子的数目会发生变化的是
②欲除去其中的
 、
、 ,并得到中性溶液,设计的工艺流程如图所示。
,并得到中性溶液,设计的工艺流程如图所示。
操作X的名称是
③测得100 mL废水中
 、
、 、
、 、
、 的物质的量浓度分别为0.5 mol/L、0.5 mol/L、0.1 mol/L、0.2 mol/L,则该废水中
的物质的量浓度分别为0.5 mol/L、0.5 mol/L、0.1 mol/L、0.2 mol/L,则该废水中
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】硫酸锌广泛应用于工农业生产中。工业上以粗氧化锌(含 等杂质)为原料生产
等杂质)为原料生产 的一种流程的部分过程如下(各过程需控制适宜条件)。
的一种流程的部分过程如下(各过程需控制适宜条件)。
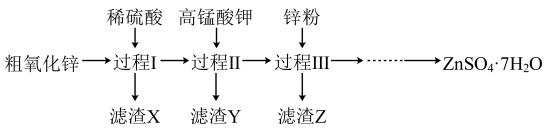
(1)过程Ⅰ、Ⅱ、Ⅲ中,分离出X、Y、Z的实验操作是_______ 。
(2)过程Ⅰ,能与稀硫酸反应的物质有________ 。写出生成氢气的离子方程式:_______ ,因此过程Ⅰ需要持续强制通风,原因是生成的氢气具有______ 性。
(3)过程Ⅱ中,滤渣Y含有 。加入高锰酸钾的主要目的是
。加入高锰酸钾的主要目的是_______ 。
(4)过程Ⅲ中,滤渣Z含铜,生成铜的离子方程式为________ 。
 等杂质)为原料生产
等杂质)为原料生产 的一种流程的部分过程如下(各过程需控制适宜条件)。
的一种流程的部分过程如下(各过程需控制适宜条件)。
(1)过程Ⅰ、Ⅱ、Ⅲ中,分离出X、Y、Z的实验操作是
(2)过程Ⅰ,能与稀硫酸反应的物质有
(3)过程Ⅱ中,滤渣Y含有
 。加入高锰酸钾的主要目的是
。加入高锰酸钾的主要目的是(4)过程Ⅲ中,滤渣Z含铜,生成铜的离子方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】I、现有下列八种物质: ①铝 ②蔗糖 ③SiO2 ④H2SO4 ⑤NaOH ⑥FeSO4溶液 ⑦Ba(OH)2 ⑧氢氧化铁胶体
(1)上述物质属于电解质的有____________ (填序号)。能导电的有__________ (填序号)。
(2)向⑤中加入①的粉末,反应的离子方程式为_____________________ 。
(3)上述物质中有两种物质在水溶液中反应的离子方程式为H++OH-=H2O,则该反应的化学方程式为__________________________ 。
(4)实验室制备⑧的离子方程式为:__________________ 。若在⑧中缓慢加入④的溶液,产生的现象是________________________ 。
(5) ③是玻璃的主要成分之一,③与⑤溶液反应的化学方程式为____________________ 。工艺师常用_______ (填物质名称) 来雕刻玻璃。
II、下列各组物质的分离或提纯,应选用下述方法的哪一种? (填选项字母)
A.分液 B.过滤 C.萃取 D.蒸馏 E.蒸发结晶 F.高温分解
(1)分离CCl4和H2O:___________ ;
(2)除去澄清石灰水中悬浮的CaCO3:___________ ;
(3)分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的液体混合物:__________ 。
(1)上述物质属于电解质的有
(2)向⑤中加入①的粉末,反应的离子方程式为
(3)上述物质中有两种物质在水溶液中反应的离子方程式为H++OH-=H2O,则该反应的化学方程式为
(4)实验室制备⑧的离子方程式为:
(5) ③是玻璃的主要成分之一,③与⑤溶液反应的化学方程式为
II、下列各组物质的分离或提纯,应选用下述方法的哪一种? (填选项字母)
A.分液 B.过滤 C.萃取 D.蒸馏 E.蒸发结晶 F.高温分解
(1)分离CCl4和H2O:
(2)除去澄清石灰水中悬浮的CaCO3:
(3)分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的液体混合物:
您最近半年使用:0次



