除去下列物质中所混有的少量杂质,括号内为杂质。指明应加入的试剂,写出有关方程式。
(1)Fe粉(Al粉):试剂___ 离子方程式___ ;
(2)FeCl2溶液(FeCl3):试剂___ 离子方程式___ ;
(3)Na2CO3固体(NaHCO3):化学方程式___ 。
(1)Fe粉(Al粉):试剂
(2)FeCl2溶液(FeCl3):试剂
(3)Na2CO3固体(NaHCO3):化学方程式
更新时间:2019-12-22 18:40:23
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】写出下列除杂的化学方程式(有离子方程式的还要写出相应的离子方程式)
⑴化学方程式________________________ ,离子方程式_________________ 。
⑵化学方程式________________________ ,离子方程式__________________ 。
⑶化学方程式________________________ ,离子方程式____________________ 。
| 混合物 | 除杂方法及试剂 |
| ⑴Na2CO3固体(NaHCO3) | 加热 |
| ⑵NaHCO3溶液(Na2CO3) | 通入足量CO2气体 |
| ⑶Na2CO3溶液(NaHCO3) | 加入适量NaOH溶液 |
⑴化学方程式
⑵化学方程式
⑶化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】除去下表各溶液中含有的少量杂质(括号内)填写下表_______
| 各物质的溶液(杂质) | 除去杂质所需试剂 | 离子方程式 |
| KCl(KHCO3) | ||
| Na2CO3(NaHCO3) | ||
| NaHCO3(Na2CO3) |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】根据信息书写反应的方程式:
(1)除去NaHCO3溶液中少量的Na2CO3,写出该反应的离子方程式:___________ 。
(2)氢氧化镁中和过多的胃酸反应的离子方程式:___________ 。
(3)“洁厕灵(含盐酸)”与“84”消毒液混合会发生反应产生Cl2,写出反应的离子方程式___________ 。
(4)已知SiO2属于酸性氧化物,H2SiO3是难溶于水的弱酸。一种以SiO2为原料制取H2SiO3的流程如下:

①写出反应Ⅰ的化学方程式:___________ 。
②写出反应Ⅱ的离子方程式:___________ 。
(1)除去NaHCO3溶液中少量的Na2CO3,写出该反应的离子方程式:
(2)氢氧化镁中和过多的胃酸反应的离子方程式:
(3)“洁厕灵(含盐酸)”与“84”消毒液混合会发生反应产生Cl2,写出反应的离子方程式
(4)已知SiO2属于酸性氧化物,H2SiO3是难溶于水的弱酸。一种以SiO2为原料制取H2SiO3的流程如下:

①写出反应Ⅰ的化学方程式:
②写出反应Ⅱ的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】家庭用的洗涤去污剂有下列几种,其含有的有效成分如下:
(1)管道疏通剂可用于疏通管道中因毛发、残渣等造成的堵塞,使用时会产生大量气泡,且要防止明火,以免发生爆炸,则疏通时反应的离子方程式为___________ ,在该反应中每生成1mol气体,被还原的物质的质量为___________ g.也不能与“洁厕灵”混合使用,降低疏通效果,其原因是___________ 。
(2)洁厕灵与84消毒液混合使用会产生黄绿色的有毒气体,易造成危险,反应的离子方程式为___________ 。
(3)彩漂剂使用时会释放出一种无色无味的气体,使污垢活化,易于洗涤。但是不能长期存放,会降低彩漂效果,则发生的反应的还原产物为___________ (写化学式)。
(4)某兴趣小组做如下探究实验,请回答下列问题:
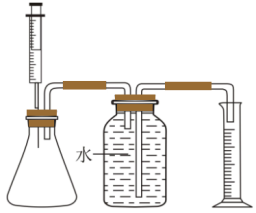
①如图组装实验装置,并___________ ;
②向锥形瓶加入10mL的84消毒液,注射器中吸入10mL的彩漂剂,
③将注射器中的彩漂剂慢慢注入锥形瓶中,产生无色无味的气体,发生的化学方程式为___________ 。
④直至不再产生气泡。
| 示例 |  |  |  |  |
| 名称 | 管道疏通剂 | 洁厕灵 | 彩漂剂 | 84消毒液 |
| 有效成分 | 氢氧化物和铝粉 | 浓盐酸 | 双氧水 | NaClO溶液 |
| 用途 | 清理管道污垢,防堵塞 | 清理马桶污垢,除异味 | 漂洗衣物,使色彩鲜艳 | 消毒漂白 |
(2)洁厕灵与84消毒液混合使用会产生黄绿色的有毒气体,易造成危险,反应的离子方程式为
(3)彩漂剂使用时会释放出一种无色无味的气体,使污垢活化,易于洗涤。但是不能长期存放,会降低彩漂效果,则发生的反应的还原产物为
(4)某兴趣小组做如下探究实验,请回答下列问题:

①如图组装实验装置,并
②向锥形瓶加入10mL的84消毒液,注射器中吸入10mL的彩漂剂,
③将注射器中的彩漂剂慢慢注入锥形瓶中,产生无色无味的气体,发生的化学方程式为
④直至不再产生气泡。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】以下元素及物质与人类的生产生活紧密相关。完成下列填空:
(1)氯元素原子结构示意图为_______ ,其与钠元素组成的化合物的电子式为_______ 。
(2)铝是地壳中含量最高的金属元素,其在周期表中位于第_______ 周期_______ 族。
(3)以下不是铝和铁的共同性质的是_______ 。
a.导电性 b.导热性 c.延展性 d.两性
(4)下列能说明氯元素的非金属性比硫元素强的事实是_______ 。
a.稳定性 b.氧化性
b.氧化性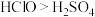
c.酸性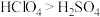 强 d.
强 d. 溶液是强酸,
溶液是强酸, 溶液是弱酸
溶液是弱酸
(1)氯元素原子结构示意图为
(2)铝是地壳中含量最高的金属元素,其在周期表中位于第
(3)以下不是铝和铁的共同性质的是
a.导电性 b.导热性 c.延展性 d.两性
(4)下列能说明氯元素的非金属性比硫元素强的事实是
a.稳定性
 b.氧化性
b.氧化性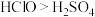
c.酸性
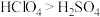 强 d.
强 d. 溶液是强酸,
溶液是强酸, 溶液是弱酸
溶液是弱酸
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】历史上铝制饭碗曾被法国皇帝当作自己富有的象征炫耀过,但现在各种铝制品已走进寻常百姓家,这得益于电解法冶炼铝技术的发明。
(1)现代工业在1273 K的温度下电解熔融氧化铝(熔点2323 K)与冰晶石(Na3AlF6)的混合物,可得到金属铝与氧气。阴极上的电极反应式为__________ ,其中冰晶石的作用可能是___ 。
a.作催化剂
b.作熔剂以降低氧化铝的熔化温度
c.作电解质增强导电性
(2)为使铝制品经久耐用,现代工业生产中常对铝材进行表面处理,具体过程通常为:
①铝材脱脂:先用碱液洗涤,然后水洗,以除去铝材表面的自然氧化膜,碱洗过程中常有气泡产生,原因是_____________________________ (用离子方程式表示)。
②电解氧化:以铝材为阳极,在稀硫酸中进行电解,铝材表面形成氧化膜,则阳极的电极反应方程式为_____________________________ ,电解过程中必须使电解质溶液的pH保持相对稳定的原因是__________________________ 。
(1)现代工业在1273 K的温度下电解熔融氧化铝(熔点2323 K)与冰晶石(Na3AlF6)的混合物,可得到金属铝与氧气。阴极上的电极反应式为
a.作催化剂
b.作熔剂以降低氧化铝的熔化温度
c.作电解质增强导电性
(2)为使铝制品经久耐用,现代工业生产中常对铝材进行表面处理,具体过程通常为:
①铝材脱脂:先用碱液洗涤,然后水洗,以除去铝材表面的自然氧化膜,碱洗过程中常有气泡产生,原因是
②电解氧化:以铝材为阳极,在稀硫酸中进行电解,铝材表面形成氧化膜,则阳极的电极反应方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】按要求完成下列除杂问题:
(1)FeCl2溶液中混有少量FeCl3,除杂试剂为___________ ,离子方程式___________ ;
(2)FeCl3溶液中混有少量FeCl2,除杂试剂为___________ ,离子方程式___________ ;
(3)Fe2O3中混有Al2O3,除杂试剂为___________ ,离子方程式 ___________ 。
(1)FeCl2溶液中混有少量FeCl3,除杂试剂为
(2)FeCl3溶液中混有少量FeCl2,除杂试剂为
(3)Fe2O3中混有Al2O3,除杂试剂为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】金属材料对于促进生产发展、改善人类生活发挥了巨大作用。请回答下列关于金属及其化合物的问题:
(1)若加入铝粉能放出氢气的溶液中分别加入下列各组离子,可能共存的是_______。
(2)实验室里保存 溶液时,常在溶液中加入
溶液时,常在溶液中加入_______ ,其目的为_______ 。
(3)实验室配制 溶液时,为了防止
溶液时,为了防止 水解,需要将
水解,需要将 溶于稀硫酸中,再加水稀释。现需配制
溶于稀硫酸中,再加水稀释。现需配制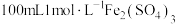 溶液,需要用托盘天平称量
溶液,需要用托盘天平称量_______ g 晶体,配制该溶液所需玻璃仪器除了烧杯、玻璃棒、量筒外,还需要
晶体,配制该溶液所需玻璃仪器除了烧杯、玻璃棒、量筒外,还需要_______ ;如果配制时俯视定容,那么所配溶液的浓度_______ (填“偏大”、“小”或“无影响”)。
(4)除杂:(括号内为杂质)
①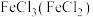 除杂试剂为
除杂试剂为_______ (填化学式),离子方程式为_______ ;
②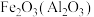 除杂试剂为
除杂试剂为_______ (填化学式),离子方程式为_______ 。
(1)若加入铝粉能放出氢气的溶液中分别加入下列各组离子,可能共存的是_______。
A.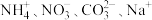 | B.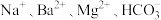 |
C.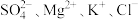 | D.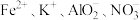 |
 溶液时,常在溶液中加入
溶液时,常在溶液中加入(3)实验室配制
 溶液时,为了防止
溶液时,为了防止 水解,需要将
水解,需要将 溶于稀硫酸中,再加水稀释。现需配制
溶于稀硫酸中,再加水稀释。现需配制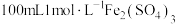 溶液,需要用托盘天平称量
溶液,需要用托盘天平称量 晶体,配制该溶液所需玻璃仪器除了烧杯、玻璃棒、量筒外,还需要
晶体,配制该溶液所需玻璃仪器除了烧杯、玻璃棒、量筒外,还需要(4)除杂:(括号内为杂质)
①
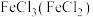 除杂试剂为
除杂试剂为②
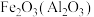 除杂试剂为
除杂试剂为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】海洋资源的利用具有广阔前景。
(1)无需经过化学变化就能从海水中获得的物质是( ) (填序号)
A.Cl2 B.淡水 C.烧碱 D.食盐
(2)下图是从海水中提取镁的简单流程。
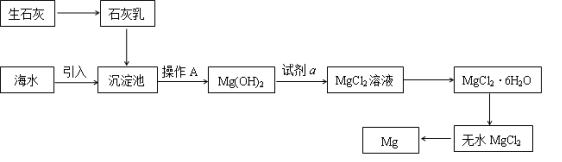
①操作A是_______________________ 。
②无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为____________________________ 。
③海水提镁的过程,为什么要将海水中的氯化镁转变为氢氧化镁,再转变为氯化镁?_____________________________________________ 。
(3)海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如下所示:

①灼烧海带至灰烬时所用的主要仪器名称是( ) (填序号)
a.坩埚 b.试管 c.蒸发皿 d.烧杯
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式________________________________ 。
③用CCl4提取碘时除了用CCl4还可以选用的试剂是( ) (填字母序号)
a.苯 b.乙醇 c.乙酸
④为检验用CCl4提取碘后的水溶液中是否还含有碘单质。请写出该实验的实验步骤、现象及结论:________ 。
(4)利用海底的“可燃冰”制作的燃料电池的总反应式为CH4+2O2+2KOH = K2CO3+3H2O,则该燃料电池的负极的电极反应为__________________ 。
(5)海底的煤经综合利用开发的副产物CO2能生产甲醇燃料,其反应的方程式为:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。某科学实验将6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a,b,c,d括号内数据表示坐标。
CH3OH(g)+H2O(g)。某科学实验将6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a,b,c,d括号内数据表示坐标。
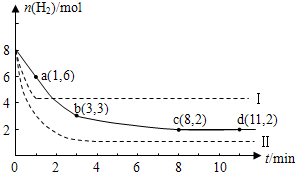
①a点正反应速率_________ (填“大于、等于或小于”)a点逆反应速率。
②平衡时CO2的物质的量浓度是___________ mol/L。
③能够说明该反应达到化学平衡状态的标志是_______ (双选)。
A.单位时间内消耗1molCO2,同时生成3mol H2 B.混合气体的密度不随时间变化
C.CH3OH、H2的浓度不再随时间变化 D.CH3OH和H2O浓度相等
(1)无需经过化学变化就能从海水中获得的物质是
A.Cl2 B.淡水 C.烧碱 D.食盐
(2)下图是从海水中提取镁的简单流程。

①操作A是
②无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为
③海水提镁的过程,为什么要将海水中的氯化镁转变为氢氧化镁,再转变为氯化镁?
(3)海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如下所示:

①灼烧海带至灰烬时所用的主要仪器名称是
a.坩埚 b.试管 c.蒸发皿 d.烧杯
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式
③用CCl4提取碘时除了用CCl4还可以选用的试剂是
a.苯 b.乙醇 c.乙酸
④为检验用CCl4提取碘后的水溶液中是否还含有碘单质。请写出该实验的实验步骤、现象及结论:
(4)利用海底的“可燃冰”制作的燃料电池的总反应式为CH4+2O2+2KOH = K2CO3+3H2O,则该燃料电池的负极的电极反应为
(5)海底的煤经综合利用开发的副产物CO2能生产甲醇燃料,其反应的方程式为:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。某科学实验将6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a,b,c,d括号内数据表示坐标。
CH3OH(g)+H2O(g)。某科学实验将6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a,b,c,d括号内数据表示坐标。
①a点正反应速率
②平衡时CO2的物质的量浓度是
③能够说明该反应达到化学平衡状态的标志是
A.单位时间内消耗1molCO2,同时生成3mol H2 B.混合气体的密度不随时间变化
C.CH3OH、H2的浓度不再随时间变化 D.CH3OH和H2O浓度相等
您最近一年使用:0次
【推荐2】现有很有少量SO2杂质的CO2气体,请选用下列部分实验装置。收集纯净干燥的CO2气体。

(1)要达到实验目的,按气流从左到右,各接口连接顺序正确的是____ (填字母)。
(2)下列溶液或用品中:①澄清石灰水;②H2S溶液;③酸性KMmO4溶液;④溴水;⑤Ba(NO3)2溶液;⑥品红溶液;⑦湿润的蓝色石蕊试纸。不能区别SO2和CO2气体的是____ 。
(3)写出SO2与酸性KMnO4溶液反应的离子方程式____ 。

(1)要达到实验目的,按气流从左到右,各接口连接顺序正确的是
(2)下列溶液或用品中:①澄清石灰水;②H2S溶液;③酸性KMmO4溶液;④溴水;⑤Ba(NO3)2溶液;⑥品红溶液;⑦湿润的蓝色石蕊试纸。不能区别SO2和CO2气体的是
| A.①⑤⑦ | B.①⑤ | C.①⑦ | D.②③④⑤⑥ |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题
(1)已知NaCl的熔点为801℃,而 (可简写为
(可简写为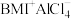 )的熔点为-65℃,室温下呈液体状态,是一种重要的室温离子液体。试解释为什么
)的熔点为-65℃,室温下呈液体状态,是一种重要的室温离子液体。试解释为什么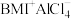 熔点远低于NaCl。
熔点远低于NaCl。_______ 。
(2)实验室中常用氨水吸收过量的 。现有一瓶500ml已经吸收
。现有一瓶500ml已经吸收 的氨水溶液,将其均分成A、B两份,对其进行如下实验分析(吸收前后溶液体积不变);
的氨水溶液,将其均分成A、B两份,对其进行如下实验分析(吸收前后溶液体积不变);
a.向A中加入足量的NaOH溶液并加热,将生成的气体先通过碱石灰,再通入盛有过量无水 的装置C中,测量得反应前后装置C增重6.80g。
的装置C中,测量得反应前后装置C增重6.80g。
b.向B中加入足量稀硫酸并加热,将生成的气体先通过浓硫酸,再通入盛有过量碱石灰的装置D中,测量得反应前后装置D增重19.2g。
试回答以下问题:
①原溶液中亚硫酸铵与亚硫酸氢铵物质的量的之比是_______
②用来吸收 的氨水原物质的量浓度为
的氨水原物质的量浓度为_______
(1)已知NaCl的熔点为801℃,而
 (可简写为
(可简写为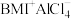 )的熔点为-65℃,室温下呈液体状态,是一种重要的室温离子液体。试解释为什么
)的熔点为-65℃,室温下呈液体状态,是一种重要的室温离子液体。试解释为什么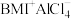 熔点远低于NaCl。
熔点远低于NaCl。(2)实验室中常用氨水吸收过量的
 。现有一瓶500ml已经吸收
。现有一瓶500ml已经吸收 的氨水溶液,将其均分成A、B两份,对其进行如下实验分析(吸收前后溶液体积不变);
的氨水溶液,将其均分成A、B两份,对其进行如下实验分析(吸收前后溶液体积不变);a.向A中加入足量的NaOH溶液并加热,将生成的气体先通过碱石灰,再通入盛有过量无水
 的装置C中,测量得反应前后装置C增重6.80g。
的装置C中,测量得反应前后装置C增重6.80g。b.向B中加入足量稀硫酸并加热,将生成的气体先通过浓硫酸,再通入盛有过量碱石灰的装置D中,测量得反应前后装置D增重19.2g。
试回答以下问题:
①原溶液中亚硫酸铵与亚硫酸氢铵物质的量的之比是
②用来吸收
 的氨水原物质的量浓度为
的氨水原物质的量浓度为
您最近一年使用:0次



