一定质量的镁、铝混合物投到2 mol·L-1的盐酸中,待金属完全溶解后,向溶液中加入2 mol·L-1的氢氧化钠溶液,生成沉淀的质量与加入氢氧化钠溶液的体积关系如图所示。
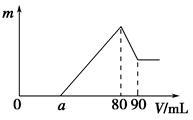
则:
(1)80~90mL对应反应的离子方程式_____________________ 。
(2)金属铝的质量为_________
(3)盐酸的体积是____________ mL。
(4)a的取值范围是___________ 。
(5)n(Mg)/n(Al)的最大值是_________ 。

则:
(1)80~90mL对应反应的离子方程式
(2)金属铝的质量为
(3)盐酸的体积是
(4)a的取值范围是
(5)n(Mg)/n(Al)的最大值是
更新时间:2016-12-09 07:06:46
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】一定量的Mg、Al的混合物中加入足量盐酸,产生标准状况下的气体5.6L,再在此溶液中加入过量NaOH溶液,产生沉淀5.8克,求:
(1)Mg、Al的物质的量各为多少_________ ?
(2)若将此混合物投入足量的NaOH溶液中,求标准状况下产生气体的体积_________ 。
(1)Mg、Al的物质的量各为多少
(2)若将此混合物投入足量的NaOH溶液中,求标准状况下产生气体的体积
您最近半年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】将一定质量的Mg和Al的混合物投入500mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示.
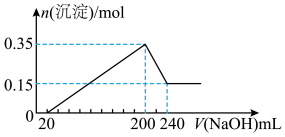
(1)Mg和Al的总质量为___________ g;
(2)硫酸的物质的量浓度为___________ ;
(3)NaOH溶液的物质的量浓度为___________ 。

(1)Mg和Al的总质量为
(2)硫酸的物质的量浓度为
(3)NaOH溶液的物质的量浓度为
您最近半年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】I.在标准状况下进行甲、乙、丙三组实验,三组实验均各取20ml相同物质的量浓度的盐酸,加入同一种镁铝合金粉末,产生气体,有关数据见表:
请回答下列问题:
(1)根据表格中的数据求盐酸的溶质的物质的量浓度为___________ ;
(2)求合金中 Mg、Al 的物质的量之比_________ 。
II.(1)V mL Al2(SO4)3溶液中含有Al3+m g,取V/4mL该溶液用水稀释至4V mL,则SO42—物质的量浓度为_____________________ 。
(3)已知硫酸溶液浓度越大,密度越大,现将3p%的硫酸与同体积的p%的硫酸混合得到q%的稀硫酸,则p、q的关系正确的是______ (填序号)。
①q=2p ②q>2p ③q<2p ④无法确定
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/mg | 255 | 385 | 459 |
| 生成气体/mL | 280 | 336 | 336 |
请回答下列问题:
(1)根据表格中的数据求盐酸的溶质的物质的量浓度为
(2)求合金中 Mg、Al 的物质的量之比
II.(1)V mL Al2(SO4)3溶液中含有Al3+m g,取V/4mL该溶液用水稀释至4V mL,则SO42—物质的量浓度为
(3)已知硫酸溶液浓度越大,密度越大,现将3p%的硫酸与同体积的p%的硫酸混合得到q%的稀硫酸,则p、q的关系正确的是
①q=2p ②q>2p ③q<2p ④无法确定
您最近半年使用:0次
【推荐1】(1)把一定质量的镁、铝混合物投入到1mol·L-1的盐酸中,待金属完全溶解后,向溶液中加入1mol·L-1的氢氧化钠溶液,生成沉淀的质量与加入氢氧化钠溶液的体积关系如图所示。则:
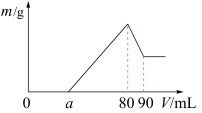
①金属铝的质量为________ g
②a的取值范围是________ mL。
(2)浓度分别为1mol /L的硫酸、氢氧化钠溶液各200mL分别放在甲、乙两烧杯中,各加等质量的铝,生成氢气的体积比为8:9,则甲、乙两烧杯中加入的铝的物质的为______ 。

①金属铝的质量为
②a的取值范围是
(2)浓度分别为1mol /L的硫酸、氢氧化钠溶液各200mL分别放在甲、乙两烧杯中,各加等质量的铝,生成氢气的体积比为8:9,则甲、乙两烧杯中加入的铝的物质的为
您最近半年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】硝酸与金属反应时,浓度越稀还原产物价态越低。现用一定量的铝粉与镁粉组成的混合物与100mL硝酸钾溶液与硫酸组成的混合溶液充分反应,反应过程中无任何气体放出,向反应后的溶液中逐滴加入4.00mol/L的NaOH溶液,加入的溶液体积与与产生的沉淀质量的关系如图所示。
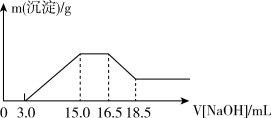
回答下列问题:
(1)写出铝与混合溶液反应的离子方程式:_______ 。
(2)参加反应硝酸根离子物质的量为_______ mol。
(3)参加反应的铝与镁的物质的量之比为_______ 。
(4)混合液中硫酸的物质的量的浓度为_______ mol/L。

回答下列问题:
(1)写出铝与混合溶液反应的离子方程式:
(2)参加反应硝酸根离子物质的量为
(3)参加反应的铝与镁的物质的量之比为
(4)混合液中硫酸的物质的量的浓度为
您最近半年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】现称取一定质量的镁铝合金样品放入500mL稀硫酸中,固体全部溶解并放出气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示。
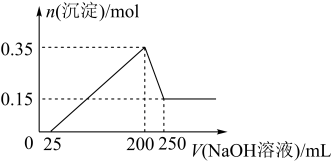
(1)合金中Al的质量为___ 。
(2)NaOH溶液的物质的量浓度为___ 。
(3)稀硫酸的物质的量浓度为__ 。

(1)合金中Al的质量为
(2)NaOH溶液的物质的量浓度为
(3)稀硫酸的物质的量浓度为
您最近半年使用:0次
计算题
|
适中
(0.65)
【推荐2】回答下列问题
(1)标准状况下112mL气体A的质量为0.32g,则A气体的摩尔质量为____ 。
(2)标准状况下有四种气体:①6.72LC2H6;②3.01×1024个HCl分子;③0.2molH2S;④10.2gNH3。各气体中氢原子数的大小顺序为(用①②③④表示):______________ 。
(3)在300mL由NaCl、MgCl2、AlCl3组成的混合液中,部分离子浓度大小如图所示,回答下列问题。

①该混合液中AlCl3的物质的量为____ mol。将该混合液加水稀释至体积为500mL,稀释后溶液中Al3+物质的量浓度为______ mol/L。
②向①中稀释后的溶液中加入过量氢氧化钠溶液,则发生反应的离子方程式为:_________ ;最终可得到沉淀质量为________ 。
(1)标准状况下112mL气体A的质量为0.32g,则A气体的摩尔质量为
(2)标准状况下有四种气体:①6.72LC2H6;②3.01×1024个HCl分子;③0.2molH2S;④10.2gNH3。各气体中氢原子数的大小顺序为(用①②③④表示):
(3)在300mL由NaCl、MgCl2、AlCl3组成的混合液中,部分离子浓度大小如图所示,回答下列问题。

①该混合液中AlCl3的物质的量为
②向①中稀释后的溶液中加入过量氢氧化钠溶液,则发生反应的离子方程式为:
您最近半年使用:0次
计算题
|
适中
(0.65)
【推荐3】某溶液含 Mg2+、Al3+,向其中滴加a mLC1mol·L—1NaOH之后,改成滴加C2mol·L—1H2SO4溶液,所得沉淀Y(mol)与所加试剂总体积V(mL)间的关系如下图所示。据此,回答下列问题:
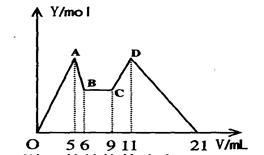
(1)C-D过程中的离子方程式________________________ ;
(2)n(Mg2+)/ n(Al3+) =______________ ;
(3)C1/C2=______________ ;
(4)所加入NaOH溶液的体积a=______________ mL。

(1)C-D过程中的离子方程式
(2)n(Mg2+)/ n(Al3+) =
(3)C1/C2=
(4)所加入NaOH溶液的体积a=
您最近半年使用:0次



