某化肥厂以氨和空气(其中氧气的体积分数为0.2)为原料生产硝酸铵过程如下:
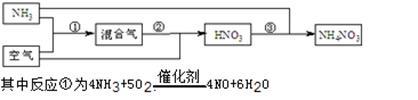
(1)步骤②发生了两个反应,将这两个化学方程式合并为一个化学方程式,可表示为_________ 。
(2)若不考虑副反应且各步反应均完全,为使生产过程中不再补充空气,则原料气中氨(包括第③步被硝酸吸收的氨)的体积分数最大值为______________ 。
(3)假设实际生产中,反应①、②中含氮物质的利用率分别为a、b,反应③中氨的利用率为c,硝酸的利用率为100%,则合成硝酸铵的整个流程中,氨的总利用率是____ 。(用含a,b,c的表示式)。

(1)步骤②发生了两个反应,将这两个化学方程式合并为一个化学方程式,可表示为
(2)若不考虑副反应且各步反应均完全,为使生产过程中不再补充空气,则原料气中氨(包括第③步被硝酸吸收的氨)的体积分数最大值为
(3)假设实际生产中,反应①、②中含氮物质的利用率分别为a、b,反应③中氨的利用率为c,硝酸的利用率为100%,则合成硝酸铵的整个流程中,氨的总利用率是
更新时间:2016-12-08 23:10:18
|
【知识点】 氮族元素及其化合物
相似题推荐
填空题
|
较难
(0.4)
解题方法
【推荐1】甲、乙两组同学分别对铜、铁与硝酸的反应进行探究,
请你参与并完成对有关问题的解答。
(1)甲组同学采用如图所示装置验证铜与硝酸的反应。已知仪器a中盛有足量一定浓度的硝酸溶液,试管b中盛有6.4g铜。
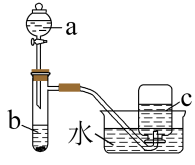
①仪器a的名称是________________ 。
②写出铜与浓硝酸反应的化学方程式_______ 。硝酸所表现出的化学性质主要有________ 。
③待试管b中反应进行完全,如果向b中液体里加入足量氢氧化钠溶液,可生成沉淀的质量是_____________ g。
(2)乙组同学对铁与稀硝酸的反应进行探究.他们用0.1mol Fe和含有0.3mol HNO3的稀硝酸进行实验,若两种物质恰好反应都无剩余,且HNO3只被还原成NO。则
①反应结束后的溶液中Fe3+、Fe2+的物质的量之比n(Fe3+):n(Fe2+) 为_____________ 。
②标准状况下,计算生成NO气体的体积____________________ 。(写出计算过程)
请你参与并完成对有关问题的解答。
(1)甲组同学采用如图所示装置验证铜与硝酸的反应。已知仪器a中盛有足量一定浓度的硝酸溶液,试管b中盛有6.4g铜。

①仪器a的名称是
②写出铜与浓硝酸反应的化学方程式
③待试管b中反应进行完全,如果向b中液体里加入足量氢氧化钠溶液,可生成沉淀的质量是
(2)乙组同学对铁与稀硝酸的反应进行探究.他们用0.1mol Fe和含有0.3mol HNO3的稀硝酸进行实验,若两种物质恰好反应都无剩余,且HNO3只被还原成NO。则
①反应结束后的溶液中Fe3+、Fe2+的物质的量之比n(Fe3+):n(Fe2+) 为
②标准状况下,计算生成NO气体的体积
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】下图中A~G是化合物,A是一种正盐,H是一种无色气态单质,C在高温下是气体,而常温下是一种无色液体, E为含钠的化合物。它们之间有如下转化关系:
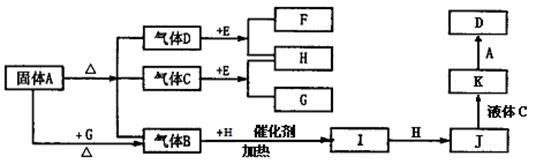
(1)实验室检验A的阳离子的一种方法为____________________________________________________________________________________________________________________________ 。
(2)K的浓溶液与碳单质反应的化学方程式______________________________ ,B与H催化氧化的化学方程式_______________________________________ 。上述转化中,属于氧化还原反应,且氧化剂和还原剂是同种物质的反应有________ 个。
(3)K的稀溶液中通入SO2气体,发生的化学反应的离子方程式为_________________________________________________________________________________________ 。
(4)H气体与H2S气体以4:5的体积比混合,电火花点燃后充分反应,发生反应的总的化学反应方程式为_________________________________________________________________ 。
(5)标准状况,将J与H按7:1的体积比充满烧瓶,将其倒置于盛有足量水的水槽中(假设进入烧瓶中的液体不扩散),实验结束后,烧瓶中溶液的物质的量浓度是___________ mol/L(计算结果保留3位小数)。

(1)实验室检验A的阳离子的一种方法为
(2)K的浓溶液与碳单质反应的化学方程式
(3)K的稀溶液中通入SO2气体,发生的化学反应的离子方程式为
(4)H气体与H2S气体以4:5的体积比混合,电火花点燃后充分反应,发生反应的总的化学反应方程式为
(5)标准状况,将J与H按7:1的体积比充满烧瓶,将其倒置于盛有足量水的水槽中(假设进入烧瓶中的液体不扩散),实验结束后,烧瓶中溶液的物质的量浓度是
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】在100mLNaOH溶液中加入NH4NO3和(NH4)2SO4的固体混合物,加热使之充分反应,下图表示加入固体的质量与产生气体的体积(标准状况)的关系。
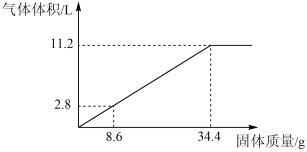
试计算:
(1) NaOH溶液的物质的量浓度是_______________ mol·L-1
(2) 当NaOH溶液为140mL,固体为51.6g时,充分反应产生的气体为______________ L(标准状况)
(3) 当NaOH溶液为180mL,固体仍为51.6g时,充分反应产生的气体为___________ L(标准状况)。

试计算:
(1) NaOH溶液的物质的量浓度是
(2) 当NaOH溶液为140mL,固体为51.6g时,充分反应产生的气体为
(3) 当NaOH溶液为180mL,固体仍为51.6g时,充分反应产生的气体为
您最近一年使用:0次



