甲、乙两组同学分别对铜、铁与硝酸的反应进行探究,
请你参与并完成对有关问题的解答。
(1)甲组同学采用如图所示装置验证铜与硝酸的反应。已知仪器a中盛有足量一定浓度的硝酸溶液,试管b中盛有6.4g铜。
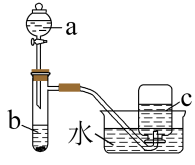
①仪器a的名称是________________ 。
②写出铜与浓硝酸反应的化学方程式_______ 。硝酸所表现出的化学性质主要有________ 。
③待试管b中反应进行完全,如果向b中液体里加入足量氢氧化钠溶液,可生成沉淀的质量是_____________ g。
(2)乙组同学对铁与稀硝酸的反应进行探究.他们用0.1mol Fe和含有0.3mol HNO3的稀硝酸进行实验,若两种物质恰好反应都无剩余,且HNO3只被还原成NO。则
①反应结束后的溶液中Fe3+、Fe2+的物质的量之比n(Fe3+):n(Fe2+) 为_____________ 。
②标准状况下,计算生成NO气体的体积____________________ 。(写出计算过程)
请你参与并完成对有关问题的解答。
(1)甲组同学采用如图所示装置验证铜与硝酸的反应。已知仪器a中盛有足量一定浓度的硝酸溶液,试管b中盛有6.4g铜。

①仪器a的名称是
②写出铜与浓硝酸反应的化学方程式
③待试管b中反应进行完全,如果向b中液体里加入足量氢氧化钠溶液,可生成沉淀的质量是
(2)乙组同学对铁与稀硝酸的反应进行探究.他们用0.1mol Fe和含有0.3mol HNO3的稀硝酸进行实验,若两种物质恰好反应都无剩余,且HNO3只被还原成NO。则
①反应结束后的溶液中Fe3+、Fe2+的物质的量之比n(Fe3+):n(Fe2+) 为
②标准状况下,计算生成NO气体的体积
更新时间:2023/03/18 22:59:29
|
相似题推荐
填空题
|
较难
(0.4)
【推荐1】NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其生产工艺如下:
(1) “合成”步骤可以得到ClO2,其反应的化学方程式为_____________________________ 。
(2) “电解”步骤阳极会生成一种气体,其化学式为____________ 。
(3) 反应生成的ClO2可用于高效脱除烟气中的SO2。以ClO2脱除SO2实验时SO2脱除率与溶液pH关系如右图所示。pH在3~7.6之间时,随pH增大,ClO2氧化性减弱,脱硫率降低。而当pH>7.6时,随pH增大,SO2脱除率又升高,其原因可能为_____________________________________ 。
(4) 国家标准规定产品中优级纯试剂纯度≥99.8%,分析纯试剂纯度≥99.7%,化学纯试剂纯度≥99.5%。为了确定某批次NaClO2产品的等级,研究小组设计测定方案如下:取10.00 g样品,用适量蒸馏水溶解后,加入略过量的KI溶液;充分反应后,将反应液定容至200 mL,取出20.00 mL于锥形瓶;向锥形瓶中滴加两滴淀粉溶液,用2.00 mol·L-1的Na2S2O3溶液与之反应,消耗Na2S2O3溶液22.00 ml。该样品可达________ 试剂纯度。(写出计算过程)
已知:ClO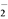 +4I-+4H+===2H2O+2I2+Cl-,I2+2S2O
+4I-+4H+===2H2O+2I2+Cl-,I2+2S2O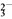 ===2I-+S4O
===2I-+S4O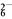
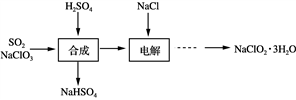
(1) “合成”步骤可以得到ClO2,其反应的化学方程式为
(2) “电解”步骤阳极会生成一种气体,其化学式为
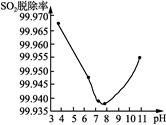
(3) 反应生成的ClO2可用于高效脱除烟气中的SO2。以ClO2脱除SO2实验时SO2脱除率与溶液pH关系如右图所示。pH在3~7.6之间时,随pH增大,ClO2氧化性减弱,脱硫率降低。而当pH>7.6时,随pH增大,SO2脱除率又升高,其原因可能为
(4) 国家标准规定产品中优级纯试剂纯度≥99.8%,分析纯试剂纯度≥99.7%,化学纯试剂纯度≥99.5%。为了确定某批次NaClO2产品的等级,研究小组设计测定方案如下:取10.00 g样品,用适量蒸馏水溶解后,加入略过量的KI溶液;充分反应后,将反应液定容至200 mL,取出20.00 mL于锥形瓶;向锥形瓶中滴加两滴淀粉溶液,用2.00 mol·L-1的Na2S2O3溶液与之反应,消耗Na2S2O3溶液22.00 ml。该样品可达
已知:ClO
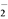 +4I-+4H+===2H2O+2I2+Cl-,I2+2S2O
+4I-+4H+===2H2O+2I2+Cl-,I2+2S2O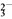 ===2I-+S4O
===2I-+S4O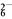
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】铜在化合物中的常见化合价有 、
、 。已知
。已知 与稀硫酸反应,溶液呈蓝色。
与稀硫酸反应,溶液呈蓝色。
(1)工业上可用 反应制取粗铜,该反应中
反应制取粗铜,该反应中_______ 元素被还原。
(2)将少量铜丝放入适量的稀硫酸中,温度控制在50℃,加入 溶液,一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜,该反应的离子方程式为
溶液,一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜,该反应的离子方程式为_______ 。温度控制在50~60℃的原因除了加快反应速率外,还有_______ 。在 溶液中加入一定量的
溶液中加入一定量的 和
和 溶液加热,生成
溶液加热,生成 沉淀,写出生成
沉淀,写出生成 的离子方程式:
的离子方程式:_______ 。
(3)现向 、
、 和
和 组成的混合物中,加入
组成的混合物中,加入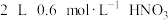 溶液恰好使混合物溶解,同时收集到
溶液恰好使混合物溶解,同时收集到 气体(标准状况)。
气体(标准状况)。 与稀硝酸反应的离方程式为
与稀硝酸反应的离方程式为_______ 。若混合物中含 ,将该混合物与稀硫酸充分反应,消耗
,将该混合物与稀硫酸充分反应,消耗 的物质的量为
的物质的量为_______  。
。
 、
、 。已知
。已知 与稀硫酸反应,溶液呈蓝色。
与稀硫酸反应,溶液呈蓝色。(1)工业上可用
 反应制取粗铜,该反应中
反应制取粗铜,该反应中(2)将少量铜丝放入适量的稀硫酸中,温度控制在50℃,加入
 溶液,一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜,该反应的离子方程式为
溶液,一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜,该反应的离子方程式为 溶液中加入一定量的
溶液中加入一定量的 和
和 溶液加热,生成
溶液加热,生成 沉淀,写出生成
沉淀,写出生成 的离子方程式:
的离子方程式:(3)现向
 、
、 和
和 组成的混合物中,加入
组成的混合物中,加入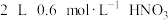 溶液恰好使混合物溶解,同时收集到
溶液恰好使混合物溶解,同时收集到 气体(标准状况)。
气体(标准状况)。 与稀硝酸反应的离方程式为
与稀硝酸反应的离方程式为 ,将该混合物与稀硫酸充分反应,消耗
,将该混合物与稀硫酸充分反应,消耗 的物质的量为
的物质的量为 。
。
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】酸性KMnO4、H2O2在生活、卫生医疗中常用作消毒剂,其中H2O2还可用于漂白,是化学实验室里必备的重要氧化试剂。高锰酸钾造成的污渍可用还原性的草酸(H2C2O4)去除,Fe(NO3)3也是重要的氧化试剂,下面是对这三种氧化剂性质的探究。
(1)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,写出该反应的离子方程式_______ ,氧化产物与还原产物的物质的量之比为_______ 。
(2)取300 mL 0.2 mol·L-1的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则转移电子的物质的量是_______ mol。
(3)在Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的原因是_______ (用文字表达),又变为棕黄色的离子方程式是_______ 。
(4)测定KMnO4样品的纯度可用标准Na2S2O3溶液进行滴定,配平下面方程式_______ 。
_______ +_______
+_______ +_______H+=_______Mn2++_______
+_______H+=_______Mn2++_______ +_______H2O
+_______H2O
(1)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,写出该反应的离子方程式
(2)取300 mL 0.2 mol·L-1的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则转移电子的物质的量是
(3)在Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的原因是
(4)测定KMnO4样品的纯度可用标准Na2S2O3溶液进行滴定,配平下面方程式
_______
 +_______
+_______ +_______H+=_______Mn2++_______
+_______H+=_______Mn2++_______ +_______H2O
+_______H2O
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】某工业废水在不考虑水的电离及离子的水解时仅含下表离子中的5种,且各种离子的物质的量浓度相等,均为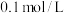 。
。
甲同学欲探究废水的组成,进行了如下实验:
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色的钴玻璃观察无紫色火焰。
Ⅱ.取少量溶液,加入 溶液无明显变化。
溶液无明显变化。
Ⅲ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中负离子种类不变。
Ⅳ.向Ⅲ中所得的溶液中加入 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。
完成下列填空:
(1)由Ⅰ、Ⅱ判断,溶液中一定不含有的正离子是___________ (写离子符号)。
(2)Ⅲ中加入少量盐酸生成无色气体的离子方程式是___________ 。
(3)在标准状态下收集Ⅲ中所得红棕色气体并将充满该气体的集气瓶倒扣入水中;气体变无色,反应的化学方程式为___________ 。
(4)反应结束后,集气瓶内溶液的物质的量浓度为___________ 。
(5)甲同学最终确定原溶液中所含正离子是___________ ,负离子是___________ 。(写离子符号)
(6)另取 原溶液,加入足量的
原溶液,加入足量的 溶液,充分反应后过滤、洗涤、灼烧至恒重,得到的固体质量为
溶液,充分反应后过滤、洗涤、灼烧至恒重,得到的固体质量为___________  。
。
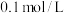 。
。| 正离子 |  、 、 、 、 、 、 、 、 |
| 负离子 |  、 、 、 、 、 、 |
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色的钴玻璃观察无紫色火焰。
Ⅱ.取少量溶液,加入
 溶液无明显变化。
溶液无明显变化。Ⅲ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中负离子种类不变。
Ⅳ.向Ⅲ中所得的溶液中加入
 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。完成下列填空:
(1)由Ⅰ、Ⅱ判断,溶液中一定不含有的正离子是
(2)Ⅲ中加入少量盐酸生成无色气体的离子方程式是
(3)在标准状态下收集Ⅲ中所得红棕色气体并将充满该气体的集气瓶倒扣入水中;气体变无色,反应的化学方程式为
(4)反应结束后,集气瓶内溶液的物质的量浓度为
(5)甲同学最终确定原溶液中所含正离子是
(6)另取
 原溶液,加入足量的
原溶液,加入足量的 溶液,充分反应后过滤、洗涤、灼烧至恒重,得到的固体质量为
溶液,充分反应后过滤、洗涤、灼烧至恒重,得到的固体质量为 。
。
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】氮的化合物在生产生活中有重要广泛运用。
(1)实验室用Cu、稀H2SO4、稀HNO3制备硫酸铜。先在大烧杯中放入铜,加入稀硫酸,再边搅拌边滴加稀硝酸至固体完全溶解,则最恰当的投料比n(H2SO4):n(HNO3)=___ 。
(2)12.8gCu与足量硝酸反应得到NO、NO2、N2O4混合气体4.256L(已折算为标准状况),将混合气体通入含0.2molNaOH的溶液中恰好被完全吸收,则参加反应的HNO3为___ mol。
(3)氨气具有一定还原性,在金属冶炼中因自身不产生污染,常作良好的还原剂,如用NH3热还原CuO的化学方程式为____ 。
(4)肼,又称联氨,化学式为N2H4,其电子式为___ 。联氨是一种二元弱碱,其电离方程式为:N2H4+H2O N2H
N2H +OH-,N2H
+OH-,N2H +H2O
+H2O N2H
N2H +OH-。联氨与硫酸反应生成一种碱式盐的化学式为
+OH-。联氨与硫酸反应生成一种碱式盐的化学式为____ 。
(5)肼—O2燃料电池是一种环境友好电池,介质为20%KOH溶液,其负极反应式为:___ 。
(1)实验室用Cu、稀H2SO4、稀HNO3制备硫酸铜。先在大烧杯中放入铜,加入稀硫酸,再边搅拌边滴加稀硝酸至固体完全溶解,则最恰当的投料比n(H2SO4):n(HNO3)=
(2)12.8gCu与足量硝酸反应得到NO、NO2、N2O4混合气体4.256L(已折算为标准状况),将混合气体通入含0.2molNaOH的溶液中恰好被完全吸收,则参加反应的HNO3为
(3)氨气具有一定还原性,在金属冶炼中因自身不产生污染,常作良好的还原剂,如用NH3热还原CuO的化学方程式为
(4)肼,又称联氨,化学式为N2H4,其电子式为
 N2H
N2H +OH-,N2H
+OH-,N2H +H2O
+H2O N2H
N2H +OH-。联氨与硫酸反应生成一种碱式盐的化学式为
+OH-。联氨与硫酸反应生成一种碱式盐的化学式为(5)肼—O2燃料电池是一种环境友好电池,介质为20%KOH溶液,其负极反应式为:
您最近一年使用:0次



