某校化学兴趣小组探究SO2与FeCl3溶液的反应,所用装置如下图所示。
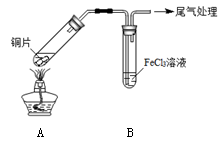
(1)该小组同学预测SO2与FeCl3溶液反应的现象为溶液由棕黄色变成浅绿色,然后开始实验。
FeCl3溶液显酸性的原因是_________。写出装置A中产生SO2的化学方程式:_________。
(2)当SO2通入到FeCl3溶液至饱和时,同学们观察到的现象是溶液由棕黄色变成红棕色,没有观察到丁达尔现象。将混合液放置12小时,溶液才变成浅绿色。
【查阅资料】 Fe(HSO3)2+离子为红棕色,它可以将Fe3+还原为Fe2+。生成Fe(HSO3)2+离子的反应为可逆反应。
解释SO2与FeCl3溶液反应生成红棕色Fe(HSO3)2+离子的原因:_____________________。
写出溶液中Fe(HSO3)2+离子与Fe3+反应的离子方程式:______________________________。
(3)为了探究如何缩短红棕色变为浅绿色的时间,该小组同学进行了步骤③的实验。
用铁氰化钾溶液检验步骤②和步骤③所得溶液中的Fe2+,其现象为_______________。
(4)综合上述实验探究过程,可以获得的实验结论:
I.SO2与FeCl3溶液反应生成红棕色中间产物Fe(HSO3)2+离子;
II.红棕色中间产物转变成浅绿色溶液是一个较慢的过程;
III._________________________________。

(1)该小组同学预测SO2与FeCl3溶液反应的现象为溶液由棕黄色变成浅绿色,然后开始实验。
| 步骤① | 配制1 mol·L-1 FeCl3溶液(未用盐酸酸化),测其pH约为1,取少量装入试管B中,加热A。 |
(2)当SO2通入到FeCl3溶液至饱和时,同学们观察到的现象是溶液由棕黄色变成红棕色,没有观察到丁达尔现象。将混合液放置12小时,溶液才变成浅绿色。
【查阅资料】 Fe(HSO3)2+离子为红棕色,它可以将Fe3+还原为Fe2+。生成Fe(HSO3)2+离子的反应为可逆反应。
解释SO2与FeCl3溶液反应生成红棕色Fe(HSO3)2+离子的原因:_____________________。
写出溶液中Fe(HSO3)2+离子与Fe3+反应的离子方程式:______________________________。
(3)为了探究如何缩短红棕色变为浅绿色的时间,该小组同学进行了步骤③的实验。
| 步骤② | 往5mL1mol·L-1 FeCl3溶液中通入SO2气体,溶液立即变为红棕色。微热3 min,溶液颜色变为浅绿色。 |
| 步骤③ | 往5mL重新配制的1mol·L-1 FeCl3溶液(用浓盐酸酸化)中通入SO2气体,溶液立即变为红棕色。几分钟后,发现溶液颜色变成浅绿色。 |
(4)综合上述实验探究过程,可以获得的实验结论:
I.SO2与FeCl3溶液反应生成红棕色中间产物Fe(HSO3)2+离子;
II.红棕色中间产物转变成浅绿色溶液是一个较慢的过程;
III._________________________________。
15-16高三上·北京海淀·期末 查看更多[2]
更新时间:2016-12-09 07:11:44
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
【推荐1】亚硝酸钠常用作食品防腐剂。现用下图所示仪器(夹持装置已省略)及药品。探究亚硝酸钠与硫酸的反应及生成气体产物的成分。已知气体液化的温度:NO2:21℃;NO:-152 ℃
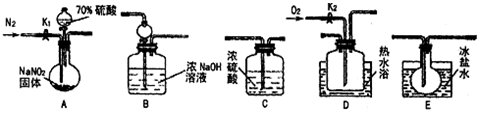
回答下列问题:
(1)为了检验装置A中生成的气体产物,仪器的连接顺序为(按从左到右连接): A→C→___ →____ →______ 。
(2)组装好仪器后,接下来进行的操作是____ ;实验开始时通入N2的作用是______ .
(3)关闭弹簧夹K1,打开分液漏斗活塞,滴入70%硫酸后,A中产生红棕色气体。确认A中产生的气体中含有NO,依据的现象是__________ ;装置E的作用是__________ 。
(4)根据上述实验,写出该反应的化学方程式:__________ 。
如果没有装置C,对验证结论造成的影响是__________ 。
(5)实验结束后还需通入N2的作用是_______ ;如果向D中通入过量O2,则装置B中发生反应的离子方程式为_____________ 。

回答下列问题:
(1)为了检验装置A中生成的气体产物,仪器的连接顺序为(按从左到右连接): A→C→
(2)组装好仪器后,接下来进行的操作是
(3)关闭弹簧夹K1,打开分液漏斗活塞,滴入70%硫酸后,A中产生红棕色气体。确认A中产生的气体中含有NO,依据的现象是
(4)根据上述实验,写出该反应的化学方程式:
如果没有装置C,对验证结论造成的影响是
(5)实验结束后还需通入N2的作用是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】用铁粉和氧水联合处理含氮( )酸性废水是目前环保领域广泛采用的一种方法,其主要过程如下:
)酸性废水是目前环保领域广泛采用的一种方法,其主要过程如下:
步骤一:向酸性废水中加入足量铁粉,生成 和铵盐;
和铵盐;
步骤二:向所得体系中加入饱和氯水,将 转化为
转化为 。
。
某科研小组在实验室中对该方法进行探究,回答下列问题:
查阅资料: 能传递电子;本实验条件下,铁粉表面的
能传递电子;本实验条件下,铁粉表面的 逐渐转化为不能传递电子的
逐渐转化为不能传递电子的 。
。
(1)用色谱分析法测得本实验所用酸性废水中 的质量浓度为
的质量浓度为 ,则其物质的量浓度为
,则其物质的量浓度为_______  。
。
(2)步骤一中,从溶液中分离出过量铁粉和 的操作所用玻璃仪器有烧杯、
的操作所用玻璃仪器有烧杯、_______ ;检验 中含有
中含有 (Ⅱ)的实验操作和现象为
(Ⅱ)的实验操作和现象为_______ 。
(3)步骤二中反应的离子方程式为_______ 。
(4)实验表明,步骤一向酸性废水中预先加入适量 ,可较大程度增大
,可较大程度增大 的转化率。为研究可能原因,某小组同学取甲,乙两份
的转化率。为研究可能原因,某小组同学取甲,乙两份 本实验所用酸性废水,向甲中加入足量铁粉;向乙中加入足量铁粉和
本实验所用酸性废水,向甲中加入足量铁粉;向乙中加入足量铁粉和 。实验测得甲中
。实验测得甲中 的转化率约为50%,乙中接近100%。
的转化率约为50%,乙中接近100%。
提出预测:
预测1:加入的 直接还原
直接还原 ;
;
预测2: 能将
能将 转化为
转化为 ;
;
预测3: 能将
能将 转化为
转化为 。
。
①由氧化还原反应理论通过定量分析推知预测1不成立,其具体过程为_______ 。
②将所取酸性废水乙中所加 用
用_______ 代替,即可证明预测2不成立。
③结合反应方程式和简单文字说明预测3成立,其原因为_______ 。
 )酸性废水是目前环保领域广泛采用的一种方法,其主要过程如下:
)酸性废水是目前环保领域广泛采用的一种方法,其主要过程如下:步骤一:向酸性废水中加入足量铁粉,生成
 和铵盐;
和铵盐;步骤二:向所得体系中加入饱和氯水,将
 转化为
转化为 。
。某科研小组在实验室中对该方法进行探究,回答下列问题:
查阅资料:
 能传递电子;本实验条件下,铁粉表面的
能传递电子;本实验条件下,铁粉表面的 逐渐转化为不能传递电子的
逐渐转化为不能传递电子的 。
。(1)用色谱分析法测得本实验所用酸性废水中
 的质量浓度为
的质量浓度为 ,则其物质的量浓度为
,则其物质的量浓度为 。
。(2)步骤一中,从溶液中分离出过量铁粉和
 的操作所用玻璃仪器有烧杯、
的操作所用玻璃仪器有烧杯、 中含有
中含有 (Ⅱ)的实验操作和现象为
(Ⅱ)的实验操作和现象为(3)步骤二中反应的离子方程式为
(4)实验表明,步骤一向酸性废水中预先加入适量
 ,可较大程度增大
,可较大程度增大 的转化率。为研究可能原因,某小组同学取甲,乙两份
的转化率。为研究可能原因,某小组同学取甲,乙两份 本实验所用酸性废水,向甲中加入足量铁粉;向乙中加入足量铁粉和
本实验所用酸性废水,向甲中加入足量铁粉;向乙中加入足量铁粉和 。实验测得甲中
。实验测得甲中 的转化率约为50%,乙中接近100%。
的转化率约为50%,乙中接近100%。提出预测:
预测1:加入的
 直接还原
直接还原 ;
;预测2:
 能将
能将 转化为
转化为 ;
;预测3:
 能将
能将 转化为
转化为 。
。①由氧化还原反应理论通过定量分析推知预测1不成立,其具体过程为
②将所取酸性废水乙中所加
 用
用③结合反应方程式和简单文字说明预测3成立,其原因为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】为研究铁质材料与热浓硫酸的反应,某学习小组用碳素钢(即铁和碳的合金)进行了以下探究活动:
探究一:
(1)将已去除表面氧化物的铁钉(碳素钢-含杂质碳)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是____________________________________________________ 。
(2)称取碳素钢6.0g放入15.0ml浓硫酸中,加热,充分反应后得到溶液X并收集到混合气体Y。
①甲同学认为X中除Fe3+之外还可能含有Fe2+。若要确认其中的Fe2+,应选用____________ (选填序号)。
A.KSCN溶液和氯水 B.铁粉和KSCN溶液 C.浓氨水 D.酸性KMnO4溶液
②乙同学取560mL(标准状况)气体Y通入足量溴水中,发生SO2+Br2+2H2O=2HBr+H2SO4反应,然后加入足量BaCl2溶液,经适当操作后得干燥固体4.66g。由此推知气体Y中SO2的体积分数的方法为_________________________________ 。
探究二:根据上述实验中SO2体积分数(80%)的分析,丙同学认为气体Y中还可能含有氢气和二氧化碳两种气体,为此设计了下列探究实验装置(假设有关气体完全反应)
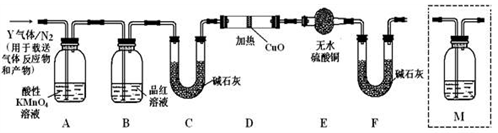
(3)装置B中试剂的作用是_______________________________________ ;
(4)分析Y气体中的CO2气体是如何生成的______ (用化学方程式表示)。
(5)已知洗气瓶M中盛装澄清石灰水,为确认CO2的存在,需在装置中添加洗气瓶M于____________ (填序号)。
A.A之前 B.A-B间 C.B-C间 D.C-D间
(6)如果气体Y中含有H2,预计实验现象应是_______________________ 。
探究一:
(1)将已去除表面氧化物的铁钉(碳素钢-含杂质碳)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是
(2)称取碳素钢6.0g放入15.0ml浓硫酸中,加热,充分反应后得到溶液X并收集到混合气体Y。
①甲同学认为X中除Fe3+之外还可能含有Fe2+。若要确认其中的Fe2+,应选用
A.KSCN溶液和氯水 B.铁粉和KSCN溶液 C.浓氨水 D.酸性KMnO4溶液
②乙同学取560mL(标准状况)气体Y通入足量溴水中,发生SO2+Br2+2H2O=2HBr+H2SO4反应,然后加入足量BaCl2溶液,经适当操作后得干燥固体4.66g。由此推知气体Y中SO2的体积分数的方法为
探究二:根据上述实验中SO2体积分数(80%)的分析,丙同学认为气体Y中还可能含有氢气和二氧化碳两种气体,为此设计了下列探究实验装置(假设有关气体完全反应)

(3)装置B中试剂的作用是
(4)分析Y气体中的CO2气体是如何生成的
(5)已知洗气瓶M中盛装澄清石灰水,为确认CO2的存在,需在装置中添加洗气瓶M于
A.A之前 B.A-B间 C.B-C间 D.C-D间
(6)如果气体Y中含有H2,预计实验现象应是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】(一)某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 mol/L 的溶液。在FeCl2溶液中需加入少量铁屑,其目的是__________________________ 。
(2)甲组同学取2mLFeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为_______________ 。
(3)乙组同学认为甲组的实验不够严谨,该组同学在2mLFeCl2溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是_____________ 。
(二)工业上用赤铁矿(含Fe2O3、FeO,也含有Al2O3、MnO2、CuO、SiO2等)制备绿矾FeSO4·7H2O的流程如下:

(4)氢氧化钠溶液加入赤铁矿中发生反应的离子方程式为____________ ;_________________ 。
(5)向滤渣Ⅰ中加入过量的试剂a为___________ ,过量的试剂b投入到滤液Ⅱ发生的所有反应的离子方程式为______________ ;_________________ ;________________ 。
(6)实验室中操作①②③的名称为_________________________ 。
(7)操作④隔绝空气的目的是_______________________________________________ 。
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 mol/L 的溶液。在FeCl2溶液中需加入少量铁屑,其目的是
(2)甲组同学取2mLFeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为
(3)乙组同学认为甲组的实验不够严谨,该组同学在2mLFeCl2溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是
(二)工业上用赤铁矿(含Fe2O3、FeO,也含有Al2O3、MnO2、CuO、SiO2等)制备绿矾FeSO4·7H2O的流程如下:

(4)氢氧化钠溶液加入赤铁矿中发生反应的离子方程式为
(5)向滤渣Ⅰ中加入过量的试剂a为
(6)实验室中操作①②③的名称为
(7)操作④隔绝空气的目的是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol/L的溶液.在FeCl2液中需加入少量铁粉,其目的是_______ 。
(2)甲组同学取2mlFeCl2溶液.加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为_______ 。
(3)乙组同学取10 mL0.1mol/L KI溶液,加入6mL0.1mol/L FeCl3溶液混合。分别取2mL此溶液于3 支试管中进行如下实验:
① 第一支试管中加入1mLCCl4充分振荡、静置,CCl4层呈紫色;
② 第二支试管中加入1滴KMnO4溶液,紫红色褪去;
③ 第三支试管中加入1滴KSCN溶液,溶液变红。
上述实验设计中不合理的是_______ (填序号);若在实验①中,将CCl4改为另一种试剂,颜色不同,但能起到相同的检测效果,该试剂是_______ ;结合药品用量及反应,预测产生实验③现象可能的原因为_______ 。
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol/L的溶液.在FeCl2液中需加入少量铁粉,其目的是
(2)甲组同学取2mlFeCl2溶液.加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为
(3)乙组同学取10 mL0.1mol/L KI溶液,加入6mL0.1mol/L FeCl3溶液混合。分别取2mL此溶液于3 支试管中进行如下实验:
① 第一支试管中加入1mLCCl4充分振荡、静置,CCl4层呈紫色;
② 第二支试管中加入1滴KMnO4溶液,紫红色褪去;
③ 第三支试管中加入1滴KSCN溶液,溶液变红。
上述实验设计中不合理的是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】某校化学兴趣小组探究SO2与FeCl3溶液的反应,所用装置如图所示:
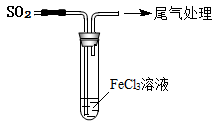
(1)该小组同学预测SO2与FeCl3溶液反应的现象为溶液由棕黄色变成浅绿色,发生反应的离子方程式为_______ 。
(2)按上图所示开始实验:
FeCl3溶液显酸性的原因是(用离子方程式表示)_______ 。
(3)当SO2通入到FeCl3溶液中,同学们观察到的现象是溶液立即由棕黄色变成红棕色。将混合液放置12小时,溶液才变成浅绿色。
【查阅资料】 Fe(HSO3)2+离子为红棕色,它可以将Fe3+还原为Fe2+。生成Fe(HSO3)2+离子的反应为可逆反应。
①请用化学用语表示SO2与FeCl3溶液反应生成红棕色Fe(HSO3)2+离子过程:_______ 。
②写出溶液中Fe(HSO3)2+离子与Fe3+反应的离子方程式:_______ 。
③请应用反应速率和反应限度知识解释产生上述实验现象的原因:_______ 。
(4)为了探究如何缩短红棕色变为浅绿色的时间,该小组同学进行了步骤③的实验。综合上述实验探究过程,可以获得的实验结论:
I.SO2与FeCl3溶液反应生成红棕色中间产物Fe(HSO3)2+离子;
II.红棕色中间产物转变成浅绿色溶液是一个较慢的过程;
III._______ 。

(1)该小组同学预测SO2与FeCl3溶液反应的现象为溶液由棕黄色变成浅绿色,发生反应的离子方程式为
(2)按上图所示开始实验:
| 步骤ⅰ | 配制1 mol·L-1 FeCl3溶液(未用盐酸酸化),测其pH约为1,取少量装入试管中。然后缓缓通入SO2气体。 |
| 步骤ⅱ | 往5mL1mol·L-1 FeCl3溶液中通入SO2气体,溶液立即变为红棕色。微热3 min,溶液颜色变为浅绿色。 |
| 步骤ⅲ | 往5mL重新配制的1mol·L-1 FeCl3溶液(用浓盐酸酸化)中通入SO2气体,溶液立即变为红棕色。几分钟后,发现溶液颜色变成浅绿色。 |
(3)当SO2通入到FeCl3溶液中,同学们观察到的现象是溶液立即由棕黄色变成红棕色。将混合液放置12小时,溶液才变成浅绿色。
【查阅资料】 Fe(HSO3)2+离子为红棕色,它可以将Fe3+还原为Fe2+。生成Fe(HSO3)2+离子的反应为可逆反应。
①请用化学用语表示SO2与FeCl3溶液反应生成红棕色Fe(HSO3)2+离子过程:
②写出溶液中Fe(HSO3)2+离子与Fe3+反应的离子方程式:
③请应用反应速率和反应限度知识解释产生上述实验现象的原因:
(4)为了探究如何缩短红棕色变为浅绿色的时间,该小组同学进行了步骤③的实验。综合上述实验探究过程,可以获得的实验结论:
I.SO2与FeCl3溶液反应生成红棕色中间产物Fe(HSO3)2+离子;
II.红棕色中间产物转变成浅绿色溶液是一个较慢的过程;
III.
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】某研究性学习小组在网上收集到如下信息:Fe(NO3)3溶液可以蚀刻银,制作美丽的银饰。他们对蚀刻银的原理进行了如下探究:
【实验】制备银镜,并与Fe(NO3)3溶液反应,发现银镜溶解。
【提出假设】
假设1:Fe3+具有氧化性,能氧化Ag。
假设2:Fe(NO3)3,溶液显酸性,在此酸性条件下NO3—能氧化Ag。
【设计实验方案,验证假设】
(1)甲同学从上述实验的生成物中检验出了Fe2+,验证了假设1成立。请写出Fe3+氧化Ag的离子方程式:_________________________________ 。
(2)乙同学设计实验验证假设2,请帮他完成下表中内容(提示:NO3—在不同条件下的还原产物较复杂,有时难以观察到气体产生)。
_______________________
【思考与交流】
(3)甲同学验证了假设1成立,若乙同学验证了假设2也成立,则丙同学由此得出结论:Fe(NO3)3溶液中的Fe3+和NO3—都氧化了Ag。你是否同意丙同学的结论,并简述理由:_________________ 。
【实验】制备银镜,并与Fe(NO3)3溶液反应,发现银镜溶解。
【提出假设】
假设1:Fe3+具有氧化性,能氧化Ag。
假设2:Fe(NO3)3,溶液显酸性,在此酸性条件下NO3—能氧化Ag。
【设计实验方案,验证假设】
(1)甲同学从上述实验的生成物中检验出了Fe2+,验证了假设1成立。请写出Fe3+氧化Ag的离子方程式:
(2)乙同学设计实验验证假设2,请帮他完成下表中内容(提示:NO3—在不同条件下的还原产物较复杂,有时难以观察到气体产生)。
| 实验步骤(不要求写具体操作过程) | 预期现象和结论 |
| ① ② …… | 若银镜消失,假设2成立; 若银镜不消失,假设2不成立 |
【思考与交流】
(3)甲同学验证了假设1成立,若乙同学验证了假设2也成立,则丙同学由此得出结论:Fe(NO3)3溶液中的Fe3+和NO3—都氧化了Ag。你是否同意丙同学的结论,并简述理由:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】某化学小组同学对乙醛与新制氢氧化铜悬浊液反应的实验进行探究。
(一)溶液配制:
(1)配制200 mL 0.1 mol/L 溶液,需用托盘天平称量胆矾(
溶液,需用托盘天平称量胆矾( )
)_______ g,用到的玻璃仪器除量筒、玻璃棒和胶头滴管外,还必须使用_______ 、_______ 。
(二)该小组同学用配制的 溶液制取新制氢氧化铜悬浊液,并和乙醛反应。在实验过程中,反应体系呈现蓝色浊液→黄绿色浊液→亮黄色浊液→橙黄色浊液的反常现象,同学们针对这一现象设计实验进行探究。
溶液制取新制氢氧化铜悬浊液,并和乙醛反应。在实验过程中,反应体系呈现蓝色浊液→黄绿色浊液→亮黄色浊液→橙黄色浊液的反常现象,同学们针对这一现象设计实验进行探究。
[查阅资料]a. 。
。
b.乙醛在NaOH溶液中会发生反应,随温度升高,生成一种树脂状物质,该物质为黄色油状固体,易黏附于滤纸,需用乙醇溶液洗涤才能透过滤纸。
[实验探究]可用试剂:
A.2 mL 10% NaOH溶液 B.4~6滴0.1 mol/L 溶液
溶液
C.0.5 mL乙醛 D.50%乙醇溶液
(2)iii__________ ,iv_________
[实验思考]氢氧化钠与乙醛的副反应严重干扰了对 沉淀的观察,为进一步了解
沉淀的观察,为进一步了解 和树脂状物质的生成受温度影响情况,该小组同学又设计了以下实验。
和树脂状物质的生成受温度影响情况,该小组同学又设计了以下实验。
注:“+”号的多少表示沉淀的相对多少
[实验结论]
(3)树脂状物质的生成温度_______ (填“高于”“低于”或“等于”) 的生成温度。
的生成温度。
[实验改进]
(4)为更好地观察到 沉淀颜色,可进行的实验操作是
沉淀颜色,可进行的实验操作是_______ (任写一条)。
(一)溶液配制:
(1)配制200 mL 0.1 mol/L
 溶液,需用托盘天平称量胆矾(
溶液,需用托盘天平称量胆矾( )
)(二)该小组同学用配制的
 溶液制取新制氢氧化铜悬浊液,并和乙醛反应。在实验过程中,反应体系呈现蓝色浊液→黄绿色浊液→亮黄色浊液→橙黄色浊液的反常现象,同学们针对这一现象设计实验进行探究。
溶液制取新制氢氧化铜悬浊液,并和乙醛反应。在实验过程中,反应体系呈现蓝色浊液→黄绿色浊液→亮黄色浊液→橙黄色浊液的反常现象,同学们针对这一现象设计实验进行探究。[查阅资料]a.
 。
。b.乙醛在NaOH溶液中会发生反应,随温度升高,生成一种树脂状物质,该物质为黄色油状固体,易黏附于滤纸,需用乙醇溶液洗涤才能透过滤纸。
[实验探究]可用试剂:
A.2 mL 10% NaOH溶液 B.4~6滴0.1 mol/L
 溶液
溶液C.0.5 mL乙醛 D.50%乙醇溶液
| 实验编号 | 实验步骤 | 实验现象 |
| ⅰ | 取0.5 mL乙醛于试管中,直接加热至沸,冷却 | 无明显现象 |
| ⅱ | 取4〜6滴 0.1 mol/L  溶液、0.5 mL乙醛于试管中,加热至沸,冷却 溶液、0.5 mL乙醛于试管中,加热至沸,冷却 | 无明显现象 |
| ⅲ | 取_______(填试剂标号)于试管中,加热至沸,冷却 | 无色溶液→亮黄色浊液→橙黄色浊液,冷却24小时后,试管底部有约3粒黄豆大小的黄色油状固体 |
| ⅳ | 取_______(填试剂标号)于试管中,加热至沸,冷却,用50%乙醇溶液洗涤,过滤 | 蓝色浊液→黄绿色浊液→亮黄色浊液→橙黄色浊液,过滤后有砖红色沉淀,滤液放置24小时后,试管底部有约3粒黄豆大小的黄色油状固体 |
[实验思考]氢氧化钠与乙醛的副反应严重干扰了对
 沉淀的观察,为进一步了解
沉淀的观察,为进一步了解 和树脂状物质的生成受温度影响情况,该小组同学又设计了以下实验。
和树脂状物质的生成受温度影响情况,该小组同学又设计了以下实验。| 设定温度/℃ | 体系颜色变化 |  沉淀相对多少 沉淀相对多少 | 沉淀颜色 |
| 36 | 蓝色浊液一黄绿色浊液 | 无 | 蓝色 |
| 46 | 蓝色浊液—黄绿色浊液一亮黄色浊液 | +(极少) | 砖红色(略显蓝色) |
| 60 | 蓝色浊液一黄绿色浊液一亮黄色浊液 | ++(极少) | 砖红色 |
| 67 | 蓝色浊液一黄绿色浊液一亮黄色浊液一橙黄色浊液 | +++++++ | 砖红色 |
| 78 | 蓝色浊液一黄绿色浊液一亮黄色浊液一橙黄色浊液 | +++++++ | 褥红色 |
| 100 | 蓝色浊液一黄绿色浊液一亮黄色浊液一橙黄色浊液 | +++++++ | 砖红色 |
[实验结论]
(3)树脂状物质的生成温度
 的生成温度。
的生成温度。[实验改进]
(4)为更好地观察到
 沉淀颜色,可进行的实验操作是
沉淀颜色,可进行的实验操作是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】小明同学在“金属拓展阅读”活动中了解到:金属钠在常温下与水剧烈反应能生成一种可燃性气体。教师结合小明已有知识设计了下图所示装置进行实验。

【小资料】金属钠一般存放在煤油中或用石蜡封存,煤油的密度为0.8g/mL。
(1)问题:采取上述保存金属钠的方法中,煤油或石蜡的作用是__________ 。
(2)实验过程
(3)反思分析
金属钠与水反应的化学方程式为_____________ ;
反应结束,C中溶液的溶质是_________ (指示剂除外,写出所有可能)。

【小资料】金属钠一般存放在煤油中或用石蜡封存,煤油的密度为0.8g/mL。
(1)问题:采取上述保存金属钠的方法中,煤油或石蜡的作用是
(2)实验过程
| 操作 | 现象及解释 | |
| ① | 打开止水夹a及分液漏斗活塞,待液体充满大试管后,关闭止水夹a及分液漏斗活塞。 | 液体分层,钠熔成银白色小球,在液体分层的界面上方跳动,产生大量气泡,下层溶液变成红色,并逐渐被压入B中。由此可知金属钠的物理性质 |
| ② | 打开止水夹b,待B中部分溶液进入C中,迅速关闭止水夹b。 | 反应的化学方程式为 |
| ③ | 打开止水夹c。 | 反应的化学方程式为 |
| ④ | 将燃着的木条伸到导管尖嘴处,打开止水夹a; 在火焰上方罩一个干冷的烧杯。 | 气体燃烧,产生淡蓝色火焰 烧杯内壁有无色液滴生成,A中气体为氢气。 |
金属钠与水反应的化学方程式为
反应结束,C中溶液的溶质是
您最近一年使用:0次



