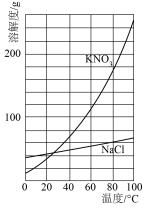
有一包白色粉末,可能是CuSO4、CaCO3、BaCl2、Na2SO4、KOH中的一种或几种,为证明其组成,进行如下实验:
(1)取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液,则白色沉淀可能是____________ ,原混合物中一定不含有_________ ;
(2)向实验(1)滤出的白色沉淀中加入足量的盐酸,沉淀全部溶解,并产生无色气体。则原混合物中一定含有______ 。 该反应的离子方程式为_____________ ;
(3)将实验(1)中得到的滤液分成两份,将实验(2)中产生的无色气体先通入其中的一份,无沉淀产生。气体导出后再通入另一份滤液中,立即产生白色沉淀,再过滤。出现上述现象的原因是实验(2)中产生的气体里含有________________ 。
(4)向实验(3)中过滤后所得的滤液里加入AgNO3溶液和稀硝酸,又产生白色沉淀,根据此现象推断,原混合物中一定还含有________ ,根据实验全过程推断,原混合物中还含有_______________ 。
(1)取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液,则白色沉淀可能是
(2)向实验(1)滤出的白色沉淀中加入足量的盐酸,沉淀全部溶解,并产生无色气体。则原混合物中一定含有
(3)将实验(1)中得到的滤液分成两份,将实验(2)中产生的无色气体先通入其中的一份,无沉淀产生。气体导出后再通入另一份滤液中,立即产生白色沉淀,再过滤。出现上述现象的原因是实验(2)中产生的气体里含有
(4)向实验(3)中过滤后所得的滤液里加入AgNO3溶液和稀硝酸,又产生白色沉淀,根据此现象推断,原混合物中一定还含有
更新时间:2016-12-09 07:13:43
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】近年来随着机动车经济的飞速发展,机动车的生产和使用量急剧增长,机动车排放的尾气对环境的污染日趋严重,机动车排气污染对环境和人们身体健康的危害已相当严重。汽车尾气的主要成分包括一氧化碳、二氧化碳、二氧化硫、一氧化氮、氮气以及铅和碳氢化合物等。回答下列问题:
(1)CO、CO2、SO2、NO几种气体中属于酸性氧化物的是____ (填化学式),CO2的结构式为____ 。
(2)Pb2+的离子结构示意图如图所示,由此可知铅在元素周期表中的位置为____ 。

(3)汽车尾气中的一种碳氢化合物其化学式为C8H18,写出该碳氢化合物分子含有6个甲基的结构简式____ ,该结构的二氯代物有____ 种。
(4)为了测定尾气中SO2的含量,某同学将汽车尾气缓慢通入盛有500mL0.1mol·L-1酸性KMnO4溶液的容器中,若通入尾气的气速为16L·min-1,经过5min溶液恰好完全褪色,假定尾气中的SO2被充分吸收且尾气中其他物质不与酸性KMnO4溶液反应,则SO2与酸性KMnO4溶液反应的离子方程式为____ ,该尾气中SO2的含量为____ g·L-1。
(1)CO、CO2、SO2、NO几种气体中属于酸性氧化物的是
(2)Pb2+的离子结构示意图如图所示,由此可知铅在元素周期表中的位置为

(3)汽车尾气中的一种碳氢化合物其化学式为C8H18,写出该碳氢化合物分子含有6个甲基的结构简式
(4)为了测定尾气中SO2的含量,某同学将汽车尾气缓慢通入盛有500mL0.1mol·L-1酸性KMnO4溶液的容器中,若通入尾气的气速为16L·min-1,经过5min溶液恰好完全褪色,假定尾气中的SO2被充分吸收且尾气中其他物质不与酸性KMnO4溶液反应,则SO2与酸性KMnO4溶液反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】“7•20”特大洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效措施之一。“84”消毒液、漂白粉和ClO2等都是有效的消杀试剂。
(1)用化学方程式表示氯气与烧碱溶液制备“84”消毒液的原理____ ,标况下56L氯气完全被吸收,需要____ L1mol/L的NaOH溶液。
(2)使用漂白粉漂白,只需取适量漂白粉溶于水即可,漂白原理用化学方程式表示为_____ 。
(3)漂白粉的保存要注意密封,为了判断一份儿久置的漂白粉是①没有失效②部分失效③完全失效。某化学兴趣小组设计实验进行验证。
已知:Ca(ClO)2溶液呈碱性;Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O;Ca(ClO)2+2HCl(稀)=CaCl2+2HClO
a.甲同学取适量漂白粉样品,滴加浓盐酸,将产生的气体直接通入澄清石灰水中,没有发现石灰水变浑浊。由此,判断结论为①,你是否同意他的结论____ (填“同意”或“不同意”),若不同意,你认为的结论是____ (若同意,此空不用填)
A.② B.③ C.①或② D.①②③均有可能
b.乙同学改用滴加稀盐酸,发现产生大量气泡,将气体通入澄清石灰水中,石灰水变浑浊;他又取少量漂白粉样品配成溶液,滴在pH试纸上,最终试纸变白。据此你得出的结论是_____ (从①②③中选填)。
(4)目前普遍使用ClO2代替Cl2及次氯酸盐作为广谱抗菌消毒剂,因为它安全、低毒,高效。其摩尔质量为_____ 。ClO2还可以将剧毒的NaCN转化为无毒物质除去,产物是氯化钠和两种常见气体。试写出该反应的化学方程式_____ 。
(1)用化学方程式表示氯气与烧碱溶液制备“84”消毒液的原理
(2)使用漂白粉漂白,只需取适量漂白粉溶于水即可,漂白原理用化学方程式表示为
(3)漂白粉的保存要注意密封,为了判断一份儿久置的漂白粉是①没有失效②部分失效③完全失效。某化学兴趣小组设计实验进行验证。
已知:Ca(ClO)2溶液呈碱性;Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O;Ca(ClO)2+2HCl(稀)=CaCl2+2HClO
a.甲同学取适量漂白粉样品,滴加浓盐酸,将产生的气体直接通入澄清石灰水中,没有发现石灰水变浑浊。由此,判断结论为①,你是否同意他的结论
A.② B.③ C.①或② D.①②③均有可能
b.乙同学改用滴加稀盐酸,发现产生大量气泡,将气体通入澄清石灰水中,石灰水变浑浊;他又取少量漂白粉样品配成溶液,滴在pH试纸上,最终试纸变白。据此你得出的结论是
(4)目前普遍使用ClO2代替Cl2及次氯酸盐作为广谱抗菌消毒剂,因为它安全、低毒,高效。其摩尔质量为
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐1】I.氢氧化铁胶体的制备步骤如下:
(1)用烧杯取少量蒸馏水,放在酒精灯上加热至沸腾;
(2)向烧杯中逐滴加入饱和FeCl3溶液;
(3)继续煮沸至液体是透明的红褐色,即得Fe(OH)3胶体.
回答下列问题:
①写出制备Fe(OH)3胶体的化学方程式_____________________ ;
②如何确定你制备的胶体是否成功?__________________________ ;
③若向Fe(OH)3胶体中逐滴加入H2SO4溶液会出现的现象:__________________ ;
II.描述下列反应的现象并写出反应的离子方程式:
①向NaHCO3溶液中加入NaHSO4溶液,现象______________ ,离子方程式___________ ;
②向FeCl3溶液中加入NaOH溶液,现象_______ ,离子方程式___________ 。
(1)用烧杯取少量蒸馏水,放在酒精灯上加热至沸腾;
(2)向烧杯中逐滴加入饱和FeCl3溶液;
(3)继续煮沸至液体是透明的红褐色,即得Fe(OH)3胶体.
回答下列问题:
①写出制备Fe(OH)3胶体的化学方程式
②如何确定你制备的胶体是否成功?
③若向Fe(OH)3胶体中逐滴加入H2SO4溶液会出现的现象:
II.描述下列反应的现象并写出反应的离子方程式:
①向NaHCO3溶液中加入NaHSO4溶液,现象
②向FeCl3溶液中加入NaOH溶液,现象
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】掌握电解质和非电解质的概念,能熟练判断一种物质是否是电解质是认识电解质的性质、研究离子反应的前提。以下有10种物质:①铜;②稀硫酸;③氯化氢;④氨气;⑤Na2CO3溶液;⑥CO2;⑦冰醋酸;⑧熔融的NaCl;⑨NH3·H2O;⑩Cl2。
按照表中提示的信息,把符合左栏条件的物质的序号填入右栏相应的位置。
按照表中提示的信息,把符合左栏条件的物质的序号填入右栏相应的位置。
序号 | 符合的条件 | 物质的序号 |
(1) | 电解质 | |
(2) | 非电解质 | |
(3) | 强电解质 | |
(4) | 弱电解质 | |
(5) | 既不是电解质也不是非电解质 | |
(6) | 能导电的物质 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】现有下列六种物质:①液态氯化氢;②二氧化碳;③硫酸铜溶液;④氢氧化铁胶体; ⑤KOH固体;⑥铁丝。
(1)上述六种物质中,属于电解质的有_______ (填序号,下同),属于非电解质的有_______ ,上述状态下能导电的有_______ 。
(2)区分③和④的简单方法是_______ 。
(3)氯化氢在水溶液中的电离方程式为_______ 。
(4)③和⑥反应的基本反应类型为_______ ,其离子方程式为_______ 。
(5)向③中加入⑤的水溶液的现象为_______ 。
(6)Cl2与⑤可能会发生如下反应,配平该方程式,并用双线桥标出电子得失:_______ 。
_______ _______
_______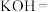 _______
_______ _______
_______ _______
_______ 。
。
(1)上述六种物质中,属于电解质的有
(2)区分③和④的简单方法是
(3)氯化氢在水溶液中的电离方程式为
(4)③和⑥反应的基本反应类型为
(5)向③中加入⑤的水溶液的现象为
(6)Cl2与⑤可能会发生如下反应,配平该方程式,并用双线桥标出电子得失:
_______
 _______
_______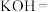 _______
_______ _______
_______ _______
_______ 。
。
您最近一年使用:0次

 )和甲苯(沸点为
)和甲苯(沸点为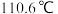 )的混合物。
)的混合物。