实验证明铜在低温下不能和O2发生反应,也不能和稀H2SO4共热发生反应,但工业上却是将废铜屑倒入热的稀硫酸中并不断通入空气来制取CuSO4溶液的,铜屑在此状态下发生的一系列化学反应为:______________ ,______________ 。利用铜和浓H2SO4在加热条件下也能制备CuSO4溶液,其化学方程式为______________ 。以上方法前者好还是后者好?原因是什么?______________________________________________
14-15高一上·吉林·期末 查看更多[2]
更新时间:2016-12-09 07:18:11
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】在“价一类”二维图中融入“杠杆模型”,可直观辨析部分物质转化及其定量关系。图中的字母分别代表硫及其常见化合物,e、f、g均为含钠元素的正盐,请回答:
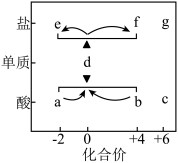
(1)当a溶液与b溶液混合时,可观察到的现象是___________ 。
(2)固体f露置在空气中易变质转化为g,该转化的化学方程式为___________ 。
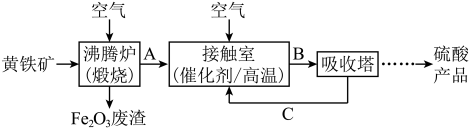
(3)工业上用黄铁矿( )为原料制备硫酸的流程如图所示,吸收塔中选择
)为原料制备硫酸的流程如图所示,吸收塔中选择___________ (填试剂名称)吸收 。
。
(4)将浓硫酸加入蔗糖中,有“黑面包”现象发生,该过程体现浓硫酸的性质是___________ 。
(5)煤和石油在燃烧过程中通常会产生 ,某同学利用下列装置测定空气中
,某同学利用下列装置测定空气中 的含量。
的含量。
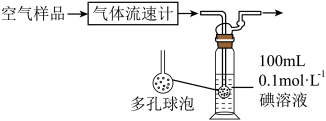
该装置中 与碘(
与碘( )溶液发生反应的化学方程式为:
)溶液发生反应的化学方程式为:___________ 。若空气流速为V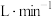 ,当
,当 与碘(
与碘( )溶液恰好完全反应时,耗时10min,则该空气样品中
)溶液恰好完全反应时,耗时10min,则该空气样品中 的含量是
的含量是___________  (用含V的最简表达式表示)。
(用含V的最简表达式表示)。

(1)当a溶液与b溶液混合时,可观察到的现象是
(2)固体f露置在空气中易变质转化为g,该转化的化学方程式为
(3)工业上用黄铁矿(
 )为原料制备硫酸的流程如图所示,吸收塔中选择
)为原料制备硫酸的流程如图所示,吸收塔中选择 。
。
(4)将浓硫酸加入蔗糖中,有“黑面包”现象发生,该过程体现浓硫酸的性质是
(5)煤和石油在燃烧过程中通常会产生
 ,某同学利用下列装置测定空气中
,某同学利用下列装置测定空气中 的含量。
的含量。
该装置中
 与碘(
与碘( )溶液发生反应的化学方程式为:
)溶液发生反应的化学方程式为: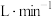 ,当
,当 与碘(
与碘( )溶液恰好完全反应时,耗时10min,则该空气样品中
)溶液恰好完全反应时,耗时10min,则该空气样品中 的含量是
的含量是 (用含V的最简表达式表示)。
(用含V的最简表达式表示)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】硫元素是动植物生长不可缺少的元素,广泛存在于自然界中。

(1)自然界中有斜方硫和单斜硫,它们的关系是__________________ ,二者转化属于_______ 变化。从图1中选择符合图2要求的X、Y代表的物质:X___________ ,Y___________ 。
(2)课堂上,老师取20g蔗糖放入烧杯中,加少量水使它润湿,注入10mL浓硫酸,搅拌,同学们看到蔗糖先变黑后“发酵”形成“黑面包”,同时还闻到了刺激性气味。这个实验中浓硫酸的作用有____________ 。
(3)为验证碳与浓硫酸在加热条件下生成的气体产物,同学们在老师指导下设计并进行如图实验:
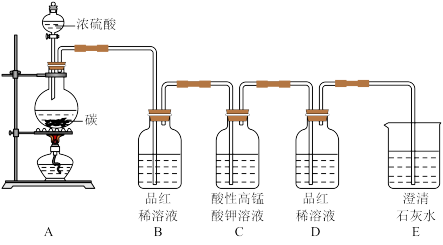
①请将能得出对应结论的实验现象填入表中。
②碳与浓硫酸反应的化学方程式是_____________________________________ 。
③C中酸性高锰酸钾溶液的作用是__________________________ 。若B、E中试剂交换,______ (填“能”或“不能”)得出有CO2产生的结论,理由是_____________________________ 。

(1)自然界中有斜方硫和单斜硫,它们的关系是
(2)课堂上,老师取20g蔗糖放入烧杯中,加少量水使它润湿,注入10mL浓硫酸,搅拌,同学们看到蔗糖先变黑后“发酵”形成“黑面包”,同时还闻到了刺激性气味。这个实验中浓硫酸的作用有
(3)为验证碳与浓硫酸在加热条件下生成的气体产物,同学们在老师指导下设计并进行如图实验:

①请将能得出对应结论的实验现象填入表中。
| 验证气体 | 实验现象 | 实验结论 |
| SO2 | 有SO2产生 | |
| CO2 | 有CO2产生 |
②碳与浓硫酸反应的化学方程式是
③C中酸性高锰酸钾溶液的作用是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某同学欲探究浓硫酸、稀硫酸、浓硝酸、稀硝酸分别与铁、铜反应的实验中的有关问题。
(1)在常温下,分别向盛有等量铁片的四支试管中加入等体积的①浓硫酸②稀硫酸③浓硝酸④稀硝酸,能观察到发生明显反应的是(填序号,下同)_____ 。
(2)先将铜与浓硫酸反应产生的气体X持续 通入如图装置中,一段时间后再将铜与浓硝酸反应产生的大量气体Y也持续通入该装置中,可观察到的现象包括_____ 。
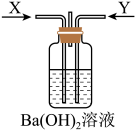
a.通入X气体后先产生白色沉淀后溶解
b.通入X气体后溶液中无明显现象
c.通入Y气体后有沉淀产生
d.通入Y气体后沉淀溶解
e.通入Y气体后溶液中无明显现象
(3)若将(2)的Ba(OH)2换为氢硫酸,则通入X气体后,反应的化学方程式为_____ 。
(4)将过量的铜置入一定量的浓硝酸中,充分反应
①反应后期的离子方程式为:_____ 。
②生成的NO2可与水发生反应,反应的化学方程式为_____ 。若该反应有0.6NA个电子转移,则被氧化的NO2的物质的量为______ 。
(1)在常温下,分别向盛有等量铁片的四支试管中加入等体积的①浓硫酸②稀硫酸③浓硝酸④稀硝酸,能观察到发生明显反应的是(填序号,下同)
(2)先将铜与浓硫酸反应产生的气体X

a.通入X气体后先产生白色沉淀后溶解
b.通入X气体后溶液中无明显现象
c.通入Y气体后有沉淀产生
d.通入Y气体后沉淀溶解
e.通入Y气体后溶液中无明显现象
(3)若将(2)的Ba(OH)2换为氢硫酸,则通入X气体后,反应的化学方程式为
(4)将过量的铜置入一定量的浓硝酸中,充分反应
①反应后期的离子方程式为:
②生成的NO2可与水发生反应,反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在浓硝酸中加入铜片,回答问题。
(1)开始反应的化学方程式为_________________________ ,实验现象为____________ 。
(2)待反应停止后,再加入少量质量分数为25%的稀硫酸,这时铜片上又有气泡产生,其原因是(用离子方程式表示)___________________________________ 。
(3)若将12.8 g铜跟一定量的浓硝酸反应,铜耗完时,共产生气体(NO和NO2的混合气体)5.6 L(标准状况),则所消耗的硝酸的物质的量是_______ ,所得气体的平均相对分子质量为_______ 。
(1)开始反应的化学方程式为
(2)待反应停止后,再加入少量质量分数为25%的稀硫酸,这时铜片上又有气泡产生,其原因是(用离子方程式表示)
(3)若将12.8 g铜跟一定量的浓硝酸反应,铜耗完时,共产生气体(NO和NO2的混合气体)5.6 L(标准状况),则所消耗的硝酸的物质的量是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】盐酸、硫酸和硝酸是中学阶段常见的三种强酸。请就三者与金属铜的反应情况,回答下列问题:
(1)①在100mL 18mol·L-1的浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准状况下的体积可能是______________
A.40.32L B. 6.72L C.20.16L D.30.24L
②若使上述反应①中剩余的铜片继续溶解,可向其中加入硝酸钠,写出反应的离子方程式______________________________ 。
(2) 若将过量铜粉与一定量浓硝酸反应,当反应完全停止时,共收集到的气体1.12L(标准状况),则该气体的成分是_________ ,反应中所消耗的硝酸的物质的量可能为______________
A. 0.25mol B. 0.2mol C.0.15mol D.0.1mol
(3) 某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解成蓝色溶液,该反应的化学方程式为_____________________ 。
(1)①在100mL 18mol·L-1的浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准状况下的体积可能是
A.40.32L B. 6.72L C.20.16L D.30.24L
②若使上述反应①中剩余的铜片继续溶解,可向其中加入硝酸钠,写出反应的离子方程式
(2) 若将过量铜粉与一定量浓硝酸反应,当反应完全停止时,共收集到的气体1.12L(标准状况),则该气体的成分是
A. 0.25mol B. 0.2mol C.0.15mol D.0.1mol
(3) 某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解成蓝色溶液,该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】在浓硝酸中放入铜片:
(1)开始反应时的化学方程式为__________________ 。
(2)若铜有剩余,则反应将要结束时的离子方程式为______________________ 。
(3)待反应停止后,再加入少量25%的稀硫酸,这时铜片上又有气泡产生,其原因是________________________ 。
(4)若将12.8 g铜跟一定量的浓硝酸反应,铜消耗完时,共产生5.6 L(标准状况)气体,则所消耗的HNO3的物质的量为________ ,其中表现氧化性的HNO3的物质的量为________ 。
(1)开始反应时的化学方程式为
(2)若铜有剩余,则反应将要结束时的离子方程式为
(3)待反应停止后,再加入少量25%的稀硫酸,这时铜片上又有气泡产生,其原因是
(4)若将12.8 g铜跟一定量的浓硝酸反应,铜消耗完时,共产生5.6 L(标准状况)气体,则所消耗的HNO3的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】按要求填空
(1)KAl(SO4)2的电离方程式:___________ 。
(2)NaHCO3的电离方程式:___________ 。
(3)铁与盐酸反应的离子方程式:___________ 。
(4)硫酸铜溶液与氢氧化钡溶液反应的离子方程式:___________ 。
(5)实验室制二氧化碳的反应的离子方程式:___________ 。
(6)家中用醋酸除水垢反应的离子方程式:___________ 。
(7)氧化亚铁与盐酸反应的离子方程式:___________ 。
(1)KAl(SO4)2的电离方程式:
(2)NaHCO3的电离方程式:
(3)铁与盐酸反应的离子方程式:
(4)硫酸铜溶液与氢氧化钡溶液反应的离子方程式:
(5)实验室制二氧化碳的反应的离子方程式:
(6)家中用醋酸除水垢反应的离子方程式:
(7)氧化亚铁与盐酸反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知:胆矾(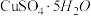 )易溶于水,难溶于乙醇。
)易溶于水,难溶于乙醇。
某小组用工业废铜焙烧得到的CuO(杂质为氧化铁及泥沙)为原料与稀硫酸反应制备胆矾,并利用热重分析法测定其结晶水的含量。
(1)将CuO加入到适量的稀硫酸中,加热,其主要反应的化学方程式为___________ ,与直接用废铜和浓硫酸反应相比,该方法的优点是___________ 。
(2)待CuO完全反应后停止加热,经过一些列处理得到滤液。滤液经如下实验操作:加热蒸发、___________ 、过滤、___________ 、干燥,得到胆矾。
(3)将制得的胆矾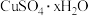 晶体进行热重分析,其热重曲线(即样品质量随温度变化曲线)如图所示。x=
晶体进行热重分析,其热重曲线(即样品质量随温度变化曲线)如图所示。x=___________ 。(结果保留2位小数)___________ (填标号)。
①胆矾未充分干燥 ②坩埚未置于干燥器中冷却 ③加热时有少胆矾迸溅出来
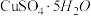 )易溶于水,难溶于乙醇。
)易溶于水,难溶于乙醇。某小组用工业废铜焙烧得到的CuO(杂质为氧化铁及泥沙)为原料与稀硫酸反应制备胆矾,并利用热重分析法测定其结晶水的含量。
(1)将CuO加入到适量的稀硫酸中,加热,其主要反应的化学方程式为
(2)待CuO完全反应后停止加热,经过一些列处理得到滤液。滤液经如下实验操作:加热蒸发、
(3)将制得的胆矾
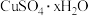 晶体进行热重分析,其热重曲线(即样品质量随温度变化曲线)如图所示。x=
晶体进行热重分析,其热重曲线(即样品质量随温度变化曲线)如图所示。x=
①胆矾未充分干燥 ②坩埚未置于干燥器中冷却 ③加热时有少胆矾迸溅出来
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】金属是非常有用的材料,以下是四种金属的相关性质。
完成下列填空:
(1)铝用作电线是利用了铝的_________ 性;铁用作炊具是利用了铁的_________ 性。
(2)工业上常以Cu为原料制备CuSO4,“绿色化学”要求从经济、技术和环保来设计可行的化学反应,生产应尽量减少对环境的副作用。下列反应符合“绿色化学”的是( )
A.Cu + 2H2SO4(浓) CuSO4 + SO2↑ + 2H2O
CuSO4 + SO2↑ + 2H2O
B.2Cu + O2 2CuO,CuO + H2SO4→CuSO4 +H2O
2CuO,CuO + H2SO4→CuSO4 +H2O
(3)常温下由于浓硫酸能使铁___________ ,因此浓硫酸可用铁槽车运输。
(4)钛是制造飞机的材料之一。根据表中数据,解释为何用钛来制造飞机。______________
(5)钢是主要含有铁的合金。汽车车身可以用铝或钢制造。已知铁在潮湿的空气中会迅速腐蚀,而铝不会。请解释铝耐腐蚀的原因。_______________________________________
(6)根据表中数据,描述用铝来取代钢制造汽车车身的一项优点和一项缺点。
优点:_____________________________________________________________________
缺点:_____________________________________________________________________
| 金属 | 熔点(℃) | 密度(g/cm3) | 相对强度 (1表示很弱) | 相对硬度 (1表示很软) | 每吨价格 (元) |
| 铝 | 660 | 2.7 | 11 | 2.8 | 11400 |
| 铜 | 1085 | 8.9 | 33 | 3.0 | 38000 |
| 铁 | 1538 | 7.9 | 20 | 4.5 | 4000 |
| 钛 | 1668 | 4.5 | 40 | 6.0 | 160000 |
完成下列填空:
(1)铝用作电线是利用了铝的
(2)工业上常以Cu为原料制备CuSO4,“绿色化学”要求从经济、技术和环保来设计可行的化学反应,生产应尽量减少对环境的副作用。下列反应符合“绿色化学”的是
A.Cu + 2H2SO4(浓)
 CuSO4 + SO2↑ + 2H2O
CuSO4 + SO2↑ + 2H2OB.2Cu + O2
 2CuO,CuO + H2SO4→CuSO4 +H2O
2CuO,CuO + H2SO4→CuSO4 +H2O(3)常温下由于浓硫酸能使铁
(4)钛是制造飞机的材料之一。根据表中数据,解释为何用钛来制造飞机。
(5)钢是主要含有铁的合金。汽车车身可以用铝或钢制造。已知铁在潮湿的空气中会迅速腐蚀,而铝不会。请解释铝耐腐蚀的原因。
(6)根据表中数据,描述用铝来取代钢制造汽车车身的一项优点和一项缺点。
优点:
缺点:
您最近一年使用:0次



