在2L的密闭容器中,进行如下化学反应:CO2(g)+H2(g)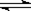 CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
回答下列问题:
(1)该反应的化学平衡常数表达式为K = 。
(2)该反应为 反应(选填“吸热”、“放热”)。反应达平衡后,若再通入一定量CO2,则平衡常数K将________,CO2的转化率________。(填“增大”、“减小”或“不变”)
(3)能判断该反应是否达到化学平衡状态的依据是 (多选扣分)。
a.容器中压强不变 b.混合气体中c(CO)不变 c.v正(H2)=v逆(H2O) d.c(CO2)=c(CO)
(4)若 600℃时,向容器中充入1mol CO、1mol H2O,反应达到平衡后,CO的转化率是 。
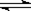 CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:| t℃ | 600 | 800 | 830 | 1000 | 1200 |
| K | 0.25 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K = 。
(2)该反应为 反应(选填“吸热”、“放热”)。反应达平衡后,若再通入一定量CO2,则平衡常数K将________,CO2的转化率________。(填“增大”、“减小”或“不变”)
(3)能判断该反应是否达到化学平衡状态的依据是 (多选扣分)。
a.容器中压强不变 b.混合气体中c(CO)不变 c.v正(H2)=v逆(H2O) d.c(CO2)=c(CO)
(4)若 600℃时,向容器中充入1mol CO、1mol H2O,反应达到平衡后,CO的转化率是 。
更新时间:2016-12-09 07:37:49
|
【知识点】 化学平衡
相似题推荐
填空题
|
较难
(0.4)
【推荐1】X是短周期中原子半径最小的元素,X、Y组成的气体甲能使湿润的红色石蕊试纸变蓝;
(1)Y的原子结构示意图是_______________ .
(2)甲的水溶液与硫酸铝溶液反应离子方程式________________ .
(3)甲与氯化氢反应生成乙.乙所含化学键类型有__________ .在0.1mol•L﹣1乙溶液中,所含离子浓度由大到小的顺序是_______________________ .
(4)工业上,可通过如下转化制得尿素晶体:
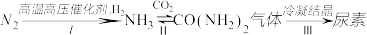
①Ⅰ中恒温恒容条件下,能同时提高化学反应速率和NH3产率的是_________ 。
②反应Ⅱ:2NH3(g)+ CO2(g) CO(NH2)2(g)+ H2O(g) △H1 = -536.1 kJ·mol-1
CO(NH2)2(g)+ H2O(g) △H1 = -536.1 kJ·mol-1
(i)此反应的平衡常数表达式K=__________ 。升高温度,K值_____ (填增大、减小或不变)。
(ii)尿素可用于处理汽车尾气。CO(NH2)2(g)与尾气中NO反应生成CO2、N2、H2O(g)排出。
已知:4NH3(g)+ 6NO(g)= 5N2(g)+ 6H2O(g) △H2 = -1806.4kJ·mol-1
写出CO(NH2)2(g)与NO反应的热化学方程式_______________________________ 。
(1)Y的原子结构示意图是
(2)甲的水溶液与硫酸铝溶液反应离子方程式
(3)甲与氯化氢反应生成乙.乙所含化学键类型有
(4)工业上,可通过如下转化制得尿素晶体:
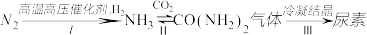
①Ⅰ中恒温恒容条件下,能同时提高化学反应速率和NH3产率的是
②反应Ⅱ:2NH3(g)+ CO2(g)
 CO(NH2)2(g)+ H2O(g) △H1 = -536.1 kJ·mol-1
CO(NH2)2(g)+ H2O(g) △H1 = -536.1 kJ·mol-1(i)此反应的平衡常数表达式K=
(ii)尿素可用于处理汽车尾气。CO(NH2)2(g)与尾气中NO反应生成CO2、N2、H2O(g)排出。
已知:4NH3(g)+ 6NO(g)= 5N2(g)+ 6H2O(g) △H2 = -1806.4kJ·mol-1
写出CO(NH2)2(g)与NO反应的热化学方程式
您最近半年使用:0次
填空题
|
较难
(0.4)
【推荐2】化学学科中的平衡理论主要内容包括:化学平衡、电离平衡、水解平衡和溶解平衡等四种。且均符合勒夏特列原理。请回答下列问题。
(1)一定温度下,在一个固定容积的密闭容器中,可逆反应A(g)+2B(g)⇌4C(g)∆H>0达到平衡时,c(A)="2mol/L," c(B)="7mol/L," c(C)=4mol/L。试确定B的起始浓度c(B)的取值范围是_________ ;若改变条件重新达到平衡后体系中C的体积分数增大,下列措施可行的是____
①增加C的物质的量 ②加 压 ③升温 ④使用催化剂
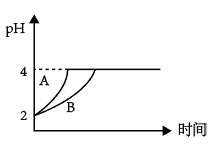
(2)常温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示。则图中表示醋酸溶液中pH变化曲线的是________ (填“A”或“B”)。设盐酸中加入的Zn质量为m1,醋酸溶液中加入的Zn质量为m2。则m1_____ m2(选填“<”、“=”、“>”)
(1)一定温度下,在一个固定容积的密闭容器中,可逆反应A(g)+2B(g)⇌4C(g)∆H>0达到平衡时,c(A)="2mol/L," c(B)="7mol/L," c(C)=4mol/L。试确定B的起始浓度c(B)的取值范围是
①增加C的物质的量 ②加 压 ③升温 ④使用催化剂
(2)常温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示。则图中表示醋酸溶液中pH变化曲线的是

您最近半年使用:0次
填空题
|
较难
(0.4)
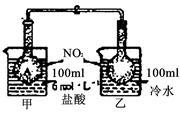
【推荐3】(1)如图所示,烧杯甲中盛放100 mL 6 mol·L-1的HCl溶液,烧杯乙中盛放100 mL冷水,现向烧杯甲的溶液中放入NaOH固体,同时向烧杯乙中放入NH4NO3固体,搅拌使之溶解。A瓶中气体颜色变深,B瓶气体颜色变浅,理由是:____________________ 。
(2)在恒温条件下将一定量NO2和N2O4的混合气体通入一容积为2 L的密闭容器中,反应物浓度随时间变化关系如下图。
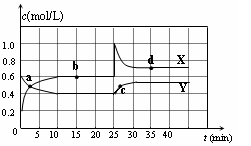
①图中的两条曲线,表示NO2浓度随时间的变化曲线______
②前10 min内用υ(N2O4)表示的化学反应速率为_______
③25 min时,NO2转变为N2O4的反应速率增大,其原因是_______
④15min时的平衡常数为__________ ,35min时的平衡常数为__________ 。
⑤在一定容积的密闭容器中,不能说明2NO2(g) N2O4(g)达到平衡状态的是
N2O4(g)达到平衡状态的是( )
E.υ(NO2)=2υ(N2O4)
F.c(NO2)=2 c(N2O4)

(2)在恒温条件下将一定量NO2和N2O4的混合气体通入一容积为2 L的密闭容器中,反应物浓度随时间变化关系如下图。

①图中的两条曲线,表示NO2浓度随时间的变化曲线
②前10 min内用υ(N2O4)表示的化学反应速率为
③25 min时,NO2转变为N2O4的反应速率增大,其原因是
④15min时的平衡常数为
⑤在一定容积的密闭容器中,不能说明2NO2(g)
 N2O4(g)达到平衡状态的是
N2O4(g)达到平衡状态的是| A.容器的压强不再变化 |
| B.容器的颜色不再变化 |
| C.混合气体的平均相对分子质量不再变化 |
| D.混合气体的密度不再变化 |
E.υ(NO2)=2υ(N2O4)
F.c(NO2)=2 c(N2O4)
您最近半年使用:0次



