在100 mL 0.5 mol/L AlCl3溶液中,加入100 mL NaOH溶液,得到1.56 g沉淀。求NaOH溶液的物质的量浓度。
更新时间:2016/12/09 07:39:26
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】A、B、C、W均为中学常见的纯净物,它们之间有如下转化关系(其他产物及反应条件已略去,反应可以在水溶液中进行)。
(1)若A为有刺激性气味的气体,其水溶液呈碱性;C为红棕色气体,与水反应生成一元强酸D,D具有强氧化性。
①实验室制取气体A的化学方程式_______ ;
②写出A→B的化学方程式为_______ ;
③将3.2g铜与60.0mL一定浓度D的溶液发生反应,铜完全溶解,产生B和C混合气体的体积为8.96L(标况)。待产生的气体全部释放后,向溶液加入100mL2.0mol/L的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原D溶液的物质的量浓度为_______ mol/L。
(2)若A、B、C的溶液均显碱性,焰色试验均呈黄色;C常作面包和糕点的发泡剂,受热分解可生成B。
①写出A溶液与C溶液反应的离子方程式_______ ;
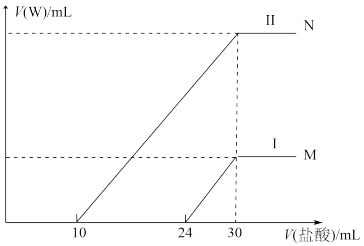
②向两份60mL同浓度的A溶液中通入不同体积的W气体,得到溶液M、N。向M、N溶液中逐滴加入浓度为0.25mol/L盐酸,如图所示Ⅰ和Ⅱ分别为加入V(盐酸)与产生V(W)的关系。则A溶液的物质的量浓度为_______ ,M、N两溶液中相同溶质的物质的量之比为_______ 。
(1)若A为有刺激性气味的气体,其水溶液呈碱性;C为红棕色气体,与水反应生成一元强酸D,D具有强氧化性。
①实验室制取气体A的化学方程式
②写出A→B的化学方程式为
③将3.2g铜与60.0mL一定浓度D的溶液发生反应,铜完全溶解,产生B和C混合气体的体积为8.96L(标况)。待产生的气体全部释放后,向溶液加入100mL2.0mol/L的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原D溶液的物质的量浓度为
(2)若A、B、C的溶液均显碱性,焰色试验均呈黄色;C常作面包和糕点的发泡剂,受热分解可生成B。
①写出A溶液与C溶液反应的离子方程式

②向两份60mL同浓度的A溶液中通入不同体积的W气体,得到溶液M、N。向M、N溶液中逐滴加入浓度为0.25mol/L盐酸,如图所示Ⅰ和Ⅱ分别为加入V(盐酸)与产生V(W)的关系。则A溶液的物质的量浓度为
您最近半年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】FeCl3是一种很重要的铁盐,主要用于污水处理,具有效果好、价格便宜等优点。工业上可将铁屑溶于盐酸中,先生成FeCl2,再通入Cl2氧化来制备FeCl3溶液。
(1)将标准状况下的aL氯化氢气体溶于100g水中,得到盐酸的密度为bg·mL-1,则该盐酸的物质的量浓度是______________________ 。
(2)向100mL的FeBr2溶液中通入标准状况下Cl23.36L,反应后的溶液中Cl-和Br-的物质的量浓度相等,则原FeBr2溶液的物质的量浓度为__________________ 。
(3)FeCl3溶液可以用来净水,其净水的原理为___________________________ (用离子方程式表示)。用100mL2mol·L-1的FeCl3溶液净水时,生成具有净水作用的微粒数________ (填“大于”“等于”或“小于”)0.2NA。
(4)ClO2对污水中Fe2+、Mn2+、S2-和CN-等有明显的去除效果。某工厂污水中含CN-bmg/L,现用ClO2将CN-氧化,只生成两种无毒气体,其离子反应方程式为________________ ,处理100m3这种污水,至少需要ClO2____ mol。
(1)将标准状况下的aL氯化氢气体溶于100g水中,得到盐酸的密度为bg·mL-1,则该盐酸的物质的量浓度是
(2)向100mL的FeBr2溶液中通入标准状况下Cl23.36L,反应后的溶液中Cl-和Br-的物质的量浓度相等,则原FeBr2溶液的物质的量浓度为
(3)FeCl3溶液可以用来净水,其净水的原理为
(4)ClO2对污水中Fe2+、Mn2+、S2-和CN-等有明显的去除效果。某工厂污水中含CN-bmg/L,现用ClO2将CN-氧化,只生成两种无毒气体,其离子反应方程式为
您最近半年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】(1)已知1.204×1023 个 X 气体分子的质量是 6.4 g,则X 气体的摩尔质量是:_______ ;
(2)同温同压下,同体积的甲烷 CH4气体和CO气体质量之比为_______ ,质子数之比_______ ;
(3)相同质量的 SO2、SO3 的氧原子的个数之比为_______ ;
(4)V L Al2(SO4)3 溶液中含 Al3+ a mol,该 Al2(SO4)3 溶液的物质的量浓度为_____ mol/L,取出 0.5V L 再加入水稀释到4V L,则稀释后的溶液中 SO 的物质的量浓度为
的物质的量浓度为_____ mol/L。
(2)同温同压下,同体积的甲烷 CH4气体和CO气体质量之比为
(3)相同质量的 SO2、SO3 的氧原子的个数之比为
(4)V L Al2(SO4)3 溶液中含 Al3+ a mol,该 Al2(SO4)3 溶液的物质的量浓度为
 的物质的量浓度为
的物质的量浓度为
您最近半年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】在100mL MgCl2和AlCl3的混和溶液中,逐滴加入NaOH溶液直至过量,经测定,加入NaOH物质的量和所得沉淀的物质的量的关系如图所示。回答下列问题。

(1)图中CD段反应的化学方程式为___________ ;C点存在的固体物质为________ 。
(2)A点的数据为_______ ;混合液中,MgCl2的浓度为_______ 。

(1)图中CD段反应的化学方程式为
(2)A点的数据为
您最近半年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】将氧化镁、氧化铝的混合物完全溶于200mL盐酸中,而后滴入1.0mol⋅L-1NaOH溶液,溶液中生成沉淀的物质的量随加入NaOH溶液的体积的变化趋势如图所示:
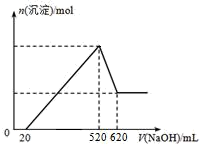
(1)最初加入20mLNaOH溶液所发生反应的离子方程式为___ 。
(2)所用盐酸的物质的量浓度为___ 。
(3)混合物中氧化镁、氧化铝的物质的量之比为__ 。

(1)最初加入20mLNaOH溶液所发生反应的离子方程式为
(2)所用盐酸的物质的量浓度为
(3)混合物中氧化镁、氧化铝的物质的量之比为
您最近半年使用:0次



