高温下,超氧化钾晶体(KO2)呈立方体结构(与NaCl晶体结构相似)。如图为超氧化钾晶体的一个晶胞。则有关下列说法不正确的是
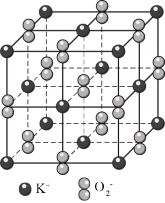

| A.KO2中既存在离子键也存在共价键 |
B.一个KO2晶胞中摊得的K+和 粒子数均为4个 粒子数均为4个 |
C.晶体中与每个K+距离最近的 有8个 有8个 |
| D.与K+距离相等且最近的K+有12个 |
更新时间:2016-12-09 07:40:37
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列各组晶体中,化学键类型相同,晶体类型也相同的是
A.HCHO、 | B.石墨、生铁 |
C. 、 、 | D. 、 、 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知 是
是 、
、 、
、 三种元素组成的离子化合物,只有
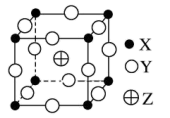
三种元素组成的离子化合物,只有 为金属元素,其晶胞如图,则下列推测错误的是
为金属元素,其晶胞如图,则下列推测错误的是
 是
是 、
、 、
、 三种元素组成的离子化合物,只有
三种元素组成的离子化合物,只有 为金属元素,其晶胞如图,则下列推测错误的是
为金属元素,其晶胞如图,则下列推测错误的是
A. 的化学式可能是 的化学式可能是 |
B.电负性: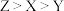 |
C.熔点:金刚石 干冰 干冰 |
D. 中可能存在离子键和共价键 中可能存在离子键和共价键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】钛铁基储氢合金是由钛、铁两种元素组成的金属间化合物。一种钛铁合金的晶胞如图ⅰ所示,该合金吸收的氢位于体心立方正八面体的中心,氢被4个钛原子和2个铁原子包围,如图ⅱ所示。不正确 的是

A.钛铁合金的化学式: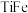 |
B.钛铁合金中每个 周围距离最近且等距的 周围距离最近且等距的 有8个 有8个 |
| C.钛铁合金与钛、铁的纯金属相比,熔点更低,硬度更大 |
D.如图ⅱ所示的每个体心立方正八面体均填充1个氢原子,则理论上形成的金属氢化物的化学式: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】关于晶体的自范性,下列叙述正确的是( )
| A.破损的晶体能自动变成规则的多面体 |
| B.缺角的氯化钠晶体在饱和NaCl溶液中慢慢变为完美的立方体晶块 |
| C.圆形容器中结出的冰是圆形的体现了晶体的自范性 |
| D.由玻璃制成规则的玻璃球体现了晶体的自范性 |
您最近一年使用:0次
【推荐1】有关晶体的结构如下图所示,下列说法中正确的是


| A.在NaCl晶体中,阳离子的配位数为8,阴离子的配位数为6 |
| B.在CaF2晶体中,每个晶胞平均占有4个Ca2+,F-的配位数是4 |
| C.在金刚石晶体中,每个碳原子被6个六元环共同占有,每个六元环最多有4个碳原子共面 |
| D.该气态团簇分子的分子式为EF或FE,其晶体不导电 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】镁铝合金具有优异的性能,其晶胞结构如图所示。下列说法不正确的是
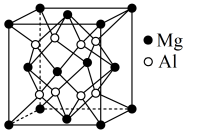
A.镁铝合金的化学式为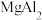 |
| B.熔点:氧化铝>氧化镁 |
| C.晶体中存在的化学键类型为金属键 |
D.该晶胞的质量是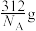 ( ( 表示阿伏加德罗常数的值) 表示阿伏加德罗常数的值) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】在20世纪90年代末期,科学家发现并证明碳有新的单质形态C60存在。后来人们又相继得到了C70、C76、C90、C94等另外一些球碳分子。21世纪初,科学家又发现了管状碳分子和洋葱状碳分子,大大丰富了碳元素单质的家族。下列有关说法错误的是
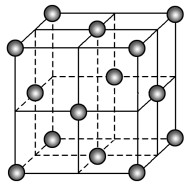

| A.熔点比较:C60<C70<C90<金刚石 |
| B.已知C(石墨)=C(金刚石) ΔH>0,则石墨比金刚石稳定 |
| C.C60晶体结构如图所示,每个C60分子周围与它最近且等距离的C60分子有10个 |
| D.金刚石、C60、C70、管状碳和洋葱状碳一定条件下都能燃烧 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某些物质的熔点数据如下表,据此做出的下列判断中错误的是( )
| Na2O | NaCl | AlF3 | AlCl3 |
| 920℃ | 801℃ | 1291℃ | 190℃ |
| BCl3 | SO2 | CO2 | SiO2 |
| -107℃ | 44.8℃ | -57℃ | 1723℃ |
| A.表中BCl3和CO2均是分子晶体 |
| B.同族元素的氧化物可形成不同类型的晶体 |
| C.只要由金属元素和非金属元素形成的晶体就一定是离子晶体 |
| D.不同族元素的氧化物可形成相同类型的晶体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列关于晶体的说法正确的是
| A.分子晶体中都存在共价键 |
| B.晶体中有阳离子,不一定有阴离子 |
| C.SiO2晶体中硅原子与硅氧键的数目比为1:2 |
| D.离子晶体CsCl中阴离子的配位数为6 |
您最近一年使用:0次

 溶液都可以除去乙烷中混有的乙烯
溶液都可以除去乙烷中混有的乙烯 ,B为
,B为 ,C为
,C为 。下列说法正确的是
。下列说法正确的是


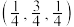
 主要用作分析试剂、脱毛剂,也可用于医药工业。其晶体具有如图所示的反萤石结构,已知晶胞参数为
主要用作分析试剂、脱毛剂,也可用于医药工业。其晶体具有如图所示的反萤石结构,已知晶胞参数为 ,
,

 之间的最短距离为
之间的最短距离为



