日用牙膏的主要成分有:活性物质、摩擦剂、甘油等。假设牙膏中摩擦剂成分为CaCO3、SiO2、Al(OH)3中的一种或几种物质组成,牙膏中其他成分均可溶于益酸,且无气体产生。
(1)牙膏中添加甘油主要作用____ 。
为进一步探究牙膏中摩擦剂成分,进行了以下探究:
I.摩擦剂成分的定性检验:设计实验方案,验证假设。请写出实验步骤以及预期现象和结论(可不填满也可补充)。可选的试剂:稀盐酸,稀硫酸,NaOH溶液,澄清石灰水
II.牙膏样品中碳酸钙的定量测定
利用如图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数。
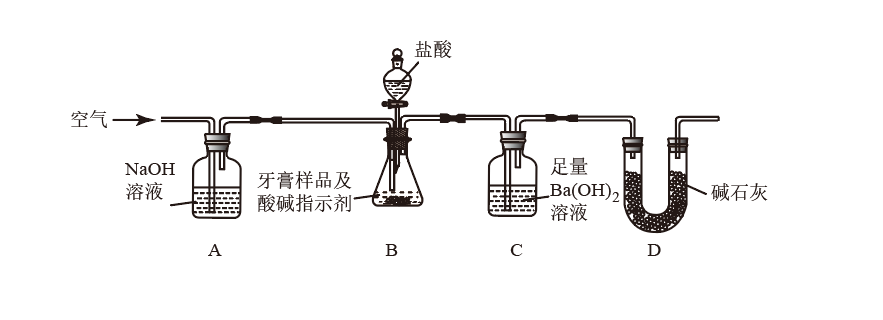
依据实验过程回答下列问题:
(2)实验过程中需持续缓缓通入空气。其主要作用____________ 。
(3)仪器C中选择Ba(OH)2而不选择Ca(OH)2溶液原因:①___________ 。②____________ 。
(4)下列各项措施中,能提高测定准确度的是____ (填标号)。
a.在加入盐酸之前,应排净装置内的CO2气体
b.缓慢滴加稀盐酸
c.在A-B之间增添盛有浓硫酸的洗气装置
d.在B-C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(5)实验中准确称取10.00g样品三份,进行三次测定,测得BaCO3平均质量为3.94g。则样品中碳酸钙的质量分数为____ 。若改测定C中生成BaCO3质量为测定装置C在吸收CO2前后的质量差来确定CaCO3的质量分数,两方法测定的结果____ (填“相同”或“不同”),原因是_____ 。
(1)牙膏中添加甘油主要作用
为进一步探究牙膏中摩擦剂成分,进行了以下探究:
I.摩擦剂成分的定性检验:设计实验方案,验证假设。请写出实验步骤以及预期现象和结论(可不填满也可补充)。可选的试剂:稀盐酸,稀硫酸,NaOH溶液,澄清石灰水
| 实验步骤 | 预期现象和结论 |
| 步骤1:取适量牙膏样品,加水充分搅拌、过滤 | 有难溶物存在 |
| 步骤2: | ①有无色气泡产生,说明有CaCO3; ② |
| 步骤3: | |
| …… |
利用如图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数。

依据实验过程回答下列问题:
(2)实验过程中需持续缓缓通入空气。其主要作用
(3)仪器C中选择Ba(OH)2而不选择Ca(OH)2溶液原因:①
(4)下列各项措施中,能提高测定准确度的是
a.在加入盐酸之前,应排净装置内的CO2气体
b.缓慢滴加稀盐酸
c.在A-B之间增添盛有浓硫酸的洗气装置
d.在B-C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(5)实验中准确称取10.00g样品三份,进行三次测定,测得BaCO3平均质量为3.94g。则样品中碳酸钙的质量分数为
更新时间:2016-12-09 07:49:23
|
【知识点】 探究物质组成或测量物质的含量解读
相似题推荐
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】氧化铬( )主要用于冶炼金属铬、有机化学合成的催化剂等。工业上以铬铁矿[主要成份:
)主要用于冶炼金属铬、有机化学合成的催化剂等。工业上以铬铁矿[主要成份: (亚铬酸亚铁),还含有
(亚铬酸亚铁),还含有 等杂质]为主要原料进行生产,其主要工艺流程如下:
等杂质]为主要原料进行生产,其主要工艺流程如下:
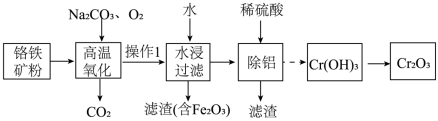
(1)基态 的核外电子排布式为
的核外电子排布式为_______ 。S8与热的浓NaOH溶液反应的产物之一为Na2S3,S 的空间结构为
的空间结构为_______ 。
(2)“高温氧化”过程中 转化为
转化为 的化学方程式为
的化学方程式为_______ 。
(3)“操作1”是将固体冷却、研磨,再加水浸取,其中研磨的目是_______ 。
(4)为获得纯净 ,需判断
,需判断 是否洗涤干净。该操作是
是否洗涤干净。该操作是_______ 。
(5)现用FeS模拟工业上处理含铬废水( )(浓度
)(浓度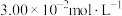 ),处理后所得滤渣主要成分为FeOOH,
),处理后所得滤渣主要成分为FeOOH, ,FeS。(已知:S元素被氧化为可溶性硫酸盐)
,FeS。(已知:S元素被氧化为可溶性硫酸盐)
①将滤渣用蒸馏水洗净后,在低温条件下干燥,将干燥后的固体在空气中加热,测得固体质量随温度的变化如图所示。
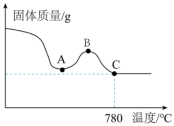
说明:780℃以上的残留固体为 、
、 的混合物。
的混合物。
A→B固体质量增加的原因是_______ 。
②IL的“废水”可氧化的FeS的质量为_______ g。
 )主要用于冶炼金属铬、有机化学合成的催化剂等。工业上以铬铁矿[主要成份:
)主要用于冶炼金属铬、有机化学合成的催化剂等。工业上以铬铁矿[主要成份: (亚铬酸亚铁),还含有
(亚铬酸亚铁),还含有 等杂质]为主要原料进行生产,其主要工艺流程如下:
等杂质]为主要原料进行生产,其主要工艺流程如下:
(1)基态
 的核外电子排布式为
的核外电子排布式为 的空间结构为
的空间结构为(2)“高温氧化”过程中
 转化为
转化为 的化学方程式为
的化学方程式为(3)“操作1”是将固体冷却、研磨,再加水浸取,其中研磨的目是
(4)为获得纯净
 ,需判断
,需判断 是否洗涤干净。该操作是
是否洗涤干净。该操作是(5)现用FeS模拟工业上处理含铬废水(
 )(浓度
)(浓度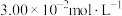 ),处理后所得滤渣主要成分为FeOOH,
),处理后所得滤渣主要成分为FeOOH, ,FeS。(已知:S元素被氧化为可溶性硫酸盐)
,FeS。(已知:S元素被氧化为可溶性硫酸盐)①将滤渣用蒸馏水洗净后,在低温条件下干燥,将干燥后的固体在空气中加热,测得固体质量随温度的变化如图所示。

说明:780℃以上的残留固体为
 、
、 的混合物。
的混合物。A→B固体质量增加的原因是
②IL的“废水”可氧化的FeS的质量为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】已知:①氧化亚铜在酸性条件下能发生歧化反应: ;②红热的铜能与氮的氧化物反应。某化学小组设计实验探究一氧化氮和铜反应的氧化产物,装置如图(部分夹持装置未画出)。
;②红热的铜能与氮的氧化物反应。某化学小组设计实验探究一氧化氮和铜反应的氧化产物,装置如图(部分夹持装置未画出)。
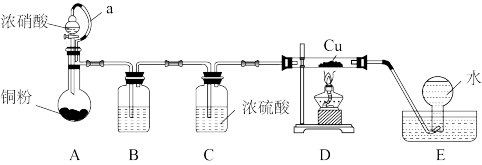
(1)①a管的作用是_______ ,②装置A中发生反应的离子方程式为_______ 。
(2)实验开始时,先打开A中分液漏斗活塞,过一会儿,点燃D处酒精灯,①这样操作的目的是_______ ,当Cu充分反应,实验结束时,②下列操作中应首先进行的是_______ (填序号)。
①停止滴加浓硝酸②熄灭酒精灯③从E装置中取出导气管
(3)为了探究氧化产物是否含有 ,取少量完全反应后的产物,进行如下实验:
,取少量完全反应后的产物,进行如下实验:
(甲)加入足量的稀硝酸,观察是否完全溶解
(乙)加入足量的稀硫酸,观察是否完全溶解
(丙)加入足量的浓硝酸,观察是否完全溶解
(丁)在加热条件下通入乙醇蒸气,观察固体是否变为红色。其中,能达到实验目的的是_______ (填代号)。
(4)查文献发现:铜与浓酸反应一旦发生就变快,是因为开始生成的 溶于水形成
溶于水形成 (弱酸,不稳定,易分解),它再和Cu反应,反应就加快。对生成
(弱酸,不稳定,易分解),它再和Cu反应,反应就加快。对生成 后反应变快的原因进行探究。
后反应变快的原因进行探究。
a.Ⅰ中加入的固体为_______ 。b.Ⅱ中“放置一段时间”的目的是_______ 。
实验Ⅰ、Ⅱ说明 氧化Cu的反应速率比
氧化Cu的反应速率比 氧化Cu快。
氧化Cu快。
(5)某同学将铜片放入盛有稀 的试管中,开始无明显现象,渐有小气泡产生,液面上方出现浅红棕色,溶液呈蓝色。结合上述实验,分析判断该反应慢的原因,除了硝酸浓度小、反应温度较低影响反应速率外,另一个重要原因是
的试管中,开始无明显现象,渐有小气泡产生,液面上方出现浅红棕色,溶液呈蓝色。结合上述实验,分析判断该反应慢的原因,除了硝酸浓度小、反应温度较低影响反应速率外,另一个重要原因是_______ 。
(6)若产物为CuO和 的混合物,取混合物5.92g与足量稀硝酸反应,测得生成448mL标准状况下NO气体,则CuO和
的混合物,取混合物5.92g与足量稀硝酸反应,测得生成448mL标准状况下NO气体,则CuO和 的物质的量之比为
的物质的量之比为_______ 。
 ;②红热的铜能与氮的氧化物反应。某化学小组设计实验探究一氧化氮和铜反应的氧化产物,装置如图(部分夹持装置未画出)。
;②红热的铜能与氮的氧化物反应。某化学小组设计实验探究一氧化氮和铜反应的氧化产物,装置如图(部分夹持装置未画出)。
(1)①a管的作用是
(2)实验开始时,先打开A中分液漏斗活塞,过一会儿,点燃D处酒精灯,①这样操作的目的是
①停止滴加浓硝酸②熄灭酒精灯③从E装置中取出导气管
(3)为了探究氧化产物是否含有
 ,取少量完全反应后的产物,进行如下实验:
,取少量完全反应后的产物,进行如下实验:(甲)加入足量的稀硝酸,观察是否完全溶解
(乙)加入足量的稀硫酸,观察是否完全溶解
(丙)加入足量的浓硝酸,观察是否完全溶解
(丁)在加热条件下通入乙醇蒸气,观察固体是否变为红色。其中,能达到实验目的的是
(4)查文献发现:铜与浓酸反应一旦发生就变快,是因为开始生成的
 溶于水形成
溶于水形成 (弱酸,不稳定,易分解),它再和Cu反应,反应就加快。对生成
(弱酸,不稳定,易分解),它再和Cu反应,反应就加快。对生成 后反应变快的原因进行探究。
后反应变快的原因进行探究。| 序号 | 实验操作 | 实验现象 |
| Ⅰ | 取B中溶液,加入一定量_______固体,再加入铜片 | 立即产生无色气体;液面上方呈红棕色 |
| Ⅱ | 取B中溶液,放置一段时间,溶液变为无色,再加入钢片 | 产生无色气体,较Ⅰ慢;液面上方呈浅红棕色 |
实验Ⅰ、Ⅱ说明
 氧化Cu的反应速率比
氧化Cu的反应速率比 氧化Cu快。
氧化Cu快。(5)某同学将铜片放入盛有稀
 的试管中,开始无明显现象,渐有小气泡产生,液面上方出现浅红棕色,溶液呈蓝色。结合上述实验,分析判断该反应慢的原因,除了硝酸浓度小、反应温度较低影响反应速率外,另一个重要原因是
的试管中,开始无明显现象,渐有小气泡产生,液面上方出现浅红棕色,溶液呈蓝色。结合上述实验,分析判断该反应慢的原因,除了硝酸浓度小、反应温度较低影响反应速率外,另一个重要原因是(6)若产物为CuO和
 的混合物,取混合物5.92g与足量稀硝酸反应,测得生成448mL标准状况下NO气体,则CuO和
的混合物,取混合物5.92g与足量稀硝酸反应,测得生成448mL标准状况下NO气体,则CuO和 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】某化学兴趣小组为研究生铁(含碳)与浓硫酸的反应情况及产物的性质,设计按如图所示装置进行实验(夹持装置及尾气处理装置未画出)。请回答下列问题:
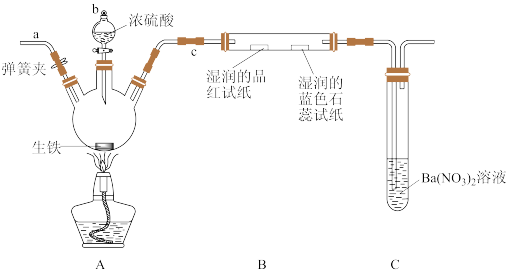
(1)仪器b的名称为_______ 。未点燃酒精灯前,A、B处均无明显现象,其原因是_______ 。点燃酒精灯后,实验过程中,观察到装置B中的现象是_______ ;装置C中有白色沉淀生成,该沉淀是_____ (填化学式),若装置C中盛放的溶液为溴水,发生反应的离子方程式为____ 。
(2)装置A中还会产生CO2气体,请写出产生CO2的化学方程式____ 。为了验证装置A中产生的气体中含CO2,应先从下列①~④中选出必要的装置连接A装置中c处管口,从左到右的顺序为_____ (填序号);连接装置后,为了赶尽装置中的空气,防止空气中的CO2影响实验,可从a处多次鼓入____ 。
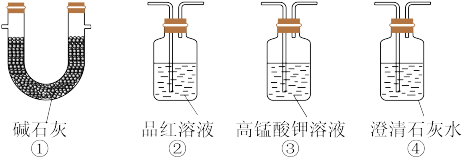
(3)有同学认为实验后期装置A中产生的气体中还可能含有H2,理由是_______ (用离子方程式表示)。
(4)某同学想利用下图所示的装置和其它常用实验仪器快速、准确地计算出铁的质量分数,最简便的实验操作是_______ (填字母)。
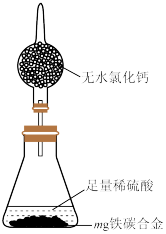
A.用排水法测定H2的体积
B.反应结束后,过滤、洗涤、干燥、称量残渣的质量
C.测定反应前后装置和药品的总质量

(1)仪器b的名称为
(2)装置A中还会产生CO2气体,请写出产生CO2的化学方程式

(3)有同学认为实验后期装置A中产生的气体中还可能含有H2,理由是
(4)某同学想利用下图所示的装置和其它常用实验仪器快速、准确地计算出铁的质量分数,最简便的实验操作是

A.用排水法测定H2的体积
B.反应结束后,过滤、洗涤、干燥、称量残渣的质量
C.测定反应前后装置和药品的总质量
您最近一年使用:0次



