氮的固定是几百年来科学家一直研究的课题。
(1)下表列举了不同温度下大气固氮和工业固氮的部分K值。
①分析数据可知:大气固氮反应属于__________ (填“吸热”或“放热”)反应。
②分析数据可知:人类不适合大规模模拟大气固氮的原因__________ 。
③从平衡视角考虑,工业固氮应该选择常温条件,但实际工业生产却选择500℃左右的高温,解释其原因_______________________ 。
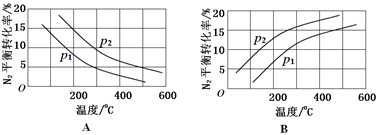
(2)工业固氮反应中,在其他条件相同时,分别测定N2的平衡转化率在不同压强(р1、р2)下随温度变化的曲线,下图所示的图示中,正确的是______ (填“A”或“B”);比较р1、р2的大小关系_______ 。
(3)近年,又有科学家提出在常温、常压、催化剂等条件下合成氨气的新思路,反应原理为:2N2(g)+6H2O(1) 4NH3(g)+3O2(g),则其反应热ΔH=
4NH3(g)+3O2(g),则其反应热ΔH=___________________ 。
(已知:N2(g)+3H2(g) 2NH3(g) △H=-92.4kJ·mol-1
2NH3(g) △H=-92.4kJ·mol-1
2H2(g) +O2(g) 2H2O(l) △H=-571.6kJ·mol-1 )
2H2O(l) △H=-571.6kJ·mol-1 )
(1)下表列举了不同温度下大气固氮和工业固氮的部分K值。
| 反应 | 大气固氮 N2 (g)+O2 (g)  2NO(g) 2NO(g) | 工业固氮 N2 (g)+3H2 (g)  2NH3(g) 2NH3(g) | |||
| 温度/℃ | 27 | 2000 | 25[ | 400 | 450 |
| K | 3.84×10-31 | 0.1 | 5×108 | 0.507 | 0.152 |
②分析数据可知:人类不适合大规模模拟大气固氮的原因
③从平衡视角考虑,工业固氮应该选择常温条件,但实际工业生产却选择500℃左右的高温,解释其原因
(2)工业固氮反应中,在其他条件相同时,分别测定N2的平衡转化率在不同压强(р1、р2)下随温度变化的曲线,下图所示的图示中,正确的是

(3)近年,又有科学家提出在常温、常压、催化剂等条件下合成氨气的新思路,反应原理为:2N2(g)+6H2O(1)
 4NH3(g)+3O2(g),则其反应热ΔH=
4NH3(g)+3O2(g),则其反应热ΔH=(已知:N2(g)+3H2(g)
 2NH3(g) △H=-92.4kJ·mol-1
2NH3(g) △H=-92.4kJ·mol-12H2(g) +O2(g)
 2H2O(l) △H=-571.6kJ·mol-1 )
2H2O(l) △H=-571.6kJ·mol-1 )
更新时间:2016-12-09 08:11:14
|
相似题推荐
填空题
|
较难
(0.4)
解题方法
【推荐1】按要求回答下列问题:
(1)航天员呼吸产生的 利用Bosch反应:
利用Bosch反应: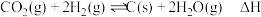 ,再电解水可实现
,再电解水可实现 的循环利用。热力学中规定由最稳定单质生成
的循环利用。热力学中规定由最稳定单质生成 某物质的焓变称为该物质的标准生成焓(符号:
某物质的焓变称为该物质的标准生成焓(符号: ),最稳定单质的标准生成焓规定为0。已知上述反应中:
),最稳定单质的标准生成焓规定为0。已知上述反应中: ;
; ,
, ;
; ,则
,则
_______  。
。
(2)乙苯催化脱氢制苯乙烯反应:
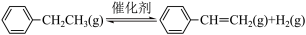
已知:
计算上述反应的
_______  。
。
(3)已知反应 的
的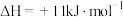 ,
, 、
、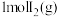 分子中化学键断裂时分别需要吸收
分子中化学键断裂时分别需要吸收 、
、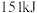 的能量,则
的能量,则 分子中化学键断裂时需吸收的能量为
分子中化学键断裂时需吸收的能量为_______  。
。
(1)航天员呼吸产生的
 利用Bosch反应:
利用Bosch反应: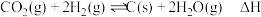 ,再电解水可实现
,再电解水可实现 的循环利用。热力学中规定由最稳定单质生成
的循环利用。热力学中规定由最稳定单质生成 某物质的焓变称为该物质的标准生成焓(符号:
某物质的焓变称为该物质的标准生成焓(符号: ),最稳定单质的标准生成焓规定为0。已知上述反应中:
),最稳定单质的标准生成焓规定为0。已知上述反应中: ;
; ,
, ;
; ,则
,则
 。
。(2)乙苯催化脱氢制苯乙烯反应:

已知:
| 化学键 |  |  |  |  |
键能/( ) ) | 412 | 348 | 612 | 436 |

 。
。(3)已知反应
 的
的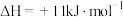 ,
, 、
、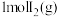 分子中化学键断裂时分别需要吸收
分子中化学键断裂时分别需要吸收 、
、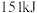 的能量,则
的能量,则 分子中化学键断裂时需吸收的能量为
分子中化学键断裂时需吸收的能量为 。
。
您最近半年使用:0次
【推荐2】高炉炼铁是重要的工业过程,冶炼过程中涉及如下反应:
①FeO(s)+CO(g) Fe(s)+CO2(g) ΔH1 =-11kJ/mol
Fe(s)+CO2(g) ΔH1 =-11kJ/mol
②FeO(s)+C(s) Fe(s)+CO(g) ΔH2=+161.5kJ/mol
Fe(s)+CO(g) ΔH2=+161.5kJ/mol
③C(s)+CO2(g) 2CO(g)
2CO(g)
(1)反应③的ΔH=___________ kJ/mol。
(2)在恒温恒容密闭容器中投入足量石墨与CO2进行反应③,可判定其达到平衡的条件有___________(填序号)。
(3)反应②的压力平衡常数表达式Kp2=___________ 。
(4)恒容密闭容器中加入足量C、FeO,进行上述反应。改变温度,测得平衡时容器总压的对数lg(p总/kPa)、各气体的物质的量分数x(CO)、x(CO2)的变化如图所示:
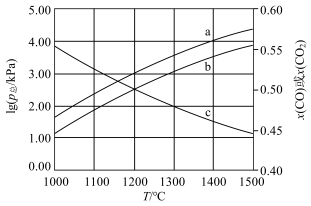
①x( CO)对应的曲线是___________ (填序号),判断依据是___________ 。
②在1200℃下进行上述反应,平衡时CO2分压为___________ kPa,反应①在此温度下的压力平衡常数Kp1 =___________ 。
(5)高炉炼铁过程中会生成“渗碳体”Fe3C (相对分子质量为M),晶胞为长方体 (如图),晶胞参数为a pm, b pm, c pm,阿伏加德罗常数为NA,则其密度为___________ g/cm3(用含M、a、b、c、NA的式子表示)。

①FeO(s)+CO(g)
 Fe(s)+CO2(g) ΔH1 =-11kJ/mol
Fe(s)+CO2(g) ΔH1 =-11kJ/mol②FeO(s)+C(s)
 Fe(s)+CO(g) ΔH2=+161.5kJ/mol
Fe(s)+CO(g) ΔH2=+161.5kJ/mol③C(s)+CO2(g)
 2CO(g)
2CO(g)(1)反应③的ΔH=
(2)在恒温恒容密闭容器中投入足量石墨与CO2进行反应③,可判定其达到平衡的条件有___________(填序号)。
| A.容器总压保持不变 |
| B.石墨断开3mol碳碳σ键的同时,CO断开2mol碳氧三键 |
| C.CO的体积分数保持不变 |
D.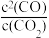 保持不变 保持不变 |
(4)恒容密闭容器中加入足量C、FeO,进行上述反应。改变温度,测得平衡时容器总压的对数lg(p总/kPa)、各气体的物质的量分数x(CO)、x(CO2)的变化如图所示:

①x( CO)对应的曲线是
②在1200℃下进行上述反应,平衡时CO2分压为
(5)高炉炼铁过程中会生成“渗碳体”Fe3C (相对分子质量为M),晶胞为长方体 (如图),晶胞参数为a pm, b pm, c pm,阿伏加德罗常数为NA,则其密度为

您最近半年使用:0次
填空题
|
较难
(0.4)
【推荐3】下表列出了断裂某些化学键所需的能量:
请回答下列问题:
(1)如图表示某反应的能量变化关系图,此反应为______ (填“放热”或“吸热”)反应,其中ΔH=______ kJ·mol-1(用含C和D的字母表示)。
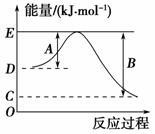
(2)若此能量变化关系图表示反应H2(g)+1/2O2(g)===H2O(g)
ΔH=-241.8 kJ·mol-1,则B=_______ kJ·mol-1,x=_____ 。
(3)表示Cl2与HI气体反应生成碘蒸气与氯化氢的____________ 。
| 化学键 | H—H | Cl-Cl | I—I | O=O | O—H | H-Cl | H—I |
| 断裂1 mol化学键所吸收的能量(kJ) | 436 | 247 | 151 | x | 463 | 431 | 299 |
请回答下列问题:
(1)如图表示某反应的能量变化关系图,此反应为

(2)若此能量变化关系图表示反应H2(g)+1/2O2(g)===H2O(g)
ΔH=-241.8 kJ·mol-1,则B=
(3)表示Cl2与HI气体反应生成碘蒸气与氯化氢的
您最近半年使用:0次
【推荐1】捕碳技术(主要指捕获CO2)在降低温室气体排放中具有重要的作用。
(1) 在海洋碳循环中,通过右图所示的途径固碳。

①写出钙化作用的离子方程式:___________________ 。
②同位素示踪法证实光合作用释放出的O2只来自于H2O。 用18O标记光合作用的化学方程式如下,将其补充完整。
__________ +__________  (CH2O)x+x18O2+ xH2O)
(CH2O)x+x18O2+ xH2O)
(2)工业上常用高浓度K2CO3溶液吸收CO2得到溶液X,再利用电解法使K2CO3溶液再生,并将CO2富集,其装置如下图。在阳极区发生的反应包括_________ 和H++HCO3-=H2O+CO2↑。简述 在阴极区再生的原理:
在阴极区再生的原理:______________ 。

(3)将上述富集的CO2和甲烷重整制合成气(CO和H2)是CO2资源化利用的有效途径。合成气用干制备甲醇的反应为:2H2(g) +CO (g) CH3OH(g) △H=-90.l kJ/mol
CH3OH(g) △H=-90.l kJ/mol
在T℃时,容积相同的甲、乙、丙三个恒容密闭容器中,按不同方式投入反应物,测得反应达到平衡时的有关数据如下表。
根据上表信息填空(填写“>”“< ”或“=”):
① 2c1_________ c3;②|x|+|y|___________ 90.1;
② ③2p2_________ p3;④α1+α2_________ 1
(1) 在海洋碳循环中,通过右图所示的途径固碳。

①写出钙化作用的离子方程式:
②同位素示踪法证实光合作用释放出的O2只来自于H2O。 用18O标记光合作用的化学方程式如下,将其补充完整。
 (CH2O)x+x18O2+ xH2O)
(CH2O)x+x18O2+ xH2O)
(2)工业上常用高浓度K2CO3溶液吸收CO2得到溶液X,再利用电解法使K2CO3溶液再生,并将CO2富集,其装置如下图。在阳极区发生的反应包括
 在阴极区再生的原理:
在阴极区再生的原理:
(3)将上述富集的CO2和甲烷重整制合成气(CO和H2)是CO2资源化利用的有效途径。合成气用干制备甲醇的反应为:2H2(g) +CO (g)
 CH3OH(g) △H=-90.l kJ/mol
CH3OH(g) △H=-90.l kJ/mol在T℃时,容积相同的甲、乙、丙三个恒容密闭容器中,按不同方式投入反应物,测得反应达到平衡时的有关数据如下表。
容器 | 甲 | 乙 | 丙 | |
起始反应物投入量 | 2 mol H2、1 mol CO | 1 mol CH3OH | 2 mol CH3OH | |
平 衡 数 据 | c(CH3OH)/mol/L | c1 | c2 | c3 |
反应的能量变化/kJ | x | y | z | |
体系压强/Pa | p1 | p2 | p3 | |
反应物转化率 | α1 | α2 | α3 | |
根据上表信息填空(填写“>”“< ”或“=”):
① 2c1
② ③2p2
您最近半年使用:0次
填空题
|
较难
(0.4)
【推荐2】近年来燃煤脱硫技术受到各界科研人员的重视,某脱硫技术涉及如下反应:
I CaSO4(s)+ CO(g) CaO(s)+SO2(g)+CO2(g) △H1=+218.4 kJ·mol-l
CaO(s)+SO2(g)+CO2(g) △H1=+218.4 kJ·mol-l
II CaO(s) +3CO(g)+SO2(g) CaS(s)+3CO2(g) △H2=-394.0 kJ·mol-l
CaS(s)+3CO2(g) △H2=-394.0 kJ·mol-l
(1)若用K1、K2分别表示反应I、II的化学平衡常数,则反应1/2CaSO4(s)+2CO(g) 1/2CaS(s)+2CO2(g)的平衡常数K=_________(用含K1、K2的式子表示)
1/2CaS(s)+2CO2(g)的平衡常数K=_________(用含K1、K2的式子表示)
(2)某温度下在一密闭容器中若只发生反应I,测得数据如下:
前20 s 内v(SO2)=__________mol·L-l·s-l,平衡时CO的转化率为__________。
(3)某科研小组研究在其它条件不变的情况下,改变起始一氧化碳物质的量,对反应IICaO(s) +3CO(g) +SO2 (g) CaS(s)+3CO2(g)的影响,实验结果如图所示(图中T表示温度):
CaS(s)+3CO2(g)的影响,实验结果如图所示(图中T表示温度):
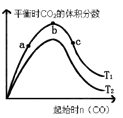
①比较在a、b、c三点所处的平衡状态中,反应物SO2的转化率最高的是_______________。
②图象中T2_____T1(填“高于”、“低于”、“等于”或 “无法确定”)判断的理由是____________________。
I CaSO4(s)+ CO(g)
 CaO(s)+SO2(g)+CO2(g) △H1=+218.4 kJ·mol-l
CaO(s)+SO2(g)+CO2(g) △H1=+218.4 kJ·mol-lII CaO(s) +3CO(g)+SO2(g)
 CaS(s)+3CO2(g) △H2=-394.0 kJ·mol-l
CaS(s)+3CO2(g) △H2=-394.0 kJ·mol-l(1)若用K1、K2分别表示反应I、II的化学平衡常数,则反应1/2CaSO4(s)+2CO(g)
 1/2CaS(s)+2CO2(g)的平衡常数K=_________(用含K1、K2的式子表示)
1/2CaS(s)+2CO2(g)的平衡常数K=_________(用含K1、K2的式子表示)(2)某温度下在一密闭容器中若只发生反应I,测得数据如下:
| t/s | 0 | 10 | 20 | 30 | 50 |
| c(CO)mol/L | 3 | 1.8 | 1.2 | 0.9 | 0.9 |
(3)某科研小组研究在其它条件不变的情况下,改变起始一氧化碳物质的量,对反应IICaO(s) +3CO(g) +SO2 (g)
 CaS(s)+3CO2(g)的影响,实验结果如图所示(图中T表示温度):
CaS(s)+3CO2(g)的影响,实验结果如图所示(图中T表示温度):
①比较在a、b、c三点所处的平衡状态中,反应物SO2的转化率最高的是_______________。
②图象中T2_____T1(填“高于”、“低于”、“等于”或 “无法确定”)判断的理由是____________________。
您最近半年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】氢气是未来理想的能源。
(1)实验室用铁与2mol·L-1的硫酸反应生成H2的物质的量与反应时间的关系如图所示。按要求回答下列问题。
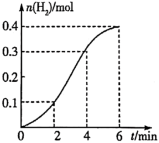
①产生H2的平均反应速率最大的时间段是___ (填“0~2min”“2~4min”或“4~6min”),该时间段内对反应速率起关键作用的影响因素是___ 。
②若向体系中加入少量硫酸铜溶液,可以加快氢气的生成速率,其原因是___ 。
③要加快上述实验中产生氢气的速率,还可采取的措施是__ (填一种)。
(2)工业上用海水制氢气的新技术的原理为2H2O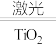 2H2↑+O2↑。回答下列问题:
2H2↑+O2↑。回答下列问题:
①分解海水的反应属于___ “反应(填“放热”或“吸热”)。
②分解产生的氢气储存比较困难,有一种储存方法的原理可表示为NaHCO3+H2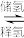 HCOONa+H2O。下列说法正确的是
HCOONa+H2O。下列说法正确的是__ (填序号)。
A.储氢、释氢过程中均有能量变化
B.储氢时反应物中只有离子键、非极性键的断裂
C.储氢过程中,NaHCO3被还原
D.释氢过程中,每消耗0.1molH2O放出2.24LH2
(3)H2可与I2发生反应:I2(g)+H2(g) 2HI(g)。一定温度下,在恒容密闭容器中进行该反应,下列叙述能说明该反应达到平衡的是
2HI(g)。一定温度下,在恒容密闭容器中进行该反应,下列叙述能说明该反应达到平衡的是___ (填序号)。
A.2v(H2)=v(HI)
B.断裂1molH—H键的同时形成1molI—I键
C.容器内气体的压强不变
D.容器内气体的颜色不变
(1)实验室用铁与2mol·L-1的硫酸反应生成H2的物质的量与反应时间的关系如图所示。按要求回答下列问题。

①产生H2的平均反应速率最大的时间段是
②若向体系中加入少量硫酸铜溶液,可以加快氢气的生成速率,其原因是
③要加快上述实验中产生氢气的速率,还可采取的措施是
(2)工业上用海水制氢气的新技术的原理为2H2O
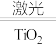 2H2↑+O2↑。回答下列问题:
2H2↑+O2↑。回答下列问题:①分解海水的反应属于
②分解产生的氢气储存比较困难,有一种储存方法的原理可表示为NaHCO3+H2
 HCOONa+H2O。下列说法正确的是
HCOONa+H2O。下列说法正确的是A.储氢、释氢过程中均有能量变化
B.储氢时反应物中只有离子键、非极性键的断裂
C.储氢过程中,NaHCO3被还原
D.释氢过程中,每消耗0.1molH2O放出2.24LH2
(3)H2可与I2发生反应:I2(g)+H2(g)
 2HI(g)。一定温度下,在恒容密闭容器中进行该反应,下列叙述能说明该反应达到平衡的是
2HI(g)。一定温度下,在恒容密闭容器中进行该反应,下列叙述能说明该反应达到平衡的是A.2v(H2)=v(HI)
B.断裂1molH—H键的同时形成1molI—I键
C.容器内气体的压强不变
D.容器内气体的颜色不变
您最近半年使用:0次



