铜是人类认识并应用最早的金属之一,我国是最早使用铜器的国家之一。铁与人类生活密切相关,几乎无处不在,是地壳中含量仅次于铝的金属。某研究性学习小组为了证明铁的金属活动性比铜强,设计了如下实验方案:
(1)将铁片置于硫酸铜溶液中有铜析出
(2)足量的铁粉和铜粉与浓硫酸在加热条件下反应分别生成FeSO4和CuSO4
(3)将铜片置于FeCl3溶液中铜片逐渐溶解
(4)把铁片和铜片置于盛有稀硫酸的烧杯中,并用导线连接,铁片上无气泡产生,而铜片上有气泡产生
(5)把铁片和铜片置于盛有浓硝酸的烧杯中,并用导线连接,铁片上有气泡产生,而铜片上无气泡产生
以上实验方案设计合理的有
(1)将铁片置于硫酸铜溶液中有铜析出
(2)足量的铁粉和铜粉与浓硫酸在加热条件下反应分别生成FeSO4和CuSO4
(3)将铜片置于FeCl3溶液中铜片逐渐溶解
(4)把铁片和铜片置于盛有稀硫酸的烧杯中,并用导线连接,铁片上无气泡产生,而铜片上有气泡产生
(5)把铁片和铜片置于盛有浓硝酸的烧杯中,并用导线连接,铁片上有气泡产生,而铜片上无气泡产生
以上实验方案设计合理的有
| A.两种 | B.三种 | C.四种 | D.五种 |
更新时间:2016-12-09 08:14:57
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列实验现象预测正确的个数是
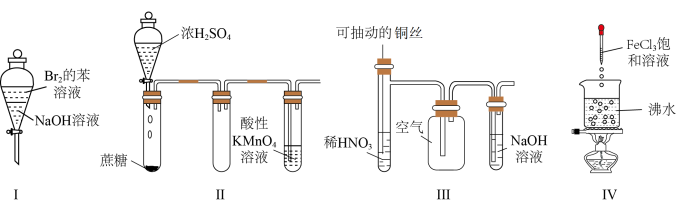
①实验 I :振荡后静置,上层溶液颜色变浅
②实验 II :酸性 KMnO4溶液中出现气泡,溶液的颜色无变化
③实验III:微热稀HNO3片刻,溶液中有气泡产生 ,广口瓶内始终保持无色
④实验IV:继续煮沸溶液至红褐色,停止加热,当光束通过体系时可产生丁达尔效应

①实验 I :振荡后静置,上层溶液颜色变浅
②实验 II :酸性 KMnO4溶液中出现气泡,溶液的颜色无变化
③实验III:微热稀HNO3片刻,溶液中有气泡产生 ,广口瓶内始终保持无色
④实验IV:继续煮沸溶液至红褐色,停止加热,当光束通过体系时可产生丁达尔效应
| A.1 | B.2 | C.3 | D.4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列方程式不能准确解释相应实验现象的是
| A.SO2气体通入Ba(NO3)2溶液中产生白色沉淀:SO2+BaCl2+H2O=BaSO3↓+2HCl |
| B.浓硝酸呈黄色的原因:4HNO3=4NO2↑+O2↑+2H2O |
| C.铜溶于浓硝酸所得溶液呈绿色:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O |
| D.将二氧化硫通入氢硫酸中产生黄色沉淀:2H2S+SO2=3S↓+2H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】根据实验操作及现象,下列结论中正确的是
| 选项 | 实验操作及现象 | 结论 |
| A | 向2 mL 0.1 mol·L  溶液中滴加几滴 0.1 mol·L 溶液中滴加几滴 0.1 mol·L  溶液,有白色沉淀产生,再滴加几滴 0.1 mol·L 溶液,有白色沉淀产生,再滴加几滴 0.1 mol·L  溶液,出现黑色沉淀 溶液,出现黑色沉淀 | 验证 |
| B | 取一定量 样品,溶解后加入 样品,溶解后加入 溶液,产生白色沉淀。加入浓 溶液,产生白色沉淀。加入浓 ,仍有沉淀 ,仍有沉淀 | 此样品中含有 |
| C | 将银和 溶液与铜和 溶液与铜和 溶液组成双液原电池。连通后银表面有银白色金属沉积,铜电极附近溶液逐渐变蓝 溶液组成双液原电池。连通后银表面有银白色金属沉积,铜电极附近溶液逐渐变蓝 | Cu的金属性比Ag强 |
| D | 向溴水中加入苯,振荡后静置,水层颜色变浅 | 溴与苯发生了加成反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】Fe和Mg与H2SO4反应的实验记录如下:
关于上述实验说法不合理 的是
| 实验 | 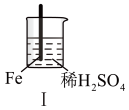 | 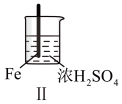 | 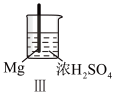 | 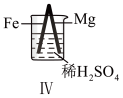 |
| 现象 | Fe表面产生大量无色气泡 | Fe表面产生少量气泡后迅速停止 | Mg表面迅速产生大量气泡 | Fe表面有大量气泡,Mg表面有少量气泡 |
| A.Ⅰ中产生气体的原因是:Fe+2H+=Fe2++H2↑ |
| B.取出Ⅱ中的铁棒放入CuSO4溶液立即析出亮红色固体 |
| C.Ⅲ中现象说明Mg在浓H2SO4中没被钝化 |
| D.Ⅳ中现象说明Mg的金属性比Fe强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】用NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.含0.2molH2SO4溶质的浓硫酸和足量铜加热反应,转移的电子数为0.2NA |
| B.常温常压下,22.4LNH3分子的电子数为10NA |
| C.1molN2与3molH2混合,充分反应后形成的N-H键数目为6NA |
| D.4.6gNO2和N2O4的混合气体中氧原子数为0.2NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】用锌片与1mol·L-l 稀盐酸反应制取氢气,下列措施不能使反应速率增大的是
| A.改用锌粉. | B.滴入几滴硫酸铜溶液 |
| C.加入少量1mol·L-1稀硫酸 | D.加入少量NaCl溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
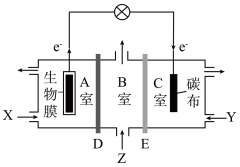
【推荐2】“绿水青山就是金山银山”,利用电池原理治理各种污染是今后科研的重要课题。某微生物电池在运行时可同时实现净化有机物污水、净化含Cr2O 废水(pH约为6)和淡化食盐水,其装置示意图如图。图中,D和E为阳离子交换膜或阴离子交换膜。已知Cr3+完全沉淀所需的pH为5.6。下列说法
废水(pH约为6)和淡化食盐水,其装置示意图如图。图中,D和E为阳离子交换膜或阴离子交换膜。已知Cr3+完全沉淀所需的pH为5.6。下列说法不正确 的是
 废水(pH约为6)和淡化食盐水,其装置示意图如图。图中,D和E为阳离子交换膜或阴离子交换膜。已知Cr3+完全沉淀所需的pH为5.6。下列说法
废水(pH约为6)和淡化食盐水,其装置示意图如图。图中,D和E为阳离子交换膜或阴离子交换膜。已知Cr3+完全沉淀所需的pH为5.6。下列说法
| A.C是正极室,E为阴离子交换膜 |
| B.X为有机物污水,Z为待淡化食盐水 |
C.理论上处理1mol的Cr2O 的同时可脱除6mol的NaCl 的同时可脱除6mol的NaCl |
D.C室的电极反应式为Cr2O +6e-+8H+=2Cr(OH)3↓+H2O +6e-+8H+=2Cr(OH)3↓+H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列实验操作和现象与实验结论一定正确的是
| 选项 | 操作 | 现象 | 结论 |
| A. | 向锌与稀硫酸的反应体系中加入少量硫酸铜 | 反应速率加快 | Cu2+是该反应的催化剂 |
| B. | 将苯加入到橙色的溴水中,充分振荡后静置 | 下层液体几乎无色 | 苯与Br2发生了取代反应 |
| C. | 向酸性KMnO4溶液中先通入少量SO2,充分反应后,再滴入几滴BaCl2溶液 | 产生白色沉淀 | SO2被氧化为 |
| D. | 室温下,向0.1 mol·L-1 HCl溶液中加入少量镁粉 | 产生大量气泡,测得溶液温度上升 | 镁与盐酸反应放热 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

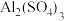 溶液中滴加过量稀氨水
溶液中滴加过量稀氨水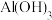 能溶于氨水
能溶于氨水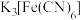 溶液
溶液
 被内焰中的乙醇蒸气氧化
被内焰中的乙醇蒸气氧化

