在如图所示的有关物质转化关系中,各物质均是我们中学化学所学的物质。C为一种黑色粉末,D为一种气体。
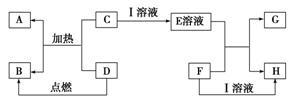
请根据框图中物质的转化关系及相关信息,用化学式填写下列空白:
(1)若F为可溶性碱,G为蓝色沉淀,则A为_________________ ;D可能为__________________ 。
(2)若G为蓝色沉淀,H为难溶性盐,则I为_________________ 。
(3)若G、H都属于盐,且G为蓝色溶液,则I可能为______________ ;F可能为_____________ 。

请根据框图中物质的转化关系及相关信息,用化学式填写下列空白:
(1)若F为可溶性碱,G为蓝色沉淀,则A为
(2)若G为蓝色沉淀,H为难溶性盐,则I为
(3)若G、H都属于盐,且G为蓝色溶液,则I可能为
更新时间:2016-12-09 08:49:31
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、C、D均为中学化学常见的纯净物,它们之间有如下转化关系(某些生成物已略去)

试回答:
(1)若A是非金属元素形成的化合物,且A与B、C在一定条件下都能反应生成一种无毒的气体。请写出下列化学方程式:
①C→D________________ ;
②A和C反应______________ 。
(2)若A是金属单质。
①向AlCl3溶液中滴加D的水溶液,能看到的现象是_________ ,理由是(用离子方程式表示)_____________ ;
②继续向所得溶液中通入足量的CO2气体,可看到的现象是____________ ,写出反应的离子方程式________________ 。

试回答:
(1)若A是非金属元素形成的化合物,且A与B、C在一定条件下都能反应生成一种无毒的气体。请写出下列化学方程式:
①C→D
②A和C反应
(2)若A是金属单质。
①向AlCl3溶液中滴加D的水溶液,能看到的现象是
②继续向所得溶液中通入足量的CO2气体,可看到的现象是
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】已知A、B、C、E的焰色反应均为黄色,其中B常用作食品的膨化剂,A与B按物质的量之比为1∶1混合并溶于足量水中,得到的溶液中只含有一种溶质。X为一种黑色固体单质,其氧化物参与大气循环,为温室气体。G为冶炼铁的原料,且为黑色晶体。G溶于盐酸中得到同种元素两种价态的化合物。A~H之间有如下的转化关系(部分物质未写出):
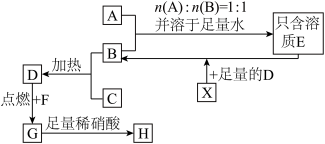
(1)写出下列物质的化学式:A___ ;C___ ;F___ 。
(2)在框图环境下,标准状况下得到11.2LD,则产生D的反应中,转移电子的物质的量为____ mol。
(3)写出A+B→E的离子方程式:____ 。
(4)写出C和B混合加热过程中的全部化学方程式:___ 。
(5)写出D→G转化的化学方程式:___ 。

(1)写出下列物质的化学式:A
(2)在框图环境下,标准状况下得到11.2LD,则产生D的反应中,转移电子的物质的量为
(3)写出A+B→E的离子方程式:
(4)写出C和B混合加热过程中的全部化学方程式:
(5)写出D→G转化的化学方程式:
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】A一J是中学化学中常见的物质,其相互转化关系如下图所示,反应条件均已略去。A、B常温下均为无色液体,且均由两种相同的元素组成;C、F、G均为非金属单质,常温下C、F为无色气体,G可用于制取“84”消毒液;D是应用最广泛的金属;J溶液中滴入KSCN 溶液显红色。
回答下列问题:
(1)A的化学式是_________ ,E 的俗称是_______ 。
(2)在空气中点燃F,然后把导管缓缓伸入盛满G的集气瓶中,观察到的实验现象是______ 。
(3)B和G能发生反应,写出反应的离子方程式______ 。
(4)G和I能发生反应,写出反应的化学方程式,并标出电子转移的方向和数目:______ 。

回答下列问题:
(1)A的化学式是
(2)在空气中点燃F,然后把导管缓缓伸入盛满G的集气瓶中,观察到的实验现象是
(3)B和G能发生反应,写出反应的离子方程式
(4)G和I能发生反应,写出反应的化学方程式,并标出电子转移的方向和数目:
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】海水中蕴藏着大量的财富,已发现含有80多种化学元素。海水晒得的粗盐中除少量泥沙外,还有少量的 、
、 、
、 等可溶性杂质离子。下图表示的是粗盐精制和利用苦卤水提取液溴的过程。
等可溶性杂质离子。下图表示的是粗盐精制和利用苦卤水提取液溴的过程。
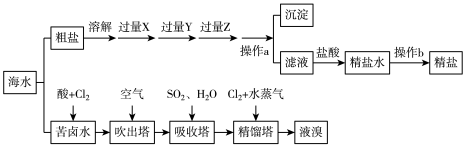
(1)在操作a与b中都用到的一种玻璃仪器是___________ ,其作用分别是___________ 、___________ 。
(2)实验室中保存液溴的方法是___________ 。
(3)“过量Y”若为过量的NaOH溶液,则Z为___________ (填试剂名称)。
(4)提取液溴的过程中两次通 ,这样做的目的是
,这样做的目的是___________ 。
(5)若要检验加入过量除杂试剂X、Y、Z后已将 除净,需取用少量待测液进行实验,请问取何处的少量待测液更好?
除净,需取用少量待测液进行实验,请问取何处的少量待测液更好?___________ (填“滤液”或“精盐水”),理由是___________ 。
 、
、 、
、 等可溶性杂质离子。下图表示的是粗盐精制和利用苦卤水提取液溴的过程。
等可溶性杂质离子。下图表示的是粗盐精制和利用苦卤水提取液溴的过程。
(1)在操作a与b中都用到的一种玻璃仪器是
(2)实验室中保存液溴的方法是
(3)“过量Y”若为过量的NaOH溶液,则Z为
(4)提取液溴的过程中两次通
 ,这样做的目的是
,这样做的目的是(5)若要检验加入过量除杂试剂X、Y、Z后已将
 除净,需取用少量待测液进行实验,请问取何处的少量待测液更好?
除净,需取用少量待测液进行实验,请问取何处的少量待测液更好?
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】三氧化硫(SO3)是生产硫酸重要的中间产物,熔点16.8℃,沸点44.8℃,与水反应的化学方程式为SO3+H2O=H2SO4。某小组设计了如图实验装置制备并吸收SO3(夹持仪器略)。回答下列问题:
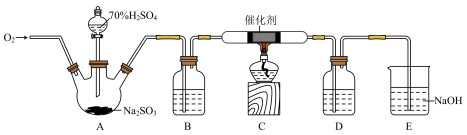
(1)盛放70%H2SO4的仪器名称是________ ,A中制备SO2的化学方程式为_________ 。
(2)装置B、D中盛放的试剂相同,该试剂是___________ 。
(3)O2除作反应物外,另一个作用是________ ,C中发生反应的化学方程式为________ 。
(4)对装置E中吸收液的成分进行探究,完成下表实验过程(限选试剂:稀盐酸、稀硫酸、稀硝酸、MgCl2溶液、BaCl2溶液、酸性KMnO4溶液、品红溶液、石蕊溶液)

(1)盛放70%H2SO4的仪器名称是
(2)装置B、D中盛放的试剂相同,该试剂是
(3)O2除作反应物外,另一个作用是
(4)对装置E中吸收液的成分进行探究,完成下表实验过程(限选试剂:稀盐酸、稀硫酸、稀硝酸、MgCl2溶液、BaCl2溶液、酸性KMnO4溶液、品红溶液、石蕊溶液)
| 操作步骤 | 实验现象 | 结论 |
| 取少量吸收液于试管中,滴加几滴MgCl2溶液 | 有白色沉淀生成 | 吸收液中含有NaOH |
| 取少量吸收液于试管中,滴加几滴酸性KMnO4溶液 | ① | 吸收液中含有② |
| 取少量吸收液于试管中,③ | ④ | 吸收液中含有Na2SO4 |
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO 、SO
、SO ,现取三份各100mL溶液进行如下实验:(已知:NH4++OH- = NH3↑+H2O)
,现取三份各100mL溶液进行如下实验:(已知:NH4++OH- = NH3↑+H2O)
第一份加入AgNO3溶液有沉淀产生。
第二份加足量NaOH溶液加热后,收集到0.08 mol气体。
第三份加足量BaCl2溶液后,得到干燥沉淀12.54 g,经足量盐酸洗涤、干燥后,沉淀质量为4.66 g。根据上述实验,回答以下问题:
(1)由第一份进行的实验推断该混合物是否一定含有Cl-_______ :
(2)由第二份进行的实验得知混合物中应含有_____________ 离子,其物质的量浓度为_____________ 。
(3)由第三份进行的实验可知12.54g沉淀的成分为_________________________ ,计算形成该沉淀的原混合物中各离子的物质的量_________________ 。
(4)综合上述实验,你认为以下结论正确的是( )
 、SO
、SO ,现取三份各100mL溶液进行如下实验:(已知:NH4++OH- = NH3↑+H2O)
,现取三份各100mL溶液进行如下实验:(已知:NH4++OH- = NH3↑+H2O)第一份加入AgNO3溶液有沉淀产生。
第二份加足量NaOH溶液加热后,收集到0.08 mol气体。
第三份加足量BaCl2溶液后,得到干燥沉淀12.54 g,经足量盐酸洗涤、干燥后,沉淀质量为4.66 g。根据上述实验,回答以下问题:
(1)由第一份进行的实验推断该混合物是否一定含有Cl-
(2)由第二份进行的实验得知混合物中应含有
(3)由第三份进行的实验可知12.54g沉淀的成分为
(4)综合上述实验,你认为以下结论正确的是
A.该混合液中一定含有:K+、NH 、CO 、CO 、SO 、SO ,可能含Cl-,且n(K+) ≥0.04mol ,可能含Cl-,且n(K+) ≥0.04mol |
B.该混合液中一定含有:NH 、CO 、CO 、SO 、SO ,可能含K+、Cl- ,可能含K+、Cl- |
C.该混合液中一定含有:NH 、CO 、CO 、SO 、SO ,可能含Mg2+、K+、Cl- ,可能含Mg2+、K+、Cl- |
D.该混合液中一定含有:NH 、 SO 、 SO ,可能含Mg2+、K+、Cl- ,可能含Mg2+、K+、Cl- |
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】CuSO4•5H2O是铜的重要化合物,有着广泛的应用.以下是CuSO4•5H2O的实验室制备流程图.
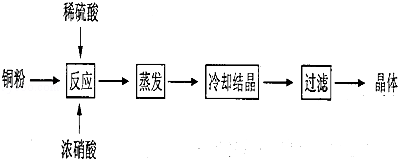
根据题意完成下列填空:
(1)向含铜粉的稀硫酸中滴加浓硝酸,在铜粉溶解时可以观察到的实验现象:_________ 、________ .
(2)如果铜粉、硫酸及硝酸都比较纯净,则制得的CuSO4•5H2O中可能存在的杂质是_____________ .
(3)已知:CuSO4+2NaOH═Cu(OH)2↓+Na2SO4
称取0.1000g提纯后的CuSO4•5H2O试样于锥形瓶中,加入0.1000mol/L氢氧化钠溶液啊28.00mL,反应完全后,过量的氢氧化钠用0.1000mol/L盐酸滴定至终点,耗用盐酸20.16mL,则0.1000g该试样中含CuSO4•5H2O_____ g.
(4)如果采用重量法测定CuSO4•5H2O的含量,完成下列步骤:
①_____________ ②加水溶解③加氯化钡溶液,沉淀④过滤(其余步骤省略)
在过滤前,需要检验是否沉淀完全,其操作是_______________ .

根据题意完成下列填空:
(1)向含铜粉的稀硫酸中滴加浓硝酸,在铜粉溶解时可以观察到的实验现象:
(2)如果铜粉、硫酸及硝酸都比较纯净,则制得的CuSO4•5H2O中可能存在的杂质是
(3)已知:CuSO4+2NaOH═Cu(OH)2↓+Na2SO4
称取0.1000g提纯后的CuSO4•5H2O试样于锥形瓶中,加入0.1000mol/L氢氧化钠溶液啊28.00mL,反应完全后,过量的氢氧化钠用0.1000mol/L盐酸滴定至终点,耗用盐酸20.16mL,则0.1000g该试样中含CuSO4•5H2O
(4)如果采用重量法测定CuSO4•5H2O的含量,完成下列步骤:
①
在过滤前,需要检验是否沉淀完全,其操作是
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】为探索工业含铝、铁、铜合金废料的再利用,某同学设计的实验方案如下:
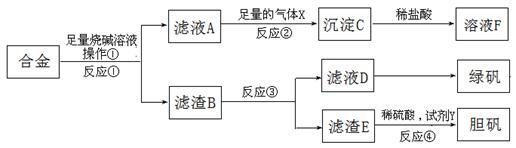
请回答:
(1)操作①用到的玻璃仪器有_________ 。
(2)写出反应①的化学方程式_________ ,反应②的离子反应方程式_________ 。
(3)在滤渣E中加入稀硫酸和试剂Y制胆矾晶体是一种绿色化学工艺,试剂Y为无色液体,反应④的总化学方程式是_________ 。

请回答:
(1)操作①用到的玻璃仪器有
(2)写出反应①的化学方程式
(3)在滤渣E中加入稀硫酸和试剂Y制胆矾晶体是一种绿色化学工艺,试剂Y为无色液体,反应④的总化学方程式是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】碳粉、CO、H2均可作为实验室还原CuO的还原剂,实验小组对CuO的还原反应及还原产物组成进行探究。
查阅资料:
I .CuO还原反应中相关信息如表所示:
II .CuO高温分解生成Cu2O,Cu2O+2H+=Cu+Cu2++H2O;
II .PdCl2溶液能吸收CO,生成黑色Pd沉淀和一种氢化物、一种氧化物。
回答下列问题:
(1)实验室还原CuO适宜选用的还原剂为_______ ,理由为_______ 。
(2)小组同学用如图所示装置探究碳粉与CuO反应的产物。

①仪器a的名称为_______ 。
②试剂X的作用为_______ 。
③若气体产物中含有CO,则观察到的现象为_______ ;其中反应的化学方程式为_______ 。
(3)某小组同学为测定碳粉还原CuO后固体混合物中单质Cu的质量分数,设计如下实验:准确称取反应管中残留固体8.000g,溶于足量稀硝酸,过滤、洗涤、干燥,所得沉淀的质量为0.160 g;将洗涤液与滤液合并,配成500mL溶液;量取所配溶液25.00mL,加入适当过量的KI溶液;以淀粉为指示剂,用0.500 0 mol·L-1 Na2S2O3标准溶液滴定,达到滴定终点时,消耗标准溶液的体积为12.00mL。已知:2Cu2++5I-=2CuI↓+ ,
, +2
+2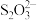 =
=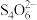 +3I-。
+3I-。
①溶解样品时,不能用稀硫酸代替稀硝酸的原因为_______ .。
②通过计算说明还原产物中是否含有Cu2O:_______ 。
③若CuI吸附部分 ,会导致所测Cu单质的质量分数
,会导致所测Cu单质的质量分数_______ .(填“偏大”“偏小”或“无影响”)。
查阅资料:
I .CuO还原反应中相关信息如表所示:
| 还原剂 | 反应温度/℃ | 产物性状 |
| 碳粉 | >800 | 可能混有砖红色固体或黑色固体 |
| CO | >500 | 可能混有砖红色固体 |
| H2 | 300左右 | 紫红色固体 |
II .PdCl2溶液能吸收CO,生成黑色Pd沉淀和一种氢化物、一种氧化物。
回答下列问题:
(1)实验室还原CuO适宜选用的还原剂为
(2)小组同学用如图所示装置探究碳粉与CuO反应的产物。

①仪器a的名称为
②试剂X的作用为
③若气体产物中含有CO,则观察到的现象为
(3)某小组同学为测定碳粉还原CuO后固体混合物中单质Cu的质量分数,设计如下实验:准确称取反应管中残留固体8.000g,溶于足量稀硝酸,过滤、洗涤、干燥,所得沉淀的质量为0.160 g;将洗涤液与滤液合并,配成500mL溶液;量取所配溶液25.00mL,加入适当过量的KI溶液;以淀粉为指示剂,用0.500 0 mol·L-1 Na2S2O3标准溶液滴定,达到滴定终点时,消耗标准溶液的体积为12.00mL。已知:2Cu2++5I-=2CuI↓+
 ,
, +2
+2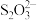 =
=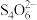 +3I-。
+3I-。①溶解样品时,不能用稀硫酸代替稀硝酸的原因为
②通过计算说明还原产物中是否含有Cu2O:
③若CuI吸附部分
 ,会导致所测Cu单质的质量分数
,会导致所测Cu单质的质量分数
您最近半年使用:0次



