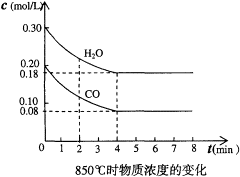
(1)在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:CO(g)+H2O(g) CO2(g)+H2(g);△H<0。CO和H2O浓度变化如下图,则0~4min的平均反应速率v(CO)=
CO2(g)+H2(g);△H<0。CO和H2O浓度变化如下图,则0~4min的平均反应速率v(CO)=______________ mol/(L·min)
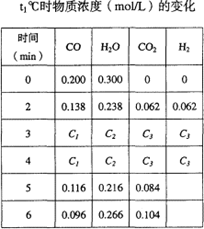
(2)t1℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如右上表。请回答:
①表中3min~4min之间反应处于____________ 状态;C1数值__________ 0.08mol/L(填大于、小于或等于)。
②反应在4min~5min问,平衡向逆方向移动,可能的原因是____________ (单选),表中5min—6min之间数值发生变化,可能的原因是____________ (单选)。
a、增加了水蒸气的量 b、降低温度 c、使用催化剂 d、增加氢气浓度
 CO2(g)+H2(g);△H<0。CO和H2O浓度变化如下图,则0~4min的平均反应速率v(CO)=
CO2(g)+H2(g);△H<0。CO和H2O浓度变化如下图,则0~4min的平均反应速率v(CO)=

(2)t1℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如右上表。请回答:
①表中3min~4min之间反应处于
②反应在4min~5min问,平衡向逆方向移动,可能的原因是
a、增加了水蒸气的量 b、降低温度 c、使用催化剂 d、增加氢气浓度
更新时间:2016-12-09 08:50:25
|
相似题推荐
填空题
|
较难
(0.4)
【推荐1】环境中氮氧化物的合理控制和治理是减少雾霾天气、优化生存环境的有效途径之一。请运用化学反应原理知识,回答下列问题:
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4 (g)+ 4NO2 (g)=== 4NO(g)+ CO2 (g)+ 2H2O(1) △H1 = -662kJ·mol-1
②CH4 (g)+ 4NO(g) === 2N2 (g)+ CO2 (g)+ 2H2O(1) △H2 = -1251 kJ·mol-1
据此,写出CH4将NO2还原为N2的热化学方程式:____________
(2)用活性炭还原法也可处理氮氧化物。有关反应为:C(s)+2NO(g) N2 (g)+CO2 (g)
N2 (g)+CO2 (g)
某研究小组向一个容积(3L)恒定的真空密闭容器中加入0.3mol NO和足量的活性炭与催化剂(固体试样的体积忽略不计),在恒温(T1℃)条件下发生反应,经10min反应达到平衡,测得N2的物质的量为0.09mol。
①0min~10min内以v(NO)表示的平均化学反应速率为_________ 。
②下列各项能判断该反应达到平衡状态的是_________ 。
③在相同条件下,若在容器中放入生石灰,则NO的平衡转化率_________ (填增大、不变或减小)。
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4 (g)+ 4NO2 (g)=== 4NO(g)+ CO2 (g)+ 2H2O(1) △H1 = -662kJ·mol-1
②CH4 (g)+ 4NO(g) === 2N2 (g)+ CO2 (g)+ 2H2O(1) △H2 = -1251 kJ·mol-1
据此,写出CH4将NO2还原为N2的热化学方程式:
(2)用活性炭还原法也可处理氮氧化物。有关反应为:C(s)+2NO(g)
 N2 (g)+CO2 (g)
N2 (g)+CO2 (g)某研究小组向一个容积(3L)恒定的真空密闭容器中加入0.3mol NO和足量的活性炭与催化剂(固体试样的体积忽略不计),在恒温(T1℃)条件下发生反应,经10min反应达到平衡,测得N2的物质的量为0.09mol。
①0min~10min内以v(NO)表示的平均化学反应速率为
②下列各项能判断该反应达到平衡状态的是
| A.容器内压强保持不变 |
| B.速率关系:2v(NO)(正) = v (N2)(逆) |
| C.容器内CO2的体积分数不变 |
| D.混合气体的密度保持不变 |
③在相同条件下,若在容器中放入生石灰,则NO的平衡转化率
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】Ⅰ.某实验小组对H2O2的分解做了如下探究。下表是该实验小组研究影响H2O2分解速率的因素时记录的一组数据,将质量相同但状态不同的MnO2分别加入盛有15 ml 5%的H2O2溶液的大试管中,并用带火星的木条测试,结果如下:
(1)写出大试管中发生反应的化学方程式:_________________ ,该反应是______ 反应(填放热[或吸热)。
(2)实验结果表明,催化剂的催化效果与___________________________ 有关。
Ⅱ.某可逆反应在某体积为5L的密闭容器中进行,在从0—3分钟各物质的量的变化情况如图所示(A,B,C均为气体)。

(3)该反应的的化学方程式为_____________________________________________ ;
(4)反应开始至2分钟时,B的平均反应速率为_____________________________ 。
(5)能说明该反应已达到平衡状态的是________________________ 。
a.v(A)= 2v(B)
b.容器内压强保持不变
c.2v逆(A)= v正(B)
d.容器内混合气体的密度保持不变
(6)在密闭容器里,通入a mol A (g)、b mol B (g)、c molC(g),发生上述反应,当改变下列条件时,反应速率会减小的是____ 。
A.降低温度 B.加入催化剂(正) C.增大容器体积
Ⅲ.为了减缓过量Zn与盐酸产生氢气的反应速率而又不减少产生氢气的量,在盐酸中分别加入下列物质:
A.H2O
B.NaCl溶液
C.Na2CO3溶液
D.Na2NO3溶液
E.CuSO4粉末
你认为可行的是(填编号)________________ 。
| MnO2 | 触摸试管情况 | 观察结果 | 反应完成所需的时间 |
| 粉末状 | 很烫 | 剧烈反应,带火星的木条复燃 | 3.5 min |
| 块状 | 微热 | 反应较慢,火星红亮但木条未复燃 | 30 min |
(2)实验结果表明,催化剂的催化效果与
Ⅱ.某可逆反应在某体积为5L的密闭容器中进行,在从0—3分钟各物质的量的变化情况如图所示(A,B,C均为气体)。

(3)该反应的的化学方程式为
(4)反应开始至2分钟时,B的平均反应速率为
(5)能说明该反应已达到平衡状态的是
a.v(A)= 2v(B)
b.容器内压强保持不变
c.2v逆(A)= v正(B)
d.容器内混合气体的密度保持不变
(6)在密闭容器里,通入a mol A (g)、b mol B (g)、c molC(g),发生上述反应,当改变下列条件时,反应速率会减小的是
A.降低温度 B.加入催化剂(正) C.增大容器体积
Ⅲ.为了减缓过量Zn与盐酸产生氢气的反应速率而又不减少产生氢气的量,在盐酸中分别加入下列物质:
A.H2O
B.NaCl溶液
C.Na2CO3溶液
D.Na2NO3溶液
E.CuSO4粉末
你认为可行的是(填编号)
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】向2L密闭容器中加入0.15 mol·L-1A、0.05 mol·L-1C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如图中甲图所示[t0~t1时c(B)未画出,t1时增大到0.05 mol·L-1]。乙图为t2时刻后改变反应条件,平衡体系中正、逆反应速率随时间变化的情况。
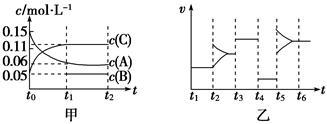
(1)若t4时改变的条件为减小压强,则B的起始物质的量为____________ mol。
(2)若t5时改变的条件是升温,此时v(正)>v(逆),若A的物质的量减少0.03 mol时,容器与外界的热交换总量为a kJ,写出反应的热化学方程式:_______________________ 。
(3)t3时改变的某一反应条件可能是________ (选填序号)。
A.t3时刻,增大了X的浓度 B.t3时刻,升高了体系温度
C.t3时刻,缩小了容器体积 D.t3时刻,使用了催化剂
(4)在恒温恒压下通入惰性气体,v(正)_________ v(逆)(填“>”、“=”或“<”)。
(5)如图两个容器A、B中,A容器的容积保持不变,B容器保持和外界大气压一致。开始时,在保持两个容器体积相等的情况下,分别同时充入2moLH2S和1moLSO2。反应开始后两容器内反应平均反应速率A_________________ B (填“大于”、“小于”或“等于”)。


(1)若t4时改变的条件为减小压强,则B的起始物质的量为
(2)若t5时改变的条件是升温,此时v(正)>v(逆),若A的物质的量减少0.03 mol时,容器与外界的热交换总量为a kJ,写出反应的热化学方程式:
(3)t3时改变的某一反应条件可能是
A.t3时刻,增大了X的浓度 B.t3时刻,升高了体系温度
C.t3时刻,缩小了容器体积 D.t3时刻,使用了催化剂
(4)在恒温恒压下通入惰性气体,v(正)
(5)如图两个容器A、B中,A容器的容积保持不变,B容器保持和外界大气压一致。开始时,在保持两个容器体积相等的情况下,分别同时充入2moLH2S和1moLSO2。反应开始后两容器内反应平均反应速率A

您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】氨在工农业生产中应用广泛。德国人哈伯发明了合成氨反应,其原理为:N2(g)+3H2(g)  2NH3(g) ΔH=-92.4kJ/mol。在500℃、20MPa时,将N2和H2通入到体积为2 L的密闭容器中,反应过程中各种物质的物质的量变化如右图所示:
2NH3(g) ΔH=-92.4kJ/mol。在500℃、20MPa时,将N2和H2通入到体积为2 L的密闭容器中,反应过程中各种物质的物质的量变化如右图所示:

(1)10 min内用NH3表示该反应的平均速率,v(NH3)= 。
(2)在10~20min内NH3浓度变化的原因可能是 (填字母)。
A.加了催化剂 b.降低温度 C.增加NH3的物质的量
(3)该可逆反应达到平衡的标志是__________ (填字母)。
a.3v(H2)正 = 2v(NH3)逆 b.混合气体的密度不再随时间变化
c.容器内的总压强不再随时间而变化 d.N2、H2、NH3的分子数之比为1∶3∶2
e.单位时间生成m mol N2的同时消耗3 m mol H2 f.a mol N≡N键断裂的同时,有6 a mol N—H键合成
(4)第一次平衡时,平衡常数K1= (用数学表达式表示)。NH3的体积分数是 (保留2位小数)。
(5)在反应进行到25min时,曲线发生变化的原因是________________。
(6)已知:N2(g)+3H2(g) 2NH3(g) ΔH =-92.4 kJ/mol; 2H2(g)+O2(g)=2H2O(g) ΔH =-483.6kJ/mol,氨气与氧气反应产生氮气和水的热化学方程式是_______________。
2NH3(g) ΔH =-92.4 kJ/mol; 2H2(g)+O2(g)=2H2O(g) ΔH =-483.6kJ/mol,氨气与氧气反应产生氮气和水的热化学方程式是_______________。
(7)氨氧燃料电池具有很大的发展潜力。氨氧燃料电池工作原理如右图所示:
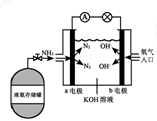
① a电极的电极反应式是______________;
②一段时间后,需向装置中补充KOH,请依据反应原理解释原因是_______________。
 2NH3(g) ΔH=-92.4kJ/mol。在500℃、20MPa时,将N2和H2通入到体积为2 L的密闭容器中,反应过程中各种物质的物质的量变化如右图所示:
2NH3(g) ΔH=-92.4kJ/mol。在500℃、20MPa时,将N2和H2通入到体积为2 L的密闭容器中,反应过程中各种物质的物质的量变化如右图所示:
(1)10 min内用NH3表示该反应的平均速率,v(NH3)= 。
(2)在10~20min内NH3浓度变化的原因可能是 (填字母)。
A.加了催化剂 b.降低温度 C.增加NH3的物质的量
(3)该可逆反应达到平衡的标志是__________ (填字母)。
a.3v(H2)正 = 2v(NH3)逆 b.混合气体的密度不再随时间变化
c.容器内的总压强不再随时间而变化 d.N2、H2、NH3的分子数之比为1∶3∶2
e.单位时间生成m mol N2的同时消耗3 m mol H2 f.a mol N≡N键断裂的同时,有6 a mol N—H键合成
(4)第一次平衡时,平衡常数K1= (用数学表达式表示)。NH3的体积分数是 (保留2位小数)。
(5)在反应进行到25min时,曲线发生变化的原因是________________。
(6)已知:N2(g)+3H2(g)
 2NH3(g) ΔH =-92.4 kJ/mol; 2H2(g)+O2(g)=2H2O(g) ΔH =-483.6kJ/mol,氨气与氧气反应产生氮气和水的热化学方程式是_______________。
2NH3(g) ΔH =-92.4 kJ/mol; 2H2(g)+O2(g)=2H2O(g) ΔH =-483.6kJ/mol,氨气与氧气反应产生氮气和水的热化学方程式是_______________。(7)氨氧燃料电池具有很大的发展潜力。氨氧燃料电池工作原理如右图所示:

① a电极的电极反应式是______________;
②一段时间后,需向装置中补充KOH,请依据反应原理解释原因是_______________。
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】在一固定体积的密闭容器中,在850℃时发生如下反应:CO(g)+H2O(g) CO2(g)+H2(g);△H="-42" kJ•mol-1,容器内各物质的浓度(mol•L-1)变化如下(在850℃时其化学平衡常数k=1.0)。
CO2(g)+H2(g);△H="-42" kJ•mol-1,容器内各物质的浓度(mol•L-1)变化如下(在850℃时其化学平衡常数k=1.0)。
(1)下列可以作为判断该反应已经达到化学平衡状态依据的是____________ ;
A.容器内压强不变
B.v正(H2)=v逆(CO)
C.混合气体中CO2的浓度不变
D.c(CO2)=c(H2)
(2)若在850℃时向反应容器中充入H2O(g),K值__________ (填“增大”、“减小”或“不变”,下同);若升高反应体系的温度,K值___________ 。
(3)(该题写计算过程)上表中:cl=_________ mol/L,H2O(g)的转化率为____________ 。
 CO2(g)+H2(g);△H="-42" kJ•mol-1,容器内各物质的浓度(mol•L-1)变化如下(在850℃时其化学平衡常数k=1.0)。
CO2(g)+H2(g);△H="-42" kJ•mol-1,容器内各物质的浓度(mol•L-1)变化如下(在850℃时其化学平衡常数k=1.0)。| 时间/min | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
A.容器内压强不变
B.v正(H2)=v逆(CO)
C.混合气体中CO2的浓度不变
D.c(CO2)=c(H2)
(2)若在850℃时向反应容器中充入H2O(g),K值
(3)(该题写计算过程)上表中:cl=
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】煤燃烧排放的烟气含有 SO2和 NOx,形成酸雨、污染大气。
(1)采用 NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。在鼓泡反应器中通入含有 SO2和 NO 的烟气,写出 NaClO2溶液脱硝过程中主要反应的离子方程式______________ .
(2)NO2与SO2能发生反应:NO2+SO2 SO3+NO,在固定体积的密闭容器中,使用某种催化剂,改变原料气配比[n0(N02) : n0 (SO2)] 进行多组实验(各次实验的温度可能相同,也可能不同),测定NO2的平衡转化率[α(NO2)]。 部分实验结果如图所示:
SO3+NO,在固定体积的密闭容器中,使用某种催化剂,改变原料气配比[n0(N02) : n0 (SO2)] 进行多组实验(各次实验的温度可能相同,也可能不同),测定NO2的平衡转化率[α(NO2)]。 部分实验结果如图所示:

①当容器内________ (填标号)不再随时间的变化而改变时,可以判断反应达到了化学平衡状态。
a.气体的压强
b.气体的平均摩尔质量
c.气体的密度
d.N02的体积分数
e.气体的颜色
②如果要将图中C点的平衡状态改变为B点的平衡状态,应采取的措施是__________ 。
③图中C、D两点对应的实验温度分别为Tc和Td,试判断: Tc_____ Td(填“>”、“=”或“<”)。
(3)已知:2NO(g)+O2(g) 2NO2(g) △H=-113.0 kJ• mol-1
2NO2(g) △H=-113.0 kJ• mol-1
2SO2(g) + O2(g) 2SO3(g) △H=-196. 6 kJ• mol-1
2SO3(g) △H=-196. 6 kJ• mol-1
则 NO2(g)+SO2(g) SO3(g)+NO(g) △H=
SO3(g)+NO(g) △H= ________ .
(1)采用 NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。在鼓泡反应器中通入含有 SO2和 NO 的烟气,写出 NaClO2溶液脱硝过程中主要反应的离子方程式
(2)NO2与SO2能发生反应:NO2+SO2
 SO3+NO,在固定体积的密闭容器中,使用某种催化剂,改变原料气配比[n0(N02) : n0 (SO2)] 进行多组实验(各次实验的温度可能相同,也可能不同),测定NO2的平衡转化率[α(NO2)]。 部分实验结果如图所示:
SO3+NO,在固定体积的密闭容器中,使用某种催化剂,改变原料气配比[n0(N02) : n0 (SO2)] 进行多组实验(各次实验的温度可能相同,也可能不同),测定NO2的平衡转化率[α(NO2)]。 部分实验结果如图所示:
①当容器内
a.气体的压强
b.气体的平均摩尔质量
c.气体的密度
d.N02的体积分数
e.气体的颜色
②如果要将图中C点的平衡状态改变为B点的平衡状态,应采取的措施是
③图中C、D两点对应的实验温度分别为Tc和Td,试判断: Tc
(3)已知:2NO(g)+O2(g)
 2NO2(g) △H=-113.0 kJ• mol-1
2NO2(g) △H=-113.0 kJ• mol-12SO2(g) + O2(g)
 2SO3(g) △H=-196. 6 kJ• mol-1
2SO3(g) △H=-196. 6 kJ• mol-1则 NO2(g)+SO2(g)
 SO3(g)+NO(g) △H=
SO3(g)+NO(g) △H=
您最近一年使用:0次



