铝是地壳中含量最多的金属元素,铝及其化合物应用日趋广泛。
(1)铝的原子结构示意图是_________________
(2)氧化铝是两性氧化物,写出其与NaOH溶液反应的化学方程式___________________________
(3)工业上常用铝土矿(含SiO2等杂质)生产铝。从Na2SiO3和NaAlO2混合溶液中制得Al(OH)3,需要从下列试剂中选择两种,选用的试剂组合最好是_____________________ 。
a. NaOH溶液 b. CO2c. 氨水 d. 盐酸
最终获得铝单质是电解________ 填化学式),电解过程中加入冰晶石的作用是_____________
(4)下图表示将足量的CO2不断通入KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀与通入CO2的量的关系(已知Ba(AlO2)2:可溶),最先与CO2反应的物质是_________ ,ab段反应的离子方程式为________

(5)某Mg-Al合金是一种潜在的储氢材料。73.2g该合金恰好溶解于1.4 L 5. 0mol·L-1HCl溶液,则合金中Mg和Al的物质的量之比为____________ 。
(1)铝的原子结构示意图是
(2)氧化铝是两性氧化物,写出其与NaOH溶液反应的化学方程式
(3)工业上常用铝土矿(含SiO2等杂质)生产铝。从Na2SiO3和NaAlO2混合溶液中制得Al(OH)3,需要从下列试剂中选择两种,选用的试剂组合最好是
a. NaOH溶液 b. CO2c. 氨水 d. 盐酸
最终获得铝单质是电解
(4)下图表示将足量的CO2不断通入KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀与通入CO2的量的关系(已知Ba(AlO2)2:可溶),最先与CO2反应的物质是

(5)某Mg-Al合金是一种潜在的储氢材料。73.2g该合金恰好溶解于1.4 L 5. 0mol·L-1HCl溶液,则合金中Mg和Al的物质的量之比为
更新时间:2015-11-18 13:37:48
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】写出下列物质在水溶液中的(1)~(3)得电离方程式,写出(4)~(5)的化学方程式。
(1)碳酸钾___________
(2)硫酸氢钠___________
(3)碳酸氢钾___________
(4)二氧化硫和氢氧化钙反应___________
(5)氧化铁和稀硫酸___________
(1)碳酸钾
(2)硫酸氢钠
(3)碳酸氢钾
(4)二氧化硫和氢氧化钙反应
(5)氧化铁和稀硫酸
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】有以下9种熟悉的元素的单质及熟悉的化合物:氯化氢、二氧化硫、铜片、食盐、生石灰、一氧化氮、纯碱、镁片和木炭粉,结合下图中①~⑤选择适当的物质,使有连线的两物质能发生反应。
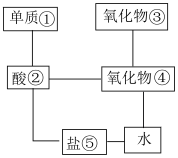
(1)请推断它们的化学式分别为①___________ ;②___________ ;③___________ ;⑤___________ 。
(2)写出下列序号之间的化学方程式
①和②:___________ ;②和④:___________ ;③和④:___________ 。

(1)请推断它们的化学式分别为①
(2)写出下列序号之间的化学方程式
①和②:
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】甘肃马家窑遗址出土的青铜刀是我国最早冶炼的青铜器,由于时间久远,其表面有一层“绿锈”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、CO2、O2作用产生的,化学式为[Cu2(OH)2CO3],“铜绿”能跟酸反应生成铜盐、CO2和H2O。某同学利用以下反应实现了“铜―→铜绿―→……―→铜”的转化。
(1)从物质分类标准看,“铜绿”属于________ (填字母)。
A.酸 B.碱 C.盐 D.氧化物
(2)写出B的化学式:________________ 。
(3)请写出铜绿与盐酸反应的化学方程式:__________________
铜 铜绿
铜绿 A
A Cu(OH)2
Cu(OH)2 B
B Cu
Cu
(1)从物质分类标准看,“铜绿”属于
A.酸 B.碱 C.盐 D.氧化物
(2)写出B的化学式:
(3)请写出铜绿与盐酸反应的化学方程式:
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】根据所学知识,回答下列问题:
(1)K2FeO4是常见的水处理剂,净水原理如图所示。请回答下列问题:

①高铁酸钾(K2FeO4)中铁元素的化合价为_______ 。
②过程a中K2FeO4体现_______ (填“氧化”或“还原”)性,反应过程中转移5.418×1022个电子,需要_______ mol K2FeO4。
(2)碱性条件下用Fe(OH)3和KClO反应制备K2FeO4。配平其反应的化学方程式:_______ 。
_______Fe(OH)3+_______KOH+_______KClO=_______ K2FeO4+_______KCl+_______H2O
(3)干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中的还原剂是_______ ,生产1mol的高铁酸钠,需要消耗Na2O2的物质的量是_______ mol。
(4)将铝箔放入NaOH稀溶液中,开始时无气体生成,写出反应的离子方程式:_______ ;反应片刻后,可观察到有气体产生。
(1)K2FeO4是常见的水处理剂,净水原理如图所示。请回答下列问题:

①高铁酸钾(K2FeO4)中铁元素的化合价为
②过程a中K2FeO4体现
(2)碱性条件下用Fe(OH)3和KClO反应制备K2FeO4。配平其反应的化学方程式:
_______Fe(OH)3+_______KOH+_______KClO=_______ K2FeO4+_______KCl+_______H2O
(3)干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中的还原剂是
(4)将铝箔放入NaOH稀溶液中,开始时无气体生成,写出反应的离子方程式:
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有下列4种物质:①Cl2、② NH3.③浓H2SO4、④A12O3。其中,能与水反应生成两种酸的是__ (填序号,下同);与强酸、强碱溶液均可反应生成盐的是______ ;能使湿润的红色石蕊试纸变蓝的是___ ;能使蔗糖变黑并有气体生成的是_____ 。
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】现有以下物质:①Na ② ③
③ ④
④ ⑤漂白粉 ⑥
⑤漂白粉 ⑥ 溶液 ⑦
溶液 ⑦ ⑧
⑧ 。回答下列问题:
。回答下列问题:
(1)上述物质中属于非电解质的有___________ ,⑤的有效成分为_______ (填化学式)。
(2)将③加入足量⑥中,发生反应的离子方程式为___________ 。
(3)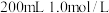 ⑥的溶液加入适量铝(无氧化膜),正好完全反应,消耗铝
⑥的溶液加入适量铝(无氧化膜),正好完全反应,消耗铝_______ g,生成标况下
___________ L。
(4)把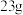 ①加入到标况下
①加入到标况下 ⑧溶于水所形成的溶液中,生成的气体体积
⑧溶于水所形成的溶液中,生成的气体体积______ (标况)。
(5)向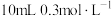 ⑦的水溶液中逐滴滴加
⑦的水溶液中逐滴滴加 ④的水溶液至中性,此时溶液中的
④的水溶液至中性,此时溶液中的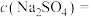
___________  (假设混合后溶液体积的变化忽略不计)。
(假设混合后溶液体积的变化忽略不计)。
 ③
③ ④
④ ⑤漂白粉 ⑥
⑤漂白粉 ⑥ 溶液 ⑦
溶液 ⑦ ⑧
⑧ 。回答下列问题:
。回答下列问题:(1)上述物质中属于非电解质的有
(2)将③加入足量⑥中,发生反应的离子方程式为
(3)
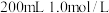 ⑥的溶液加入适量铝(无氧化膜),正好完全反应,消耗铝
⑥的溶液加入适量铝(无氧化膜),正好完全反应,消耗铝
(4)把
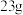 ①加入到标况下
①加入到标况下 ⑧溶于水所形成的溶液中,生成的气体体积
⑧溶于水所形成的溶液中,生成的气体体积(5)向
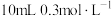 ⑦的水溶液中逐滴滴加
⑦的水溶液中逐滴滴加 ④的水溶液至中性,此时溶液中的
④的水溶液至中性,此时溶液中的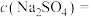
 (假设混合后溶液体积的变化忽略不计)。
(假设混合后溶液体积的变化忽略不计)。
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】按要求填空:
(1)常用作制冷剂的物质的电子式_______ ;
(2)氮气常用作保护气,但是氮气不能用作金属镁的保护气,其原因用化学方程式表示是_______ ;
(3)浓氨水可以检验输送氯气的管道是否泄露,若泄露则会产生白烟,其原理用化学方程式表示为_______ ;
(4)铵盐与NaOH等强碱的溶液在加热条件下反应的离子方程式是_______ ;
(5)汽车尾气(含有烃类、CO、SO2、NO等物质)是城市空气的污染源之一,治理的方法之一是在汽车的排气管上装一个“催化转换器”,使CO和NO转化为无毒气体,其反应方程式为_______ ;
(6)铝土矿(主要成分为Al2O3,含有少量杂质)是提取铝的原料。提取铝的工艺流程如下:

请用离子方程式表示以上工艺流程中第①步反应:_______ ;写出以上工艺流程中第③步反应的化学方程式:_______ ;若第①步加入的是盐酸,则发生反应的离子方程式为_______ 。
(1)常用作制冷剂的物质的电子式
(2)氮气常用作保护气,但是氮气不能用作金属镁的保护气,其原因用化学方程式表示是
(3)浓氨水可以检验输送氯气的管道是否泄露,若泄露则会产生白烟,其原理用化学方程式表示为
(4)铵盐与NaOH等强碱的溶液在加热条件下反应的离子方程式是
(5)汽车尾气(含有烃类、CO、SO2、NO等物质)是城市空气的污染源之一,治理的方法之一是在汽车的排气管上装一个“催化转换器”,使CO和NO转化为无毒气体,其反应方程式为
(6)铝土矿(主要成分为Al2O3,含有少量杂质)是提取铝的原料。提取铝的工艺流程如下:

请用离子方程式表示以上工艺流程中第①步反应:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】请按要求书写下列离子方程式:
(1)利用FeCl3溶液制备胶体的离子方程式为_______________________________ ;
(2)将过量的 通入
通入 溶液中反应的离子方程式
溶液中反应的离子方程式________________________ 。
(3)FeSO4的酸性溶液与H2O2反应试写出该反应的离子方程式:____________________ ;
(4)氧化亚铜中加入稀硫酸____________________________ ;
(5)工业上用次氯酸钠和FeCl3在碱性条件下制备新型绿色消毒剂高铁酸钠(Na2FeO4)该反应的离子方程式是:______________________________ 。
(1)利用FeCl3溶液制备胶体的离子方程式为
(2)将过量的
 通入
通入 溶液中反应的离子方程式
溶液中反应的离子方程式(3)FeSO4的酸性溶液与H2O2反应试写出该反应的离子方程式:
(4)氧化亚铜中加入稀硫酸
(5)工业上用次氯酸钠和FeCl3在碱性条件下制备新型绿色消毒剂高铁酸钠(Na2FeO4)该反应的离子方程式是:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】副产品Y主要含氢氧化铝,还含少量镁、铁的难溶化合物及可溶性杂质,精确分析Y中氢氧化铝含量的方法是称取n g样品,加入过量______ (填写试剂)、溶解、过滤、再通入足量______ (填写试剂)、……灼烧、冷却、称量,得干燥固体mg。计算样品中氢氧化铝的质量分数为_______ (用含m、n的代数式表示)。
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】常温下,在没有氧气存在时,铁与水几乎不反应,但高温下,铁能与水蒸气反应。
(1)铁粉与水蒸气反应的化学方程式是______
(2)停止反应,待装置冷却后,取出反应过的铁粉混合物,加入过量的稀硫酸充分反应。过滤。简述检验所得滤液中Fe3+的操作方法______
(3)经检验上述滤液中不含Fe3+,这不能说明铁粉与水蒸气反应所得产物中不含+3价的铁。原因是________ (结合化学方程式说明):
(4)某同学利用上述滤液制取白色的Fe(OH)2沉淀,向滤液中加入NaOH溶液后,观察到生成的白色沉淀迅速变成灰绿色,最后变成红褐色。
①沉淀由白色变为红褐色的化学方程式是_______
②为了得到白色的Fe(OH)2沉淀,并尽可能使沉淀长时间保持白色,有人设计如图所示的装置:

请简述实验操作及原理_______
(1)铁粉与水蒸气反应的化学方程式是
(2)停止反应,待装置冷却后,取出反应过的铁粉混合物,加入过量的稀硫酸充分反应。过滤。简述检验所得滤液中Fe3+的操作方法
(3)经检验上述滤液中不含Fe3+,这不能说明铁粉与水蒸气反应所得产物中不含+3价的铁。原因是
(4)某同学利用上述滤液制取白色的Fe(OH)2沉淀,向滤液中加入NaOH溶液后,观察到生成的白色沉淀迅速变成灰绿色,最后变成红褐色。
①沉淀由白色变为红褐色的化学方程式是
②为了得到白色的Fe(OH)2沉淀,并尽可能使沉淀长时间保持白色,有人设计如图所示的装置:

请简述实验操作及原理
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】氮及其化合物在生产、生活中有重要的应用。回答下列问题:
(1)下列选项可作为比较氮和氧非金属性强弱的判断依据的是________ 。
a.氢化物稳定性:H2O>NH3 b.沸点:H2O>NH3
c.一定条件下,O2能将NH3氧化 d.碱性:NH3>H2O
(2)氢氰酸(HCN)可用于制造丙烯腈和丙烯酸树脂,HCN分子中含________ 对极性共价键。
(3)NaNO2是一种白色易溶于水的固体,俗称工业盐.其水溶液显碱性,则该溶液中离子浓度由大到小的顺序是________ 。
(4)氰化钠是一种剧毒物质,处理该物质的方法之一是在碱性条件下通入氯气,其中CN﹣被氧化成CO32﹣和N2,写出该反应的离子方式________ 。
(1)下列选项可作为比较氮和氧非金属性强弱的判断依据的是
a.氢化物稳定性:H2O>NH3 b.沸点:H2O>NH3
c.一定条件下,O2能将NH3氧化 d.碱性:NH3>H2O
(2)氢氰酸(HCN)可用于制造丙烯腈和丙烯酸树脂,HCN分子中含
(3)NaNO2是一种白色易溶于水的固体,俗称工业盐.其水溶液显碱性,则该溶液中离子浓度由大到小的顺序是
(4)氰化钠是一种剧毒物质,处理该物质的方法之一是在碱性条件下通入氯气,其中CN﹣被氧化成CO32﹣和N2,写出该反应的离子方式
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】如图是“铁链状”图案,图中相连的两物质可归属于同一类别,相交部分A、B、C、D为其相应的分类依据代号。

(1)①写出相邻两种物质之间能发生反应的化学方程式______________________________
②写出除去NaCl溶液中杂质FeCl3的化学方程式__________________________ 。
(2)请简述选用图中物质制备Fe(OH)3胶体的实验操作_________________________ 。
(3)以下框图中化合物A是上述链状图中的一种物质,是生活中常见的一种调味品,如下图是该物质在化工生产中的一系列反应;其中化合物F俗称烧碱,单质C也是上述链状图中的一种物质。
①写出单质B与H2O反应的离子方程式______________________________ 。
②单质A与Ca(OH)2反应制取漂白粉的化学方程式为________________________ 。

(1)①写出相邻两种物质之间能发生反应的化学方程式
②写出除去NaCl溶液中杂质FeCl3的化学方程式
(2)请简述选用图中物质制备Fe(OH)3胶体的实验操作
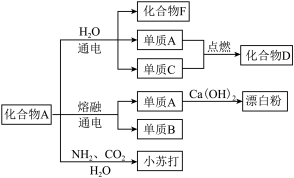
(3)以下框图中化合物A是上述链状图中的一种物质,是生活中常见的一种调味品,如下图是该物质在化工生产中的一系列反应;其中化合物F俗称烧碱,单质C也是上述链状图中的一种物质。

①写出单质B与H2O反应的离子方程式
②单质A与Ca(OH)2反应制取漂白粉的化学方程式为
您最近半年使用:0次



