下列说法正确的是
| A.需要加热才能发生的反应一定是吸热反应 |
| B.任何放热反应在常温条件下一定能发生反应 |
| C.反应物和生成物所具有的总能量决定了放热还是吸热 |
| D.吸热反应在任何条件下都不能发生反应 |
13-14高二上·福建福州·期末 查看更多[3]
陕西省宝鸡市渭滨区2020-2021学年高二上学期期末考试化学试题2015-2016学年湖北省黄石市有色一中高二上学期10月月考化学试卷(已下线)2012-2013学年福建省福州文博中学高二上学期期末考试化学试卷
更新时间:2016-12-09 09:02:23
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】某气体反应的能量变化分析如图所示,以下判断错误的是
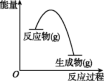

| A.这是一个放热反应 |
| B.该反应可能需要加热 |
| C.反应物比生成物更稳定 |
| D.该反应的反应物键能总和小于生成物的键能总和 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列依据热化学方程式得出的结论正确的是
| A.甲烷的燃烧热是890kJ/mol,则甲烷燃烧的热化学方程式:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890kJ/mol |
| B.已知C(石墨,s)=C(金刚石,s) ΔH>0,则金刚石比石墨稳定 |
| C.已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1,则任何酸碱中和反应的热效应均为57.3 kJ |
| D.已知2C(s)+2O2(g)=2CO2(g) ΔH1,2C(s)+O2(g)="2CO(g)" ΔH2,则ΔH1<ΔH2 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列说法正确的是
| A.需要加热才能发生的反应一定是吸热反应 |
| B.放热反应在常温条件下一定能进行 |
| C.NaOH固体溶于水是放热反应 |
| D.A+B=C+D是放热反应,说明A和B物质的总能量高于C和D的总能量 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】酸催化丙烯与一元醇合成醚的反应机理、能量变化与反应过程的关系如图所示。下列说法正确的是


| A.①②均为放热过程 |
| B.②的逆反应吸收的能量比③的逆反应吸收的能量多 |
| C.反应过程中只存在2种过渡态 |
| D.总反应为放热反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】下列叙述正确的是 ( )
| A.生成物总能量一定低于反应物总能量 |
| B.酒精可用作燃料,说明酒精燃烧是放热反应 |
| C.硝酸铵溶于水温度降低,这个变化是吸热反应 |
| D.同温同压下,H2和Cl2在光照和点燃条件下的ΔH不同 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列反应既属于氧化还原反应,又是吸热反应的是
| A.灼热的炭与CO2的反应 |
| B.Na2O2与H2O的反应 |
| C.镁条与稀盐酸的反应 |
| D.碳酸钙高温分解的反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】以下过程在常温下都可以自发进行,可利用焓判据来解释的是
| A.2N2O5(g)=4N2O4(g)+O2(g) ΔH=+56.7kJ·mol-1 |
| B.2H2(g)+O2(g)=2H2O(l) ΔH=-571.6kJ·mol-1 |
| C.硝酸铵自发地溶于水 |
| D.湿衣服经过晾晒变干 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】将水蒸气通过红热的炭即可产生水煤气。反应为:C(s)+H2O(g) CO(g)+H2(g) △H=+131.3kJ/mol,△S=+133.7J/(K·mol)。下列说法正确的是( )
CO(g)+H2(g) △H=+131.3kJ/mol,△S=+133.7J/(K·mol)。下列说法正确的是( )
 CO(g)+H2(g) △H=+131.3kJ/mol,△S=+133.7J/(K·mol)。下列说法正确的是( )
CO(g)+H2(g) △H=+131.3kJ/mol,△S=+133.7J/(K·mol)。下列说法正确的是( )| A.常温下不能自发进行 |
| B.常温下能自发进行 |
| C.100℃下能自发进行 |
| D.任何温度下都不能自发进行 |
您最近一年使用:0次



