用编号填空:
(1)下列关于燃烧热的说法正确的是_____________ ;
A.101kPa时1mol氢气完全燃烧生成水蒸气所放出的热量即氢气的燃烧热;
B.101kPa时1mol碳在氧气中燃烧生成CO所放出的热量即碳的燃烧热;
C.某物质的燃烧热不随热化学方程式计量数的改变而改变。
(2)下列关于用稀盐酸和氢氧化钠稀溶液测中和热的说法错误的是_____________ ;
A.实验结果随反应物用量改变而改变;
B.实验中氢氧化钠溶液稍过量是为了使盐酸完全被氢氧化钠中和;
C.实验中不可用环形铜质搅拌棒代替环形玻璃搅拌棒。
(3)下列关于化学平衡的说法错误的是_____________ ;
A.若改变影响化学平衡的条件之一,平衡向能够使这种改变减弱的方向移动;
B.达到化学平衡时,各组分的浓度不再改变,反应停止;
C.化学平衡移动,化学平衡常数不一定改变。
(4)改变下列条件,化学平衡一定向正反应方向移动的是_____________ ;
A.增大反应物浓度 B.升高温度 C.增大压强
(5)下列关于电解质的说法错误的是_____________ ;
A.酸、碱、盐及氧化物都是电解质;
B.电解质溶液能导电是因为发生了电离,产生了自由移动的离子;
C.电解质不一定能导电,能导电的物质不一定是电解质。
(6)下列反应的△H<0的是_____________ ;
A.铝和稀硫酸反应 B.碳酸氢铵受热分解 C.氢氧化钡晶体与氯化铵晶体反应
(7)下列情况,均为日常生活中为了改变反应速率而采取的措施,其中不属于浓度影响反应速率的是_____________ ;
A.汽车加大油门 B.食物放冰箱 C.糕点包装袋里放小包除氧剂
(8)下列实验现象与实际不符的是_____________ ;
A.向4mL0.01mol/LKMnO4酸性溶液中加入2mL0.1mol/LH2C2O4溶液:溶液褪色;
B.浓度均为0.1mol/L的Na2S2O3和H2SO4溶液等体积混合:溶液变浑浊;
C.将盛有NO2和N2O4混合气体的容器压缩:混合气体颜色比压缩前浅。
(9)一定温度下,有三种酸:A.盐酸,B.硫酸,C.醋酸,回答下列问题:
①三种酸溶液等物质的量浓度时,c(H+)最大的是_____________ ;
②三种酸的c(H+)相同时,溶液浓度最大的是_________________ ;
③将c(H+)相同的三种酸均加水稀释至原来的100倍后,再加入同样的锌粒,反应最快的是__________ 。
(1)下列关于燃烧热的说法正确的是
A.101kPa时1mol氢气完全燃烧生成水蒸气所放出的热量即氢气的燃烧热;
B.101kPa时1mol碳在氧气中燃烧生成CO所放出的热量即碳的燃烧热;
C.某物质的燃烧热不随热化学方程式计量数的改变而改变。
(2)下列关于用稀盐酸和氢氧化钠稀溶液测中和热的说法错误的是
A.实验结果随反应物用量改变而改变;
B.实验中氢氧化钠溶液稍过量是为了使盐酸完全被氢氧化钠中和;
C.实验中不可用环形铜质搅拌棒代替环形玻璃搅拌棒。
(3)下列关于化学平衡的说法错误的是
A.若改变影响化学平衡的条件之一,平衡向能够使这种改变减弱的方向移动;
B.达到化学平衡时,各组分的浓度不再改变,反应停止;
C.化学平衡移动,化学平衡常数不一定改变。
(4)改变下列条件,化学平衡一定向正反应方向移动的是
A.增大反应物浓度 B.升高温度 C.增大压强
(5)下列关于电解质的说法错误的是
A.酸、碱、盐及氧化物都是电解质;
B.电解质溶液能导电是因为发生了电离,产生了自由移动的离子;
C.电解质不一定能导电,能导电的物质不一定是电解质。
(6)下列反应的△H<0的是
A.铝和稀硫酸反应 B.碳酸氢铵受热分解 C.氢氧化钡晶体与氯化铵晶体反应
(7)下列情况,均为日常生活中为了改变反应速率而采取的措施,其中不属于浓度影响反应速率的是
A.汽车加大油门 B.食物放冰箱 C.糕点包装袋里放小包除氧剂
(8)下列实验现象与实际不符的是
A.向4mL0.01mol/LKMnO4酸性溶液中加入2mL0.1mol/LH2C2O4溶液:溶液褪色;
B.浓度均为0.1mol/L的Na2S2O3和H2SO4溶液等体积混合:溶液变浑浊;
C.将盛有NO2和N2O4混合气体的容器压缩:混合气体颜色比压缩前浅。
(9)一定温度下,有三种酸:A.盐酸,B.硫酸,C.醋酸,回答下列问题:
①三种酸溶液等物质的量浓度时,c(H+)最大的是
②三种酸的c(H+)相同时,溶液浓度最大的是
③将c(H+)相同的三种酸均加水稀释至原来的100倍后,再加入同样的锌粒,反应最快的是
更新时间:2019-01-30 10:14:09
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
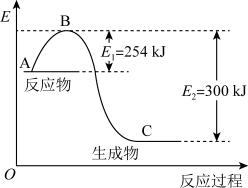
(1)如图是 和
和 反应生成
反应生成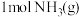 过程中能量的变化示意图,该化学反应属于
过程中能量的变化示意图,该化学反应属于___________ (放热或吸热)反应,正反应的活化能为___________ ,写出该反应的热化学方程式:___________ 。
(2)上述反应用到的氢气是一种清洁燃料,已知氢气的燃烧热为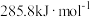 ,请写出氢气燃烧热的热化学方程式:
,请写出氢气燃烧热的热化学方程式:________ 。已知 转化成
转化成 吸收
吸收 的热量,
的热量,________ 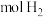 完全燃烧生成气态水可以放出
完全燃烧生成气态水可以放出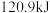 的热量(不可虑热量损失)。
的热量(不可虑热量损失)。

(1)如图是
 和
和 反应生成
反应生成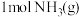 过程中能量的变化示意图,该化学反应属于
过程中能量的变化示意图,该化学反应属于(2)上述反应用到的氢气是一种清洁燃料,已知氢气的燃烧热为
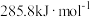 ,请写出氢气燃烧热的热化学方程式:
,请写出氢气燃烧热的热化学方程式: 转化成
转化成 吸收
吸收 的热量,
的热量,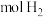 完全燃烧生成气态水可以放出
完全燃烧生成气态水可以放出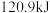 的热量(不可虑热量损失)。
的热量(不可虑热量损失)。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】甲烷是一种高效清洁的新能源,0.25mol甲烷完全燃烧生成液态水时放出222.5kJ热量,则甲烷燃烧的热化学方程式为_____________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】依据事实,写出下列反应的热化学方程式。
(1)16gCH4(g)与适量O2(g)发生反应,生成CO2(g)和H2O(l),放出890.3kJ热量_________ 。
(2)1L1mol·L-1KOH溶液中和1L1mol·L-1HNO3溶液,放出57.3kJ热量________ 。
(3)12gC(s)与适量O2(g)发生反应生成CO2(g),放出283.0kJ热量________ 。
(4)1mol葡萄糖[C6H12O6(s)]在人体中完全氧化,生成CO2(g)和H2O(l)产生2800kJ热量_________ 。
(1)16gCH4(g)与适量O2(g)发生反应,生成CO2(g)和H2O(l),放出890.3kJ热量
(2)1L1mol·L-1KOH溶液中和1L1mol·L-1HNO3溶液,放出57.3kJ热量
(3)12gC(s)与适量O2(g)发生反应生成CO2(g),放出283.0kJ热量
(4)1mol葡萄糖[C6H12O6(s)]在人体中完全氧化,生成CO2(g)和H2O(l)产生2800kJ热量
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】NaOH稀溶液跟稀盐酸反应的中和热与KOH稀溶液跟稀硫酸反应的中和热___________ (填“相等”或“不等”),原因是(用适当的文字和离子方程式解释)___________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】已知稀溶液中,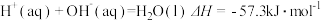 ,则稀醋酸与稀氢氧化钠溶液反应生成
,则稀醋酸与稀氢氧化钠溶液反应生成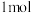 水时放出
水时放出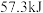 的热量。
的热量。______
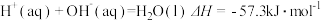 ,则稀醋酸与稀氢氧化钠溶液反应生成
,则稀醋酸与稀氢氧化钠溶液反应生成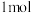 水时放出
水时放出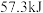 的热量。
的热量。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】按要求填空
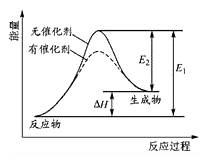
(1)某反应的反应过程中能量变化如图所示,回答下列问题:
E逆反应的活化能___ E反应的活化能(填“大于”或“小于”)
(2)50mL 0.50mol/L盐酸与50mL 0.55mo/L NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热,回答下列问题:
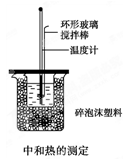
①烧杯间填满碎泡沫塑料作用是________
②实验中改用60mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量_________ (填“相等“或“不相等”)
(1)某反应的反应过程中能量变化如图所示,回答下列问题:
E逆反应的活化能

(2)50mL 0.50mol/L盐酸与50mL 0.55mo/L NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热,回答下列问题:

①烧杯间填满碎泡沫塑料作用是
②实验中改用60mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】(1)在下列事实中,什么因素影响了化学反应的速率?
①石灰石煅烧时要粉碎成细小的矿粒_______ ;
②熔化的KClO3放出气泡很慢,撒入少量MnO2,则很快产生气体_______ ;
③同样大小的石灰石分别在0.1mol·L-1的盐酸和1mol·L-1的盐酸中反应速率不同_______ ;
④夏天的食品易霉变,冬天就不易发生该现象_______ ;
(2)依据实验数据,写出下列反应的热化学方程式。
①1molC2H4(g)与适量O2(g)反应,生成CO2(g)和H2O(1),放出1411kJ热量_______ 。
②2molAl(s)与适量O2(g)发生反应,生成Al2O3(s),放出1669.8kJ热量_______ 。
③若适量的N2和O2完全反应,每生成23gNO2需要吸收16.95kJ热量,则表示该反应的热化学方程式为_______ 。
④在25℃、101kPa时,4gH2在足量O2中完全燃烧生成H2O(1)放出571.6kJ的热量,则表示H2燃烧热的热化学方程式为_______ 。
①石灰石煅烧时要粉碎成细小的矿粒
②熔化的KClO3放出气泡很慢,撒入少量MnO2,则很快产生气体
③同样大小的石灰石分别在0.1mol·L-1的盐酸和1mol·L-1的盐酸中反应速率不同
④夏天的食品易霉变,冬天就不易发生该现象
(2)依据实验数据,写出下列反应的热化学方程式。
①1molC2H4(g)与适量O2(g)反应,生成CO2(g)和H2O(1),放出1411kJ热量
②2molAl(s)与适量O2(g)发生反应,生成Al2O3(s),放出1669.8kJ热量
③若适量的N2和O2完全反应,每生成23gNO2需要吸收16.95kJ热量,则表示该反应的热化学方程式为
④在25℃、101kPa时,4gH2在足量O2中完全燃烧生成H2O(1)放出571.6kJ的热量,则表示H2燃烧热的热化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】燃料的热值
热值是指一定条件下_______ 的可燃物_______ 所放出的热。常见的燃料中,热值最大的是_______ ,其次是_______ 。
热值是指一定条件下
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】已知下列热化学方程式:
①2H2(g) +O2(g) = 2H2O(l) △H = -571.6 kJ / mol
②C(s) + O2(g) = CO2(g) △H = -393.5 kJ / mol
③C(s) + H2O(g) = CO(g) + H2(g) △H = +131.5 kJ/mol
请回答:
(1)上述反应中属于放热反应的是_______ (填序号),固体碳的燃烧热为_______ 。
(2)2g H2完全燃烧生成液态水,放出的热量为_______ 。
(3)依据事实,写出下列反应的热化学方程式。
①1molN2(g)与适量O2(g)反应生成NO(g),需吸收68 kJ的热量,该反应的热化学方程式为_______ 。
②已知HCN稀溶液与NaOH稀溶液反应生成1mol H2O时,放出12.1kJ热量,用离子方程式表示该反应的热化学方程为_______ 。
①2H2(g) +O2(g) = 2H2O(l) △H = -571.6 kJ / mol
②C(s) + O2(g) = CO2(g) △H = -393.5 kJ / mol
③C(s) + H2O(g) = CO(g) + H2(g) △H = +131.5 kJ/mol
请回答:
(1)上述反应中属于放热反应的是
(2)2g H2完全燃烧生成液态水,放出的热量为
(3)依据事实,写出下列反应的热化学方程式。
①1molN2(g)与适量O2(g)反应生成NO(g),需吸收68 kJ的热量,该反应的热化学方程式为
②已知HCN稀溶液与NaOH稀溶液反应生成1mol H2O时,放出12.1kJ热量,用离子方程式表示该反应的热化学方程为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】在一定体积的密闭容器中,进行化学反应CO2 (g)+H2 (g) CO (g)+H2O (g),其化学平衡常数K和温度t的关系如下表:
CO (g)+H2O (g),其化学平衡常数K和温度t的关系如下表:
回答下列问题:
(1)该反应的化学平衡常数表达式为K=_______ 。
(2)正反应为_______ 反应(填“吸热”或“放热”)。
(3)能判断该反应是否达到化学平衡状态的依据是_______(多选扣分)。
(4)某温度下,平衡浓度符合下式:c (CO2)·c (H2)=c (CO)·c (H2O)可判断此时的温度为_______ ℃。
(5)增大压强,平衡常数_______ (填“增大”“减小”“不变”)
 CO (g)+H2O (g),其化学平衡常数K和温度t的关系如下表:
CO (g)+H2O (g),其化学平衡常数K和温度t的关系如下表:| t / ℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的化学平衡常数表达式为K=
(2)正反应为
(3)能判断该反应是否达到化学平衡状态的依据是_______(多选扣分)。
| A.容器中压强不变 | B.混合气体中c (CO)不变 |
| C.v正(H2)=v逆(H2O) | D.c (CO2)=c (CO) |
(5)增大压强,平衡常数
您最近一年使用:0次
【推荐2】已知一定温度下,氧化铁可以与一氧化碳发生下列反应:Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g)。该温度下,在2L盛有Fe2O3粉末的密闭容器中通入CO气体,10min后,生成了单质铁11.2g。
2Fe(s)+3CO2(g)。该温度下,在2L盛有Fe2O3粉末的密闭容器中通入CO气体,10min后,生成了单质铁11.2g。
(1)根据题干信息,计算出10min内CO的平均反应速率为_______ 。
(2)保持温度不变,待密闭容器中反应达到平衡后,再向容器中通入1molCO气体,重新平衡后,平衡体系中CO所占的体积分数_______。
(3)请用上述反应中某种气体的有关物理量来说明该反应已达到平衡状态:①_______ ②_______ 。
 2Fe(s)+3CO2(g)。该温度下,在2L盛有Fe2O3粉末的密闭容器中通入CO气体,10min后,生成了单质铁11.2g。
2Fe(s)+3CO2(g)。该温度下,在2L盛有Fe2O3粉末的密闭容器中通入CO气体,10min后,生成了单质铁11.2g。(1)根据题干信息,计算出10min内CO的平均反应速率为
(2)保持温度不变,待密闭容器中反应达到平衡后,再向容器中通入1molCO气体,重新平衡后,平衡体系中CO所占的体积分数_______。
| A.增大 | B.减小 | C.不变 | D.无法判断 |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】某温度时,在一个2 L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示。
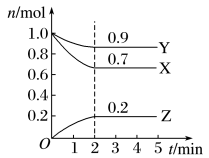
根据图中数据,试填写下列空白:
(1)该反应的化学方程式为________________________ 。
(2)从开始到2 min,Z的平均反应速率为_______________ ;
(3)平衡时,X的浓度为________ 。
(4)在第4 min时Z的消耗速率和生产速率____ (填>,=,<)
(5)下列叙述能说明该反应已达到化学平衡状态的是________ (填字母)。
A.体系总物质的质量不变化 B.同一时刻,X 与Y的反应速率相等
C.X的物质的量浓度不再发生变化 D.相同时间内Z的消耗速率等于生成速率

根据图中数据,试填写下列空白:
(1)该反应的化学方程式为
(2)从开始到2 min,Z的平均反应速率为
(3)平衡时,X的浓度为
(4)在第4 min时Z的消耗速率和生产速率
(5)下列叙述能说明该反应已达到化学平衡状态的是
A.体系总物质的质量不变化 B.同一时刻,X 与Y的反应速率相等
C.X的物质的量浓度不再发生变化 D.相同时间内Z的消耗速率等于生成速率
您最近一年使用:0次



