氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,工业上合成氨反应通常用铁触媒作催化剂,反应方程式为:N2+3H2 2NH3 △H<0。
2NH3 △H<0。
(1)已知N2(g)+3H2(g) 2NH3(g) ΔH=-92kJ·mol-1,拆开1mol H-H键,1molN≡N键分别需要的能量是436kJ、、946kJ,则拆开1molN-H键需要的能量是
2NH3(g) ΔH=-92kJ·mol-1,拆开1mol H-H键,1molN≡N键分别需要的能量是436kJ、、946kJ,则拆开1molN-H键需要的能量是__________ 。
(2)合成氨反应达到平衡后将容器的容积压缩到原来的1/2,其他条件不变,对平衡体系产生的影响是__________ (填字母序号)。
E.平衡向正方向移动
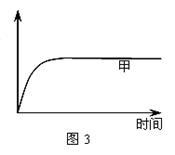
(3) 如图2所示,在甲、乙两容器中分别充入1molN2和3molH2,使甲、乙两容器初始容积相等。在相同温度下发生反应N2(g)+3H2(g) 2NH3(g) ,并维持反应过程中温度不变。已知甲容器中H2的转化率随时间变化的图象如图3所示,请在图3中画出乙容器中H2的转化率随时间变化的图象。
2NH3(g) ,并维持反应过程中温度不变。已知甲容器中H2的转化率随时间变化的图象如图3所示,请在图3中画出乙容器中H2的转化率随时间变化的图象。
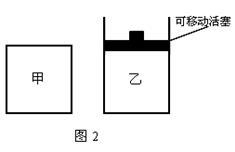
(4)若反应N2(g)+3H2(g) 2NH3(g)在一容积固定不变的容器内进行,并维持反应过程中温度不变。若平衡从正向建立,且起始时N2与H2的物质的量分别为amol、bmol,当a:b=
2NH3(g)在一容积固定不变的容器内进行,并维持反应过程中温度不变。若平衡从正向建立,且起始时N2与H2的物质的量分别为amol、bmol,当a:b=______ 时,达到平衡后NH3的体积分数最大。
 2NH3 △H<0。
2NH3 △H<0。(1)已知N2(g)+3H2(g)
 2NH3(g) ΔH=-92kJ·mol-1,拆开1mol H-H键,1molN≡N键分别需要的能量是436kJ、、946kJ,则拆开1molN-H键需要的能量是
2NH3(g) ΔH=-92kJ·mol-1,拆开1mol H-H键,1molN≡N键分别需要的能量是436kJ、、946kJ,则拆开1molN-H键需要的能量是(2)合成氨反应达到平衡后将容器的容积压缩到原来的1/2,其他条件不变,对平衡体系产生的影响是
| A.c(H2)减小 |
| B.正反应速率加快,逆反应速率减慢 |
| C.NH3的物质的量增加 |
| D.平衡常数K增大 |
E.平衡向正方向移动
(3) 如图2所示,在甲、乙两容器中分别充入1molN2和3molH2,使甲、乙两容器初始容积相等。在相同温度下发生反应N2(g)+3H2(g)
 2NH3(g) ,并维持反应过程中温度不变。已知甲容器中H2的转化率随时间变化的图象如图3所示,请在图3中画出乙容器中H2的转化率随时间变化的图象。
2NH3(g) ,并维持反应过程中温度不变。已知甲容器中H2的转化率随时间变化的图象如图3所示,请在图3中画出乙容器中H2的转化率随时间变化的图象。

(4)若反应N2(g)+3H2(g)
 2NH3(g)在一容积固定不变的容器内进行,并维持反应过程中温度不变。若平衡从正向建立,且起始时N2与H2的物质的量分别为amol、bmol,当a:b=
2NH3(g)在一容积固定不变的容器内进行,并维持反应过程中温度不变。若平衡从正向建立,且起始时N2与H2的物质的量分别为amol、bmol,当a:b=
更新时间:2019-01-30 18:14:09
|
【知识点】 化学平衡
相似题推荐
填空题
|
较难
(0.4)
解题方法
【推荐1】黑色金属材料是工业上对铁、铬、锰的统称, 、
、 、
、 及其化合物在日常生活生产中的用途相当广泛。
及其化合物在日常生活生产中的用途相当广泛。
Ⅰ. 根据所学知识,回答下列问题:
(1) 具有净水作用,
具有净水作用, 净水的原理是
净水的原理是_______ 。
(2)向 溶液中加入
溶液中加入 溶液至过量,微热。再通入
溶液至过量,微热。再通入 ,可观察到溶液呈紫色(高铁酸钾:
,可观察到溶液呈紫色(高铁酸钾: )。写出此过程发生反应的离子方程式:
)。写出此过程发生反应的离子方程式:_______ 。
(3) 可用于治疗缺铁性贫血症,为验证药品的还原性,某实验小组取少量药用
可用于治疗缺铁性贫血症,为验证药品的还原性,某实验小组取少量药用 配制成溶液,并取
配制成溶液,并取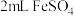 溶液于试管中,滴入几滴浓硝酸,振荡,试管中产生红棕色气体,溶液变为深棕色。为探究溶液没有变为黄色的原因补充了如下实验:向
溶液于试管中,滴入几滴浓硝酸,振荡,试管中产生红棕色气体,溶液变为深棕色。为探究溶液没有变为黄色的原因补充了如下实验:向 溶液和
溶液和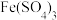 溶液中分别通入
溶液中分别通入 ,观察到
,观察到 溶液变为深棕色,
溶液变为深棕色,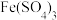 溶液无明显变化。
溶液无明显变化。
①“试管中产生红棕色气体,溶液变为深棕色”的原因是_______ 。
②实验小组改进实验,观察到溶液变为黄色的实验操作是_______ 。
Ⅱ.在 溶液中存在下列平衡:
溶液中存在下列平衡: 。
。
(4)下列有关 溶液的说法正确的是_______(填标号)。
溶液的说法正确的是_______(填标号)。
Ⅲ. 可用作电讯器材元件材料。还可用作瓷釉、颜料及制造锰盐的原料。它在空气中加热易转化为不同价态锰的氧化物,其固体残留率(
可用作电讯器材元件材料。还可用作瓷釉、颜料及制造锰盐的原料。它在空气中加热易转化为不同价态锰的氧化物,其固体残留率( )随温度的变化如图所示。
)随温度的变化如图所示。

(5) 时,剩余固体中
时,剩余固体中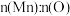 为
为_______ 。
(6)图中C点对应固体的成分为_______ (填化学式)。
 、
、 、
、 及其化合物在日常生活生产中的用途相当广泛。
及其化合物在日常生活生产中的用途相当广泛。Ⅰ. 根据所学知识,回答下列问题:
(1)
 具有净水作用,
具有净水作用, 净水的原理是
净水的原理是(2)向
 溶液中加入
溶液中加入 溶液至过量,微热。再通入
溶液至过量,微热。再通入 ,可观察到溶液呈紫色(高铁酸钾:
,可观察到溶液呈紫色(高铁酸钾: )。写出此过程发生反应的离子方程式:
)。写出此过程发生反应的离子方程式:(3)
 可用于治疗缺铁性贫血症,为验证药品的还原性,某实验小组取少量药用
可用于治疗缺铁性贫血症,为验证药品的还原性,某实验小组取少量药用 配制成溶液,并取
配制成溶液,并取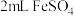 溶液于试管中,滴入几滴浓硝酸,振荡,试管中产生红棕色气体,溶液变为深棕色。为探究溶液没有变为黄色的原因补充了如下实验:向
溶液于试管中,滴入几滴浓硝酸,振荡,试管中产生红棕色气体,溶液变为深棕色。为探究溶液没有变为黄色的原因补充了如下实验:向 溶液和
溶液和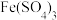 溶液中分别通入
溶液中分别通入 ,观察到
,观察到 溶液变为深棕色,
溶液变为深棕色,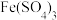 溶液无明显变化。
溶液无明显变化。①“试管中产生红棕色气体,溶液变为深棕色”的原因是
②实验小组改进实验,观察到溶液变为黄色的实验操作是
Ⅱ.在
 溶液中存在下列平衡:
溶液中存在下列平衡: 。
。(4)下列有关
 溶液的说法正确的是_______(填标号)。
溶液的说法正确的是_______(填标号)。| A.加入少量硫酸,溶液的橙色加深 |
| B.加入少量水稀释,溶液中离子总数增加 |
C.入少量 溶液,平衡逆向移动 溶液,平衡逆向移动 |
D.加入少量 固体,平衡正向移动, 固体,平衡正向移动, 转化率变大 转化率变大 |
Ⅲ.
 可用作电讯器材元件材料。还可用作瓷釉、颜料及制造锰盐的原料。它在空气中加热易转化为不同价态锰的氧化物,其固体残留率(
可用作电讯器材元件材料。还可用作瓷釉、颜料及制造锰盐的原料。它在空气中加热易转化为不同价态锰的氧化物,其固体残留率( )随温度的变化如图所示。
)随温度的变化如图所示。
(5)
 时,剩余固体中
时,剩余固体中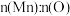 为
为(6)图中C点对应固体的成分为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】碳及其化合物有广泛的用途。
(1)将水蒸气通过红热的碳即可产生水煤气。反应为:C(s)+H2O(g) CO(g)+H2(g) ΔH>0,以上反应达到平衡后,在体积不变的条件下,以下措施有利于提高H2O(g)的平衡转化率的是
CO(g)+H2(g) ΔH>0,以上反应达到平衡后,在体积不变的条件下,以下措施有利于提高H2O(g)的平衡转化率的是__________ 。
(2)将一定量的CO(g)和H2O(g)分别通入到体积为2.0L的恒容密闭容器中,发生以下反应:
CO(g)+H2O(g) CO2(g)+H2(g),得到如下数据:
CO2(g)+H2(g),得到如下数据:
通过计算求出该反应的平衡常数(计算结果保留两位有效数字)。
(3)把水煤气中的混合气体经过处理后获得的较纯H2用于工业合成氨。已知:
N2(g)+3H2(g) 2NH3(g) ΔH=-92.4kJ•mol-1
2NH3(g) ΔH=-92.4kJ•mol-1
2N2(g)+6H2O(l) 4NH3(g)+3O2(g) ΔH=" +1530.0kJ" /mol
4NH3(g)+3O2(g) ΔH=" +1530.0kJ" /mol
①氢气的燃烧热ΔH=_______________ 。
②实验Ⅲ比实验Ⅰ的温度要高,其它条件相同,请在下图中画出实验Ⅰ和实验Ⅲ中NH3浓度随时间变化的示意图,并作必要的标注。______________

(1)将水蒸气通过红热的碳即可产生水煤气。反应为:C(s)+H2O(g)
 CO(g)+H2(g) ΔH>0,以上反应达到平衡后,在体积不变的条件下,以下措施有利于提高H2O(g)的平衡转化率的是
CO(g)+H2(g) ΔH>0,以上反应达到平衡后,在体积不变的条件下,以下措施有利于提高H2O(g)的平衡转化率的是| A.升高温度 | B.增加碳的用量 |
| C.加入催化剂 | D.用CO吸收剂除去CO |
(2)将一定量的CO(g)和H2O(g)分别通入到体积为2.0L的恒容密闭容器中,发生以下反应:
CO(g)+H2O(g)
 CO2(g)+H2(g),得到如下数据:
CO2(g)+H2(g),得到如下数据:| 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所 需时间/min | ||
| H2O | CO | H2 | CO | ||
| 900 | 1.0 | 2.0 | 0.4 | 1.6 | 3.0 |
通过计算求出该反应的平衡常数(计算结果保留两位有效数字)。
(3)把水煤气中的混合气体经过处理后获得的较纯H2用于工业合成氨。已知:
N2(g)+3H2(g)
 2NH3(g) ΔH=-92.4kJ•mol-1
2NH3(g) ΔH=-92.4kJ•mol-12N2(g)+6H2O(l)
 4NH3(g)+3O2(g) ΔH=" +1530.0kJ" /mol
4NH3(g)+3O2(g) ΔH=" +1530.0kJ" /mol①氢气的燃烧热ΔH=
②实验Ⅲ比实验Ⅰ的温度要高,其它条件相同,请在下图中画出实验Ⅰ和实验Ⅲ中NH3浓度随时间变化的示意图,并作必要的标注。

您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】将一定量的H2O(g)和CO(g)分别通入到一体积为2 L的恒容密闭容器中进行反应:H2O(g)+CO(g)CO2(g)+H2(g),得到以下三组数据,据此回答下列问题:
(1)①由以上数据,实验1中以v(CO2)表示反应速率为_______ ,以α(CO)表示转化率为_____ 。
②该反应在650℃时平衡常数数值为_________ ,该反应的逆反应为_________ (填“吸”或“放”)热反应。
③若实验3和实验2中CO的百分含量相同,且t<3 min,则a、b应满足的关系是_______ 。
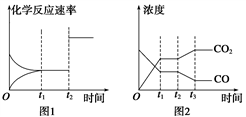
(2)下图1、2表示上述反应在时刻t1达到平衡,在时刻t2因改变某个条件而发生变化的情况:
①图1中时刻t2发生改变的条件可能是____________ (写一条即可,下同)。
②图2中时刻t2发生改变的条件可能是______________________________________ 。
(3)在850 ℃时,其平衡常数K=1,850 ℃时在该容器中同时充入1.0 mol CO、3.0 mol H2O、1.0 mol CO2、5.0 mol H2,此时反应向________ (填“正反应”或“逆反应”)方向进行,平衡时CO2的物质的量为__________ 。
| 实验组 | 温度 | 起始量 | 平衡量 | 达到平衡所需时间 | ||
| H2O | CO | H2 | CO | |||
| 1 | 650℃ | 1 mol | 2 mol | 0.8 mol | 1.2 mol | 5 min |
| 2 | 900℃ | 0.5 mol | 1 mol | 0.2 mol | 0.8 mol | 3 min |
| 3 | 900℃ | a | b | c | d | t |
(1)①由以上数据,实验1中以v(CO2)表示反应速率为
②该反应在650℃时平衡常数数值为
③若实验3和实验2中CO的百分含量相同,且t<3 min,则a、b应满足的关系是
(2)下图1、2表示上述反应在时刻t1达到平衡,在时刻t2因改变某个条件而发生变化的情况:
①图1中时刻t2发生改变的条件可能是
②图2中时刻t2发生改变的条件可能是
(3)在850 ℃时,其平衡常数K=1,850 ℃时在该容器中同时充入1.0 mol CO、3.0 mol H2O、1.0 mol CO2、5.0 mol H2,此时反应向
您最近一年使用:0次



