(1)下列物质能导电的是________ ,属于电解质的是_________ 。
①NaOH固体 ②液态SO2 ③液态醋酸 ④液态金属钠
⑤BaSO4固体 ⑥纯蔗糖(C12H22O11) ⑦氨水 ⑧融化的KNO3
(2)按要求写出下列方程式:
①钠与水反应的离子方程式:__________________________
②将NaHSO4溶液逐滴加入到Ba(OH)2溶液中,当Ba2+恰好沉淀完全时的离子方程式为:_________________
(3)根据离子方程式,写出一个符合条件的化学方程式
CaO+2H+=Ca2++H2O_________________
(4)今有K2SO4和Al2(SO4)3的混合溶液,其中K+物质的量浓度是0.2mol·L-1,SO42-物质的量浓度是0.7mol·L-1。则混合溶液中Al3+物质的量浓度应等于________
①NaOH固体 ②液态SO2 ③液态醋酸 ④液态金属钠
⑤BaSO4固体 ⑥纯蔗糖(C12H22O11) ⑦氨水 ⑧融化的KNO3
(2)按要求写出下列方程式:
①钠与水反应的离子方程式:
②将NaHSO4溶液逐滴加入到Ba(OH)2溶液中,当Ba2+恰好沉淀完全时的离子方程式为:
(3)根据离子方程式,写出一个符合条件的化学方程式
CaO+2H+=Ca2++H2O
(4)今有K2SO4和Al2(SO4)3的混合溶液,其中K+物质的量浓度是0.2mol·L-1,SO42-物质的量浓度是0.7mol·L-1。则混合溶液中Al3+物质的量浓度应等于
更新时间:2016-12-09 09:54:39
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】已知下列物质:①CO2②Mg③NaHSO4溶液④CaCO3⑤NaOH溶液⑥NH3•H2O⑦乙醇⑧盐酸
(1)属于电解质的有___________ (填序号下同),属于非电解质的有___________
(2)能导电的有___________
(3)写出⑥的电离方程式:___________
(4)写出③与⑤发生反应的离子方程式:___________
(5)已知①与②发生反应的化学方程式为 ,请用双线桥标出该反应的电子转移方向和数目:
,请用双线桥标出该反应的电子转移方向和数目:___________
(1)属于电解质的有
(2)能导电的有
(3)写出⑥的电离方程式:
(4)写出③与⑤发生反应的离子方程式:
(5)已知①与②发生反应的化学方程式为
 ,请用双线桥标出该反应的电子转移方向和数目:
,请用双线桥标出该反应的电子转移方向和数目:
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐2】(1)一个12C原子质量为ag, 有一种X原子的质量为bg.设NA为阿伏加德罗常数,则X的相对原子质量可表示为:_______________
(2)现有下列物质:①氢氧化钾固体 ②稀硫酸 ③铜片 ④蔗糖 (C12H22O11) 固体 ⑤熔融的氯化钠。
用以上物质的序号填空:属于电解质的是_______________ ,属于非电解质的是____________ ;所给状态下能够导电的是______________ 。
(3)反应(未配平):BrF3+H2O-Br2+O2+HBrO3+HF已知生成物中Br2与O2的物质的量之比为1:1。则:
①配平后H2O 与HF物质的量之比为________ ;
②还原剂为_________________ ;
③如有5molH2O参加反应则参加氧化还原反应的H2O物质的量为_________ mol
(2)现有下列物质:①氢氧化钾固体 ②稀硫酸 ③铜片 ④蔗糖 (C12H22O11) 固体 ⑤熔融的氯化钠。
用以上物质的序号填空:属于电解质的是
(3)反应(未配平):BrF3+H2O-Br2+O2+HBrO3+HF已知生成物中Br2与O2的物质的量之比为1:1。则:
①配平后H2O 与HF物质的量之比为
②还原剂为
③如有5molH2O参加反应则参加氧化还原反应的H2O物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】现有七种物质:①铜 ②CaO ③CO2 ④NaOH ⑤NaHCO3 ⑥氨水 ⑦FeCl3溶液。
(1)以上能导电的是_________ ,属于电解质的是_______ 。
(2)⑥的电离方程式为_________ 。
(3)④和⑤反应的离子方程式为__________ 。
(4)①与⑦发生反应的化学方程式为:________ 。
(1)以上能导电的是
(2)⑥的电离方程式为
(3)④和⑤反应的离子方程式为
(4)①与⑦发生反应的化学方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】按要求书写离子方程式:
(1)向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性_____________________________
(2)向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO42﹣恰好完全沉淀_________________
(3)重铬酸铵[(NH4)2Cr2O7]受热发生氧化还原反应,下列各组重铬酸铵受热分解产物的判断符合实际的是__________
A.CrO3+NH3+H2O B.Cr2O3+NH3+H2O
C.CrO3+N2+H2O D.Cr2O3+N2+H2O
(4)取300mL 0.2mol/L的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,KMnO4被还原成Mn2+,消耗KMnO4物质的量为__________ 。
(1)向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性
(2)向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO42﹣恰好完全沉淀
(3)重铬酸铵[(NH4)2Cr2O7]受热发生氧化还原反应,下列各组重铬酸铵受热分解产物的判断符合实际的是
A.CrO3+NH3+H2O B.Cr2O3+NH3+H2O
C.CrO3+N2+H2O D.Cr2O3+N2+H2O
(4)取300mL 0.2mol/L的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,KMnO4被还原成Mn2+,消耗KMnO4物质的量为
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐2】元素周期表中第三周期元素的单质及其化合物的用途广泛。
(1)该周期元素中,半径最小的简单离子的离子结构示意图为___________________ 。
(2)能证明氯的非金属性(得电子能力)比硫强的化学方程式为_____________ 。
(3)NaHSO3溶液呈酸性,其溶液中离子浓度由大到小的顺序为______________ 。
(4)ClO2可将弱酸性废水中的Mn2+转化为MnO2而除去,同时ClO2被还原为Cl—,该反应的离子方程式为_______________________________ 。
(5)已知下列两反应过程中能量变化如图所示:
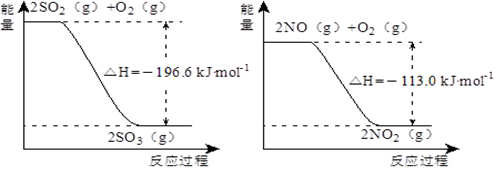
汽车尾气中含有的少量NO2和SO2在一定条件下会发生反应,该反应的热化学方程式为____________ 。
(1)该周期元素中,半径最小的简单离子的离子结构示意图为
(2)能证明氯的非金属性(得电子能力)比硫强的化学方程式为
(3)NaHSO3溶液呈酸性,其溶液中离子浓度由大到小的顺序为
(4)ClO2可将弱酸性废水中的Mn2+转化为MnO2而除去,同时ClO2被还原为Cl—,该反应的离子方程式为
(5)已知下列两反应过程中能量变化如图所示:
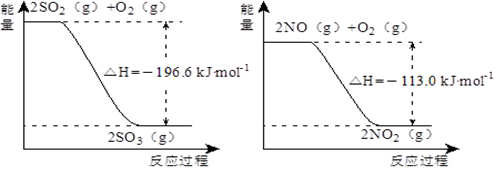
汽车尾气中含有的少量NO2和SO2在一定条件下会发生反应,该反应的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】二氧化氯(ClO2)气体是一种常用的高效自来水消毒剂。
(1)KClO3和浓盐酸在一定温度下反应会生成ClO2和Cl2,反应方程式为___________ 。
(2)实验室常用KClO3、草酸(H2C2O4)和稀硫酸制备ClO2。该反应中氧化产物与还原产物物质的量之比为___________ 。
(3)将ClO2通入到硫化氢溶液中,然后加入少量的稀盐酸酸化的氯化钡溶液,发现有白色沉淀生成,写出二氧化氯与硫化氢溶液反应的离子方程式___________ 。
(4)自来水厂用ClO2处理后的水中,要求ClO2的浓度在0.1-0.8 mol/L之间,用碘量法可以检测水中ClO2的浓度(不同pH环境中粒子种类如图所示),步骤如下:

I.取一定体积的水样,加入一定量的碘化钾,再将反应后溶液调至中性,并加入淀粉溶液,溶液变蓝。
II.加入一定量的Na2S2O3溶液;(已知: )
)
III.加硫酸调节水样pH至1~3。
请回答:
①作I中反应的离子方程式是___________ 。
②在操作III过程中,溶液又呈蓝色,反应的离子方程式是___________ 。
③若水样的体积为1.0 L,在操作II时消耗了1.0×10-3 mol/L的Na2S2O3溶液10 mL,则水样中Cl2O的浓度是___________ mol/L。
(1)KClO3和浓盐酸在一定温度下反应会生成ClO2和Cl2,反应方程式为
(2)实验室常用KClO3、草酸(H2C2O4)和稀硫酸制备ClO2。该反应中氧化产物与还原产物物质的量之比为
(3)将ClO2通入到硫化氢溶液中,然后加入少量的稀盐酸酸化的氯化钡溶液,发现有白色沉淀生成,写出二氧化氯与硫化氢溶液反应的离子方程式
(4)自来水厂用ClO2处理后的水中,要求ClO2的浓度在0.1-0.8 mol/L之间,用碘量法可以检测水中ClO2的浓度(不同pH环境中粒子种类如图所示),步骤如下:

I.取一定体积的水样,加入一定量的碘化钾,再将反应后溶液调至中性,并加入淀粉溶液,溶液变蓝。
II.加入一定量的Na2S2O3溶液;(已知:
 )
)III.加硫酸调节水样pH至1~3。
请回答:
①作I中反应的离子方程式是
②在操作III过程中,溶液又呈蓝色,反应的离子方程式是
③若水样的体积为1.0 L,在操作II时消耗了1.0×10-3 mol/L的Na2S2O3溶液10 mL,则水样中Cl2O的浓度是
您最近一年使用:0次



