用钠、镁、铝分别与盐酸反应填写下面几种情况的空白:
(1)称取相同质量的钠镁铝,然后分别与足量盐酸反应,则产生的氢气在通常条件下的体积之比为_____________ 。
(2)取相同物质的量的钠镁铝,分别与足量盐酸反应,则产生氢气质量之比为_________ 。
(3)如果要制取相同体积的氢气(同温同压下),与足量的盐酸分别反应时所消耗的钠镁铝的质量之比为________ ;物质的量之比为___________ 。
(1)称取相同质量的钠镁铝,然后分别与足量盐酸反应,则产生的氢气在通常条件下的体积之比为
(2)取相同物质的量的钠镁铝,分别与足量盐酸反应,则产生氢气质量之比为
(3)如果要制取相同体积的氢气(同温同压下),与足量的盐酸分别反应时所消耗的钠镁铝的质量之比为
15-16高一上·江西抚州·阶段练习 查看更多[2]
更新时间:2016-12-09 02:00:24
|
【知识点】 化学方程式计算中物质的量的运用解读
相似题推荐
计算题
|
适中
(0.65)
【推荐1】实验室常用的某盐酸试剂瓶的标签上的有关数据如下图,试根据标签上的有关数据进行计算:
(1)计算该浓盐酸中HCl的物质的量浓度为_____________ 。
(2)计算欲配制480mL 0.20mol/L的稀盐酸溶液,需要取上述浓盐酸的体积为_____________ 。
(3)实验室用上述浓盐酸与二氧化锰反应制取氯气,若制得0.56L(标准状况)氯气,计算被氧化的HCl的物质的量为_____________ ,转移电子的物质的量为_____________ 。
盐酸 分子式:  相对分子质量 : 36.5 密度 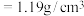  的质量分数: 的质量分数: 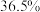 |
(1)计算该浓盐酸中HCl的物质的量浓度为
(2)计算欲配制480mL 0.20mol/L的稀盐酸溶液,需要取上述浓盐酸的体积为
(3)实验室用上述浓盐酸与二氧化锰反应制取氯气,若制得0.56L(标准状况)氯气,计算被氧化的HCl的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】把5.1 g铝镁合金的粉末放入100 mL某盐酸中,恰好完全反应,标准状况下收集到5.6 L H2。试计算(注意:无计算过程不给分):
(1)该盐酸的物质的量浓度是多少?_____________
(2)该合金中铝的质量为多少克?_____________
(1)该盐酸的物质的量浓度是多少?
(2)该合金中铝的质量为多少克?
您最近一年使用:0次



