下图是一个化学过程的示意图。
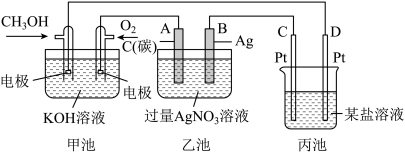
(1)图中甲池中OH-移向_________ 极(填“CH3OH”或“O2”)。
(2)写出通入CH3OH的电极的电极反应式:_____________________ 。
(3)向乙池两电极附近滴加适量紫色石蕊试液,附近变红的电极为___________ 极(填“A”或"B”),并写出此电极的反应式:________________________ 。
(4)乙池中总反应的离子方程式:_________________________ 。
(5)当乙池中B(Ag)极的质量增加5.4g时,乙池的pH是_______________ (若此时乙池中溶液的体积为500mL);此时丙池某电极析出1.60g某金属,则丙中的某盐溶液可能是__________ (填序号)。

(1)图中甲池中OH-移向
(2)写出通入CH3OH的电极的电极反应式:
(3)向乙池两电极附近滴加适量紫色石蕊试液,附近变红的电极为
(4)乙池中总反应的离子方程式:
(5)当乙池中B(Ag)极的质量增加5.4g时,乙池的pH是
| A.MgSO4 | B.CuSO4 | C.AgNO3 | D.AlCl3 |
更新时间:2016-12-09 10:07:42
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】某课外小组用如图装置进行实验,试回答下列问题:

(1)若开始时开关K与a连接,则B极的电极反应式是______ 。
(2)若开始时开关K与b连接,则B极的电极反应式是______ 。上述实验进行一段时间后,需向U形管中______ ,才能使电解质恢复原浓度。
(3)该小组同学认为,可以模拟工业上离子交换膜法制烧碱的方法,利用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。

①该电解池的阳极反应式为______ ,此时通过阴离子交换膜的离子数______ (填“大于”“小于”或“等于”)通过阳离子交换膜的离子数。
②制得的KOH溶液从出口______ (填“A”“B”“C”或“D”)导出。
③若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池,则电池正极的反应式为______ 。

(1)若开始时开关K与a连接,则B极的电极反应式是
(2)若开始时开关K与b连接,则B极的电极反应式是
(3)该小组同学认为,可以模拟工业上离子交换膜法制烧碱的方法,利用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。

①该电解池的阳极反应式为
②制得的KOH溶液从出口
③若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池,则电池正极的反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
(1)电化学法也可合成氨。如图是用低温固体质子导体作为电解质,用Pt−C3N4作阴极催化剂电解H2(g)和N2(g)合成NH3的原理示意图如图所示。

①Pt−C3N4电极反应产生NH3的电极反应式_______ 。
②该装置使用甲醇(CH3OH)燃料电池(电解质溶液为KOH)作为电源,写出负极的电极反应_______ 。
(2)某学习小组设想利用A装置电解制备绿色硝化剂N2O5,装置如图(c、d为惰性电极)。已知:无水硝酸可在液态N2O4中发生微弱电离。

①A装置中通入SO2一极的电极反应式为_______ 。
②写出生成N2O5的电极反应式_______ 。
(1)电化学法也可合成氨。如图是用低温固体质子导体作为电解质,用Pt−C3N4作阴极催化剂电解H2(g)和N2(g)合成NH3的原理示意图如图所示。

①Pt−C3N4电极反应产生NH3的电极反应式
②该装置使用甲醇(CH3OH)燃料电池(电解质溶液为KOH)作为电源,写出负极的电极反应
(2)某学习小组设想利用A装置电解制备绿色硝化剂N2O5,装置如图(c、d为惰性电极)。已知:无水硝酸可在液态N2O4中发生微弱电离。

①A装置中通入SO2一极的电极反应式为
②写出生成N2O5的电极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】以二甲醚( )-空气碱性燃料电池为电源进行如下实验,装置如图所示。用装置C精炼粗铜。已知:二甲醚–空气碱性燃料电池的总反应为
)-空气碱性燃料电池为电源进行如下实验,装置如图所示。用装置C精炼粗铜。已知:二甲醚–空气碱性燃料电池的总反应为 。
。

回答下列问题:
(1)装置A为___________ (填“原电池”或“电解池”),X极的电极名称为___________ (填“正极”、“负极”、“阴极”、“阳极”,下同),b极名称为___________ 。
(2)b极附近可能的现象是___________ 。
(3)a极上发生___________ (填“氧化”或“还原”)反应,其电极反应式为___________ 。
(4)若装置A中消耗标准状况下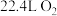 ,则理论上装置C中可得纯铜的质量为
,则理论上装置C中可得纯铜的质量为___________ g。
 )-空气碱性燃料电池为电源进行如下实验,装置如图所示。用装置C精炼粗铜。已知:二甲醚–空气碱性燃料电池的总反应为
)-空气碱性燃料电池为电源进行如下实验,装置如图所示。用装置C精炼粗铜。已知:二甲醚–空气碱性燃料电池的总反应为 。
。
回答下列问题:
(1)装置A为
(2)b极附近可能的现象是
(3)a极上发生
(4)若装置A中消耗标准状况下
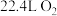 ,则理论上装置C中可得纯铜的质量为
,则理论上装置C中可得纯铜的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】良好生态环境是最普惠的民生福祉。治理大气污染物CO、NOX、SO2具有十分重要的意义。
(1)氧化还原法消除NOX的转化如下所示: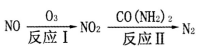 。反应I为NO+O3===NO2+O2,其还原产物是
。反应I为NO+O3===NO2+O2,其还原产物是_________ 。反应Ⅱ中,氧化剂与还原剂的物质的量之比为__________ 。
(2)吸收SO2和NO获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素)。

装置Ⅱ中,酸性条件下NO被Ce4+氧化的产物主要是NO3-和NO2-,请写出生成等物质的量的NO3-和NO2-时的离子方程式_______________ 。装置III中发生反应的离子方程式为_________________ 。
(3)已知进入装置IV的溶液中NO2-的浓度为a mol·L-1,要使1L该溶液中NO2-完全转化为NH4NO3,至少需向装置IV中通入标准状况下的氧气____ L(用含a代数式表示)。
(1)氧化还原法消除NOX的转化如下所示:
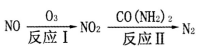 。反应I为NO+O3===NO2+O2,其还原产物是
。反应I为NO+O3===NO2+O2,其还原产物是(2)吸收SO2和NO获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素)。

装置Ⅱ中,酸性条件下NO被Ce4+氧化的产物主要是NO3-和NO2-,请写出生成等物质的量的NO3-和NO2-时的离子方程式
(3)已知进入装置IV的溶液中NO2-的浓度为a mol·L-1,要使1L该溶液中NO2-完全转化为NH4NO3,至少需向装置IV中通入标准状况下的氧气
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】利用所学电化学反应原理,解决以下问题:
(1)如图是电解未知浓度的硝酸银溶液的示意图,请根据要求答题。

①Fe电极叫做____ 极,C电极的反应式为____ 。
②当某电极的固体质量增重21.6g时,整个装置共产生气体(标准状况下)体积2.24L,推断该气体的组成____ 。
(2)图中甲池的总反应式为____ 。
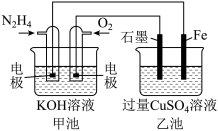
①甲池中负极上的电极反应式为____ 。
②乙池中石墨电极上发生的反应为____ 。
③要使乙池恢复到电解前的状态,应向溶液中加入适量的____ 。
A.CuOB.Cu(OH)2C.CuCO3D.CuSO4
(3)某科研小组用SO2为原料制取硫酸。
①利用原电池原理,用SO2、O2和H2O来制备硫酸,该电池用多孔材料作电极,它能吸附气体,同时也能使气体与电解质溶液充分接触。请写出该电池负极的电极反应式:____ 。
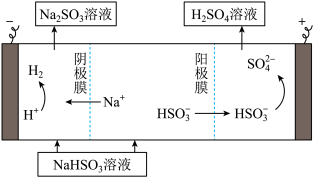
②用Na2SO3溶液充分吸收SO2得NaHSO3溶液,然后电解该溶液可制得硫酸。电解原理示意图如图。请写出开始时阳极反应的电极反应式:____ 。
(1)如图是电解未知浓度的硝酸银溶液的示意图,请根据要求答题。

①Fe电极叫做
②当某电极的固体质量增重21.6g时,整个装置共产生气体(标准状况下)体积2.24L,推断该气体的组成
(2)图中甲池的总反应式为

①甲池中负极上的电极反应式为
②乙池中石墨电极上发生的反应为
③要使乙池恢复到电解前的状态,应向溶液中加入适量的
A.CuOB.Cu(OH)2C.CuCO3D.CuSO4
(3)某科研小组用SO2为原料制取硫酸。
①利用原电池原理,用SO2、O2和H2O来制备硫酸,该电池用多孔材料作电极,它能吸附气体,同时也能使气体与电解质溶液充分接触。请写出该电池负极的电极反应式:
②用Na2SO3溶液充分吸收SO2得NaHSO3溶液,然后电解该溶液可制得硫酸。电解原理示意图如图。请写出开始时阳极反应的电极反应式:

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】按要求回答下列问题。
I.现有以下物质:①NaCl晶体②SO2③液态醋酸④铜⑤固体BaSO4⑥纯蔗糖(C12H22O11)⑦酒精(C2H5OH)⑧熔化的KHSO4⑨氨水⑩液氯。请回答下列问题。(填相应序号)
(1)以上物质能导电的是_______ ;
(2)以上物质属于强电解质的是_______ ;
II.铜是与人类关系非常密切的有色金属。已知:常温下,在溶液中Cu2+稳定,Cu+易在酸性条件下发生反应:Cu+=Cu2++Cu。大多数+1价铜的化合物是难溶物,Cu2O、CuI、CuCl、CuH等。
(3)在CuCl2溶液中逐滴加入过量KI溶液可能发生以下反应:
a.2Cu2++4I-=2CuI↓(白色)+I2
b.2Cu2++2Cl-+2I-=2CuCl↓(白色)+I2
为顺利观察到白色沉淀可以加入的最佳试剂是_______。
(4)一定条件下,在CuSO4中加入NH5反应生成氢化亚铜(CuH)。写出CuH在过量稀盐酸中有气体生成的离子方程式:_______ 。
(5)纳米级Cu2O具有特殊的光学、电学及光电化学性质,在太阳能电池、传感器、超导体等方面有着潜在的应用,研究制备纳米氧化亚铜的方法已成为当前的热点研究之一。以铜作阳极,石墨作阴极电解。已知:铜作阳极时,铜先被氧化生成Cu+,后Cu+继续氧化生成Cu2+;在碱性溶液中CuCl浊液易转化为Cu2O。
①以NaOH溶液作为电解质溶液时需添加NaCl,其目的是_______ ,写出阳极反应式:_______ 。
②写出在碱性溶液中CuCl浊液转化为Cu2O的离子方程式:_______ 。
I.现有以下物质:①NaCl晶体②SO2③液态醋酸④铜⑤固体BaSO4⑥纯蔗糖(C12H22O11)⑦酒精(C2H5OH)⑧熔化的KHSO4⑨氨水⑩液氯。请回答下列问题。(填相应序号)
(1)以上物质能导电的是
(2)以上物质属于强电解质的是
II.铜是与人类关系非常密切的有色金属。已知:常温下,在溶液中Cu2+稳定,Cu+易在酸性条件下发生反应:Cu+=Cu2++Cu。大多数+1价铜的化合物是难溶物,Cu2O、CuI、CuCl、CuH等。
(3)在CuCl2溶液中逐滴加入过量KI溶液可能发生以下反应:
a.2Cu2++4I-=2CuI↓(白色)+I2
b.2Cu2++2Cl-+2I-=2CuCl↓(白色)+I2
为顺利观察到白色沉淀可以加入的最佳试剂是_______。
| A.SO2 | B.苯 | C.NaOH溶液 | D.乙醇 |
(5)纳米级Cu2O具有特殊的光学、电学及光电化学性质,在太阳能电池、传感器、超导体等方面有着潜在的应用,研究制备纳米氧化亚铜的方法已成为当前的热点研究之一。以铜作阳极,石墨作阴极电解。已知:铜作阳极时,铜先被氧化生成Cu+,后Cu+继续氧化生成Cu2+;在碱性溶液中CuCl浊液易转化为Cu2O。
①以NaOH溶液作为电解质溶液时需添加NaCl,其目的是
②写出在碱性溶液中CuCl浊液转化为Cu2O的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极.
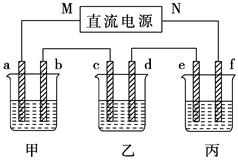
接通电源,经过一段时间后,乙中c电极质量增加16g.据此回答问题:
(1)电源的N端为_________ 极;
(2)电极b上发生的电极反应为___________ ;
(3)列式计算电极a上生成的气体在标准状况下的体积:_____________ L;
(4)丙中K2SO4质量分数将变为___________ 。

接通电源,经过一段时间后,乙中c电极质量增加16g.据此回答问题:
(1)电源的N端为
(2)电极b上发生的电极反应为
(3)列式计算电极a上生成的气体在标准状况下的体积:
(4)丙中K2SO4质量分数将变为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】应用电化学原理,解决下列问题:

(1)装置1为铁的吸氧腐蚀实验。一段时间后,向插入铁钉的玻璃筒内滴入K3[Fe(CN)6]溶液,即可观察到的现象是_____ ,表明铁被氧化。
(2)装置2中的石墨是_____ 极(填“正”或“负”),该装置发生的总反应的离子方程式为_____ 。
(3)装置3中甲烧杯盛放100mL0.2mol/L的NaCl溶液,乙烧杯盛放100mL0.5mol/L的CuSO4溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞,观察到石墨电极附近首先变红,回答下列问题:
①甲烧杯中铁电极的电极反应为_____ 。
②乙烧杯中电解反应的离子方程式为_____ 。
③停止电解,取出Cu电极,洗涤、干燥、称量、电极增重0.64g,甲烧杯中产生的气体(标准状况下)体积为_____ mL。

(1)装置1为铁的吸氧腐蚀实验。一段时间后,向插入铁钉的玻璃筒内滴入K3[Fe(CN)6]溶液,即可观察到的现象是
(2)装置2中的石墨是
(3)装置3中甲烧杯盛放100mL0.2mol/L的NaCl溶液,乙烧杯盛放100mL0.5mol/L的CuSO4溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞,观察到石墨电极附近首先变红,回答下列问题:
①甲烧杯中铁电极的电极反应为
②乙烧杯中电解反应的离子方程式为
③停止电解,取出Cu电极,洗涤、干燥、称量、电极增重0.64g,甲烧杯中产生的气体(标准状况下)体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氮肥的大量使用排出的废水是造成河流及湖泊富营养化的主要因素之一、氨氮废水中的氮元素多以 和
和 等形式存在。电解法处理氨氮酸性废水已引起广泛关注。研究表明,当以碳为阴极,
等形式存在。电解法处理氨氮酸性废水已引起广泛关注。研究表明,当以碳为阴极, 可在阴极生成
可在阴极生成 ,并进一步生成电中性且氧化性极强的羟基自由基(・OH),
,并进一步生成电中性且氧化性极强的羟基自由基(・OH), 可以将氨氮氧化为N2。
可以将氨氮氧化为N2。
1.写出 的电子式
的电子式___________ 。
2.阴极生成H2O2的电极反应为:___________ 。氨氮氧化生成2.24LN2(标准状况),转移电子数为:___________ 。
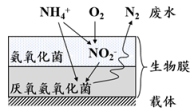
3.生物膜式厌氧氨氧化是一种较先进的氨氮废水处理工艺,通过在填料上附着不同菌种的生物膜来实现低能耗脱氨氮,其过程如图所示。___________ 。
 和
和 等形式存在。电解法处理氨氮酸性废水已引起广泛关注。研究表明,当以碳为阴极,
等形式存在。电解法处理氨氮酸性废水已引起广泛关注。研究表明,当以碳为阴极, 可在阴极生成
可在阴极生成 ,并进一步生成电中性且氧化性极强的羟基自由基(・OH),
,并进一步生成电中性且氧化性极强的羟基自由基(・OH), 可以将氨氮氧化为N2。
可以将氨氮氧化为N2。1.写出
 的电子式
的电子式2.阴极生成H2O2的电极反应为:
3.生物膜式厌氧氨氧化是一种较先进的氨氮废水处理工艺,通过在填料上附着不同菌种的生物膜来实现低能耗脱氨氮,其过程如图所示。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】电化学原理广泛应用于日常生活、生产和科学技术等方面,以满足不同的需要。根据如图所示实验装置,分别回答下列问题:
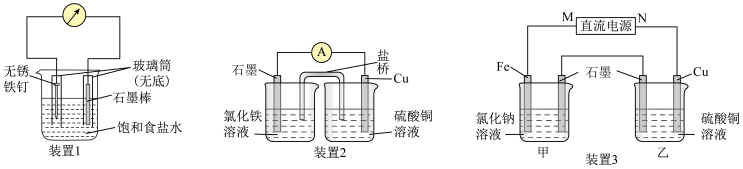
(1)装置1中无锈铁钉电极的电极反应式为_______ 。
(2)装置2中的石墨电极上发生_______ 反应,该装置发生的总反应的离子方程式为_______ 。
(3)装置3中甲烧杯盛放 的
的 溶液,乙烧杯盛放
溶液,乙烧杯盛放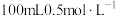 的
的 的溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞试液,观察到石墨极附近首先变红。
的溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞试液,观察到石墨极附近首先变红。
①电源的M端为_______ ,铁电极的质量会_______ (填“增加”、“减小”或“不变”)。
②乙烧杯中电解反应的离子方程式为_______ 。
③停止电解,取出Cu电极,洗涤、干燥、称量,电极增重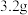 ,则甲烧杯中产生的气体在标准状况下的体积为
,则甲烧杯中产生的气体在标准状况下的体积为_______ 。
(4)装置4为甲烷燃料电池的构造示意图。正极的电极反应式为_______ 。
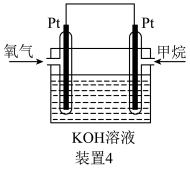

(1)装置1中无锈铁钉电极的电极反应式为
(2)装置2中的石墨电极上发生
(3)装置3中甲烧杯盛放
 的
的 溶液,乙烧杯盛放
溶液,乙烧杯盛放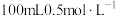 的
的 的溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞试液,观察到石墨极附近首先变红。
的溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞试液,观察到石墨极附近首先变红。①电源的M端为
②乙烧杯中电解反应的离子方程式为
③停止电解,取出Cu电极,洗涤、干燥、称量,电极增重
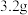 ,则甲烧杯中产生的气体在标准状况下的体积为
,则甲烧杯中产生的气体在标准状况下的体积为(4)装置4为甲烷燃料电池的构造示意图。正极的电极反应式为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】如图是一个化学过程的示意图.已知甲池的总反应式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O

(1)请回答图中甲、乙两池的名称.甲池是______ 装置,乙池是 ______ 装置;
(2)请回答下列电极的名称:通入CH3OH的电极名称是______ ,B(石墨)电极的名称是 ______ ;
(3)通入O2的电极的电极反应式为:______ ,A (Fe)电极的电极反应式为 ______ ;
(4)乙池中反应的化学方程式为______ ;
(5)电解一段时间后,乙池中A(Fe)极的质量增加5.4g时,且溶液的体积为500mL,求所得溶液在25℃时的pH=______ ,甲池中消耗O2为 ______ mL(标准状况下).
(6)钴铁氧体(CoFe2O4)不仅是重要的磁性材料、磁致伸缩材料,还是重要的锂离子电池负极材料。工业上,用电化学法制得CoFe2O4。以NaOH溶液作电解液,纯净的钴铁合金(CoFe2)作阳极进行电解,在阳极上获得CoFe2O4薄膜。该电解过程的化学方程式为_________________________ 。

(1)请回答图中甲、乙两池的名称.甲池是
(2)请回答下列电极的名称:通入CH3OH的电极名称是
(3)通入O2的电极的电极反应式为:
(4)乙池中反应的化学方程式为
(5)电解一段时间后,乙池中A(Fe)极的质量增加5.4g时,且溶液的体积为500mL,求所得溶液在25℃时的pH=
(6)钴铁氧体(CoFe2O4)不仅是重要的磁性材料、磁致伸缩材料,还是重要的锂离子电池负极材料。工业上,用电化学法制得CoFe2O4。以NaOH溶液作电解液,纯净的钴铁合金(CoFe2)作阳极进行电解,在阳极上获得CoFe2O4薄膜。该电解过程的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】一氧化氮—空气质子交换膜燃料电池将化学能转化为电能,实现了制硝酸、发电环保三位一体的结合。如图所示,某同学设计用该电池探究将雾霾中的SO2、NO转化为 的原理和粗铜的精炼原理。
的原理和粗铜的精炼原理。
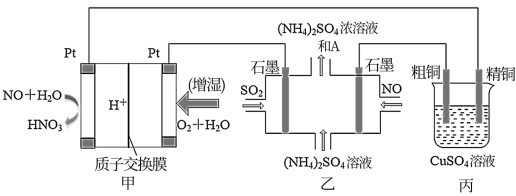
(1)燃料电池放电过程中正极的电极反应式________ 。
(2)乙装置中物质A是________ (填化学式),该装置电解过程阴极的电极反应式________ 。
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,CuSO4溶液的浓度将________ (填“增大”、“减小”或“不变”)。
(4)若在标准状况下,甲装置有22.4 L O2参加反应,则乙装置中转化SO2和NO的物质试的量共有________ mol;丙装置中阴极析出的质量为________ g。
 的原理和粗铜的精炼原理。
的原理和粗铜的精炼原理。
(1)燃料电池放电过程中正极的电极反应式
(2)乙装置中物质A是
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,CuSO4溶液的浓度将
(4)若在标准状况下,甲装置有22.4 L O2参加反应,则乙装置中转化SO2和NO的物质试的量共有
您最近一年使用:0次



