工业上,向500℃~600℃的铁屑中通入氯气生产无水氯化铁(已知炽热铁屑与氯化氢生成氯化亚铁)。现用如图所示的装置模拟上述过程进行实验。
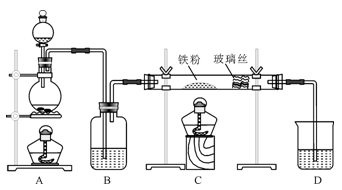
回答下列问题:
(1)盛装浓盐酸的仪器名称为_________ ,进行实验时,应先点燃__________ (选填A或C)处酒精灯。
(2)制取无水氯化铁的实验中,A中反应的离子方程式为_________ ,装置B中加入的试剂是_________ 。
(3)制取的无水氯化铁中混有少量氯化亚铁,其原因是____________ (化学方程式表示)。为除去氯气中混有的少量HCl,可以在装置A、B间加入装有______________ 的洗气瓶。
(4)工业上常用石灰乳吸收制氯气的尾气制得漂白粉,漂白粉的有效成分是_____________ (填化学式)。长期露置于空气中的漂白粉,加稀盐酸后产生的气体是_____________ (填数字代号)。
① O2 ② Cl2 ③ CO2 ④ HClO

回答下列问题:
(1)盛装浓盐酸的仪器名称为
(2)制取无水氯化铁的实验中,A中反应的离子方程式为
(3)制取的无水氯化铁中混有少量氯化亚铁,其原因是
(4)工业上常用石灰乳吸收制氯气的尾气制得漂白粉,漂白粉的有效成分是
① O2 ② Cl2 ③ CO2 ④ HClO
更新时间:2016-12-09 10:51:04
|
【知识点】 离子反应的发生及书写
相似题推荐
【推荐1】【化学——选修2:化学与技术】将海水淡化与浓海水资源化结合起来是综合利用海水的重要途径之一。一般是先将海水淡化获得淡水,再从剩余的浓海水中通过一系列工艺流程提取其他产品。
回答下列问题:
(1)下列改进和优化海水综合利用工艺的设想和做法可行的是________ (填序号)。
①用混凝法获取淡水 ②提高部分产品的质量
③优化提取产品的品种 ④改进钾、溴、镁等的提取工艺
(2)采用“空气吹出法”从浓海水吹出Br2,并用纯碱吸收。已知该反应不产生CO2,且溴歧化为Br-和BrO ,则反应的离子反应方程式为
,则反应的离子反应方程式为_______________________ 。
(3)海水提镁的一段工艺流程如下图:

浓海水的主要成分如下:
该工艺过程中,脱硫阶段主要反应的阳离子________ ,沉降阶段反应的离子方程式为_____ ,浓海水的利用率为90%,则1L浓海水最多可得到产品2的质量为________ g。
(4)由MgCl2·6H2O制备MgCl2固体时是在氯化氢气体氛围中加热进行,其目的是_________ 。
回答下列问题:
(1)下列改进和优化海水综合利用工艺的设想和做法可行的是
①用混凝法获取淡水 ②提高部分产品的质量
③优化提取产品的品种 ④改进钾、溴、镁等的提取工艺
(2)采用“空气吹出法”从浓海水吹出Br2,并用纯碱吸收。已知该反应不产生CO2,且溴歧化为Br-和BrO
 ,则反应的离子反应方程式为
,则反应的离子反应方程式为(3)海水提镁的一段工艺流程如下图:

浓海水的主要成分如下:
| 离子 | Na+ | Mg2+ | Cl- | SO42- |
| 浓度/(g·L-1) | 63.7 | 28.8 | 144.6 | 46.4 |
(4)由MgCl2·6H2O制备MgCl2固体时是在氯化氢气体氛围中加热进行,其目的是
您最近半年使用:0次
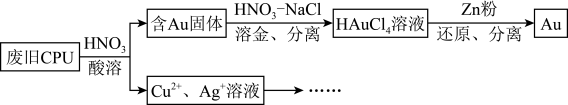
【推荐2】用如图方法回收废旧CPU中的单质Au(金),Ag和Cu。
(1)酸溶后经_______ 操作,将混合物分离。
(2)浓、稀 均可作酸溶试剂。溶解等量的Cu消耗
均可作酸溶试剂。溶解等量的Cu消耗 的物质的量不同,写出消耗
的物质的量不同,写出消耗 物质的量少的反应的化学方程式:
物质的量少的反应的化学方程式:_______ 。
(3)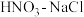 与王水[V(浓硝酸)∶V(浓盐酸)=1∶3]溶金原理相同。
与王水[V(浓硝酸)∶V(浓盐酸)=1∶3]溶金原理相同。
①将溶金反应的化学方程式补充完整:_________________ 。

②关于溶金的下列说法正确的是_______ 。
A.用到了HNO3的氧化性
B.王水中浓盐酸的主要作用是增强溶液的酸性
C.用浓盐酸与NaNO3也可使Au溶解
(4)若用Zn粉将溶液中的1 mol HAuCl4完全还原,则参加反应的Zn的物质的量是____ mol。

(1)酸溶后经
(2)浓、稀
 均可作酸溶试剂。溶解等量的Cu消耗
均可作酸溶试剂。溶解等量的Cu消耗 的物质的量不同,写出消耗
的物质的量不同,写出消耗 物质的量少的反应的化学方程式:
物质的量少的反应的化学方程式:(3)
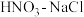 与王水[V(浓硝酸)∶V(浓盐酸)=1∶3]溶金原理相同。
与王水[V(浓硝酸)∶V(浓盐酸)=1∶3]溶金原理相同。①将溶金反应的化学方程式补充完整:

②关于溶金的下列说法正确的是
A.用到了HNO3的氧化性
B.王水中浓盐酸的主要作用是增强溶液的酸性
C.用浓盐酸与NaNO3也可使Au溶解
(4)若用Zn粉将溶液中的1 mol HAuCl4完全还原,则参加反应的Zn的物质的量是
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】实验室有五瓶标签已损坏的试剂,分别盛有碳酸钾溶液、稀硝酸、AgNO3溶液、盐酸、氯化钡溶液,为了确定各瓶中的试剂,现将它们任意编号为A、B、C、D、E,用试管各盛少量溶液多次进行两两混合反应,现象为:A与B、A与E产生沉淀,B与D、B与E产生沉淀,C与E、D与E产生气体,而C与D无明显现象。
(1)请推断出各试剂瓶中所盛试剂为(填写溶质的化学式):
A________ 、B________ 、C________ 、D________ 、E________ 。
(2)请写出B与E混合后反应的离子方程式:_________________________ 。
(1)请推断出各试剂瓶中所盛试剂为(填写溶质的化学式):
A
(2)请写出B与E混合后反应的离子方程式:
您最近半年使用:0次



