把10.2g镁铝合金的粉末放入过量的盐酸中,得到11.2L H2(标准状况下).试计算(写出计算过程):
(1)该合金中铝的质量分数;
(2)该合金中铝和镁的物质的量之比.
(1)该合金中铝的质量分数;
(2)该合金中铝和镁的物质的量之比.
更新时间:2016-12-09 10:51:44
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】在空气中加热10.98 g草酸钴晶体(CoC2O4·2H2O)样品,受热过程中不同温度范围内分别得到一种固体物质,其质量如表。
(1)加热到210 ℃时,固体物质的化学式为___________ 。
(2)经测定,加热到210~320 ℃过程中的生成物只有CO2和钴的氧化物,此过程发生反应的化学方程式为___________ 。
| 温度范围/℃ | 固体质量/g |
| 150~210 | 8.82 |
| 290~320 | 4.82 |
| 890~920 | 4.50 |
(2)经测定,加热到210~320 ℃过程中的生成物只有CO2和钴的氧化物,此过程发生反应的化学方程式为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】硅单质及其化合物应用范围很广。
(1)制备硅半导体材料必须先得到高纯硅,工业上可以按如下步骤制备纯硅:
Ⅰ.高温下用碳还原二氧化硅制得粗硅
Ⅱ.粗硅与干燥的氯气在450 ℃~500 ℃ 反应制得SiCl4
Ⅲ. SiCl4液体经精馏提纯后与过量H2在1100 ℃~1200 ℃ 反应制得纯硅
已知SiCl4沸点为57.6 ℃,能与H2O强烈反应。1 mol H2与SiCl4气体完全反应吸收的热量为120.2 kJ。请回答下列问题:
① 第Ⅰ步制备粗硅的化学反应方程式为_______________________________________ ,第Ⅲ步反应的热化学方程式是___________________________________________________ 。
②整个制备纯硅过程必须严格控制无水无氧。SiCl4在潮湿的空气中因水解而产生白色烟雾,其生成物是__________ ;H2还原SiCl4过程中若混O2,可能引起的后果是________ 。
(2)二氧化硅大量用于生产玻璃。工业上用SiO2、Na2CO3和CaCO3共283 kg在高温下完全反应时放出CO244 kg,生产出的玻璃可用化学式Na2SiO3·CaSiO3·xSiO2表示,则其中x=_________ 。
(1)制备硅半导体材料必须先得到高纯硅,工业上可以按如下步骤制备纯硅:
Ⅰ.高温下用碳还原二氧化硅制得粗硅
Ⅱ.粗硅与干燥的氯气在450 ℃~500 ℃ 反应制得SiCl4
Ⅲ. SiCl4液体经精馏提纯后与过量H2在1100 ℃~1200 ℃ 反应制得纯硅
已知SiCl4沸点为57.6 ℃,能与H2O强烈反应。1 mol H2与SiCl4气体完全反应吸收的热量为120.2 kJ。请回答下列问题:
① 第Ⅰ步制备粗硅的化学反应方程式为
②整个制备纯硅过程必须严格控制无水无氧。SiCl4在潮湿的空气中因水解而产生白色烟雾,其生成物是
(2)二氧化硅大量用于生产玻璃。工业上用SiO2、Na2CO3和CaCO3共283 kg在高温下完全反应时放出CO244 kg,生产出的玻璃可用化学式Na2SiO3·CaSiO3·xSiO2表示,则其中x=
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】在工业生产中要制取某种物质,除了要考虑反应进行的可能性,还要考虑原料来源、成本高低和设备要求等因素,以选取最适当的方法。例如,工业上制取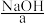 一般不采用
一般不采用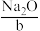 与
与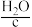 反应的方法(Na2O作为原料,来源少、成本高),而主要采用电解饱和食盐水的方法,过去也曾采用
反应的方法(Na2O作为原料,来源少、成本高),而主要采用电解饱和食盐水的方法,过去也曾采用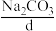 与
与 且2反应的方法。
且2反应的方法。
回答下列问题:
(1)Na与水反应的离子方程式为________ 。
(2)电解饱和食盐水的化学方程式为2NaCl+2H2O 2NaOH+H2↑+Cl2↑:
2NaOH+H2↑+Cl2↑:
①该反应中的还原剂为_______ (填化学式,下同),被氧化的物质为________ 。
②用单线桥法表示该反应中电子转移的方向和数目:_______ 。
③每生成0.2gH2,同时生成Cl2的质量为________  。
。
(3)d和e反应可制得a:
①碳酸钠的俗称为________ 。
②从碳酸钠组成的阴离子来看,其属于_______ 盐。
③将Na2CO3溶液加入澄清石灰水中,发生反应的离子方程式为_______ 。
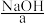 一般不采用
一般不采用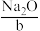 与
与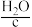 反应的方法(Na2O作为原料,来源少、成本高),而主要采用电解饱和食盐水的方法,过去也曾采用
反应的方法(Na2O作为原料,来源少、成本高),而主要采用电解饱和食盐水的方法,过去也曾采用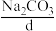 与
与 且2反应的方法。
且2反应的方法。回答下列问题:
(1)Na与水反应的离子方程式为
(2)电解饱和食盐水的化学方程式为2NaCl+2H2O
 2NaOH+H2↑+Cl2↑:
2NaOH+H2↑+Cl2↑:①该反应中的还原剂为
②用单线桥法表示该反应中电子转移的方向和数目:
③每生成0.2gH2,同时生成Cl2的质量为
 。
。(3)d和e反应可制得a:
①碳酸钠的俗称为
②从碳酸钠组成的阴离子来看,其属于
③将Na2CO3溶液加入澄清石灰水中,发生反应的离子方程式为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】将一定质量的镁铝合金投入100 mL一定物质的量浓度的盐酸中,合金全部溶解,向所得溶液中滴加5 mol/L的NaOH溶液至过量,生成沉淀的质量与加入的氢氧化钠溶液的体积关系如图所示。回答下列问题:

(1)当沉淀量达到最大值时,Al(OH)3的物质的量为________ 。
(2)原合金中Mg的质量为________ 。
(3)盐酸的物质的量浓度为________ 。

(1)当沉淀量达到最大值时,Al(OH)3的物质的量为
(2)原合金中Mg的质量为
(3)盐酸的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】一定量的Mg、Al的混合物中加入足量盐酸,产生标准状况下的气体5.6L,再在此溶液中加入过量NaOH溶液,产生沉淀5.8克,求:
(1)Mg、Al的物质的量各为多少_________ ?
(2)若将此混合物投入足量的NaOH溶液中,求标准状况下产生气体的体积_________ 。
(1)Mg、Al的物质的量各为多少
(2)若将此混合物投入足量的NaOH溶液中,求标准状况下产生气体的体积
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】把3.06 g铝和镁的混合物粉末放入100 mL盐酸中,恰好完全反应,并得到标准状况下3.36 LH2 计算:(要有过程)
(1)该合金中铝的物质的量_____ 。
(2)反应后溶液中Cl﹣的物质的量浓度(假定反应体积仍为100 mL)____ 。
(1)该合金中铝的物质的量
(2)反应后溶液中Cl﹣的物质的量浓度(假定反应体积仍为100 mL)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)分别取等质量的钠、铁、铝与足量的盐酸反应,在相同条件下产生氢气的体积比是________ 。
(2)分别取等物质的量的 钠、铁、铝与足量的盐酸反应,在相同条件下产生氢气的体积比是
钠、铁、铝与足量的盐酸反应,在相同条件下产生氢气的体积比是_____ 。
(3)分别取金属钠、铁、铝各1 mol,分别投入200 mL 1 mol·L-1盐酸中,在标准状况下产生氢气的体积比是___________ 。
(2)分别取等物质的量的
 钠、铁、铝与足量的盐酸反应,在相同条件下产生氢气的体积比是
钠、铁、铝与足量的盐酸反应,在相同条件下产生氢气的体积比是(3)分别取金属钠、铁、铝各1 mol,分别投入200 mL 1 mol·L-1盐酸中,在标准状况下产生氢气的体积比是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】有三种镁铝合金样品(组分比例不一定相同)①、②、③。小奉、小贤、小红三同学各取一种样品,对合金中镁的质量分数进行下列实验探究:
(1)小奉取样品①m1 g和过量的氢氧化钠溶液反应,然后过滤;再往滤液中通入过量的二氧化碳气体,将所得沉淀过滤、洗涤、烘干、灼烧,得到固体质量仍为m1 g。则合金中镁的质量分数为___________ 。(保留小数点后面2位)
(2)小贤取样品②m2 g和足量的稀硫酸反应,发现固体完全溶解,标准状况下得到气体体积为VL,则m2的取值范围是_________ 。(结果转化为最简分数)
(3)小红取不同质量的样品③分别和30 mL同浓度的盐酸反应,所取合金质量与产生气体的体积(标准状况下测定)如下所示:
求:I.盐酸的物质的量浓度_______
II.合金中镁的质量分数_______
III.要使c组实验后剩余合金中的铝恰好完全溶解,还需向容器中加入1.0 mol/L的氢氧化钠溶液多少mL_______ ?
(1)小奉取样品①m1 g和过量的氢氧化钠溶液反应,然后过滤;再往滤液中通入过量的二氧化碳气体,将所得沉淀过滤、洗涤、烘干、灼烧,得到固体质量仍为m1 g。则合金中镁的质量分数为
(2)小贤取样品②m2 g和足量的稀硫酸反应,发现固体完全溶解,标准状况下得到气体体积为VL,则m2的取值范围是
(3)小红取不同质量的样品③分别和30 mL同浓度的盐酸反应,所取合金质量与产生气体的体积(标准状况下测定)如下所示:
| 实验序号 | a | b | c |
| 合金质量(g) | 0.51 | 0.765 | 0.918 |
| 气体体积(mL) | 560 | 672 | 672 |
求:I.盐酸的物质的量浓度
II.合金中镁的质量分数
III.要使c组实验后剩余合金中的铝恰好完全溶解,还需向容器中加入1.0 mol/L的氢氧化钠溶液多少mL
您最近一年使用:0次

 一定浓度的盐酸中,合金完全溶解。向所得溶液中滴加浓度为
一定浓度的盐酸中,合金完全溶解。向所得溶液中滴加浓度为 的
的 溶液,生成的沉淀跟加入的
溶液,生成的沉淀跟加入的 ,纵坐标质量单位是g)求:
,纵坐标质量单位是g)求: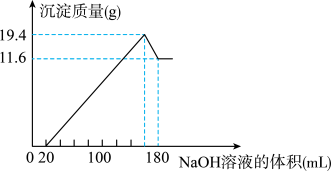
 ,
, 的质量
的质量 的物质的量浓度
的物质的量浓度

